
Wetenschap
Waarom zijn neon en andere edelgassen zo niet -reactief?
* Volledige buitenste schaal: Nobele gassen hebben een volledige buitenste schaal van elektronen, wat de meest stabiele elektronenconfiguratie is. Dit betekent dat hun buitenste energieniveau compleet is, zonder vacatures voor extra elektronen.
* Lage elektronegativiteit: Ze hebben een zeer lage elektronegativiteit, wat betekent dat ze weinig neiging hebben om elektronen aan te trekken.
* Hoge ionisatie -energie: Ze hebben hoge ionisatie -energie, wat betekent dat het veel energie vereist om een elektron uit hun atomen te verwijderen.
Waarom dit hen niet reactief maakt:
* Het is niet nodig om elektronen te winnen of te verliezen: Omdat hun buitenste schaal vol is, hoeven ze geen elektronen te krijgen of te verliezen om stabiliteit te bereiken.
* Geen sterke aantrekkingskracht op andere atomen: Hun lage elektronegativiteit en gebrek aan lege ruimtes in hun buitenste schaal betekent dat ze niet gemakkelijk bindingen vormen met andere atomen.
* Moeilijk om ionen te vormen: Hun hoge ionisatie -energie maakt het moeilijk om elektronen te verwijderen, waardoor ze voorkomen dat ze gemakkelijk positieve ionen vormen.
Samenvattend: De volledige buitenste schaal van elektronen, lage elektronegativiteit en hoge ionisatie -energie van edelgassen maken ze zeer onreactief en bestand tegen het vormen van chemische bindingen. Daarom worden ze vaak 'inerte gassen' genoemd.
 Kan deze invasieve exotische plaag betere materialen maken voor de industrie en de geneeskunde?
Kan deze invasieve exotische plaag betere materialen maken voor de industrie en de geneeskunde? Voorbeelden van Alkynes
Voorbeelden van Alkynes  Onderzoekers werken samen met kleine bedrijven in NM om nieuwe beademingsmaterialen te testen
Onderzoekers werken samen met kleine bedrijven in NM om nieuwe beademingsmaterialen te testen Wat zijn het gebruik van dibenzylideaceton?
Wat zijn het gebruik van dibenzylideaceton?  Is het oplossen van zout in water een chemische verandering?
Is het oplossen van zout in water een chemische verandering?
 Orkaanrecords gebroken in 2017
Orkaanrecords gebroken in 2017 Agroforestry kan het VK helpen de verplichtingen inzake klimaatverandering na te komen zonder de veestapel te verminderen
Agroforestry kan het VK helpen de verplichtingen inzake klimaatverandering na te komen zonder de veestapel te verminderen Wat is het meest erkende element van kunst?
Wat is het meest erkende element van kunst?  Voorspellingen verifiëren voor grote plotselinge opwarming in de stratosfeer
Voorspellingen verifiëren voor grote plotselinge opwarming in de stratosfeer Hoe de stimuleringsdollars worden uitgegeven, zal de uitstoot tientallen jaren beïnvloeden
Hoe de stimuleringsdollars worden uitgegeven, zal de uitstoot tientallen jaren beïnvloeden
Hoofdlijnen
- Waar vindt transcriptie plaats in een eukaryote cel?
- De belangrijkste werking van de flexor hallicus longus spier is om?
- Onderzoeksvraag:Wat zijn computervirussen en waar komen ze vandaan?
- Wetenschappers volgen haaien die DNA-fragmenten uit de zee plukken
- Zeldzame zangvogel heeft misschien nooit bestaan
- Wat bepaalt of een specifiek tRNA wel of niet aan een mRNA kan binden?
- Wat zijn twee processen die bijdragen aan de genetische diversiteit van mensen?
- Wat is het synoniem voor cel?
- Wetenschappers:woestijnschildpad bedreigd, 100 over in Arizona
- Enkele atomen als katalysatoren

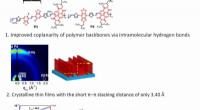
- Organische elektronica:wetenschappers ontwikkelen een hoogwaardige unipolaire n-type dunne-filmtransistor
- Smaakonderzoek voor consumentenbescherming

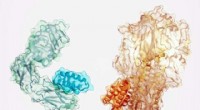
- Nieuwe methode voor het genereren van krachtige, specifieke bindende eiwitten voor nieuwe medicijnen
- Herbestemming van dimethyloxalylglycine om het glutaminemetabolisme te remmen
 Is het mogelijk om Mars te terravormen?
Is het mogelijk om Mars te terravormen?  Onderzoek levert test op om bittere pitstoornis in Honeycrisp-appels te voorspellen
Onderzoek levert test op om bittere pitstoornis in Honeycrisp-appels te voorspellen Zinkchloride plus ammoniumsulfide is gelijk?
Zinkchloride plus ammoniumsulfide is gelijk?  Hoe worden de verschillende vormen genoemd in een element met een groot aantal nuetrons?
Hoe worden de verschillende vormen genoemd in een element met een groot aantal nuetrons?  Waarom zijn alkali -metalen reactiever dan overgangsmetalen?
Waarom zijn alkali -metalen reactiever dan overgangsmetalen?  Wat is stellaire straling?
Wat is stellaire straling?  Vulkaan Bali spuwt rook en as, angst voor uitbarsting opwekken
Vulkaan Bali spuwt rook en as, angst voor uitbarsting opwekken Wat wordt spiritueel bedoeld met fotosynthese?
Wat wordt spiritueel bedoeld met fotosynthese?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

