
Wetenschap
Hoeveel atomen zijn er in 1 gram KOH?
1. Vind de molaire massa van KOH:
* K (kalium):39,10 g/mol
* O (zuurstof):16,00 g/mol
* H (waterstof):1,01 g/mol
* Totale molaire massa van KOH:39.10 + 16.00 + 1.01 =56.11 g/mol
2. Bereken het aantal mol in 1 gram KOH:
* Mol =massa / molaire massa
* Mol =1 g / 56.11 g / mol =0,0178 mol
3. Bereken het aantal moleculen in 0,0178 mol KOH:
* Gebruik Avogadro's nummer:6.022 x 10^23 moleculen/mol
* Moleculen =Moles X Avogadro's nummer
* Moleculen =0,0178 mol x 6,022 x 10^23 moleculen/mol =1,07 x 10^22 moleculen
4. Bereken het totale aantal atomen:
* Elk molecuul KOH heeft 3 atomen (1 K, 1 O, 1 H).
* Totale atomen =moleculen x atomen per molecuul
* Totale atomen =1,07 x 10^22 moleculen x 3 atomen/molecuul =3,21 x 10^22 atomen
Daarom zijn er ongeveer 3,21 x 10^22 atomen in 1 gram koh.
 Welk atmosferisch gas is een bijproduct van de lichtreactie-fotosynthese die essentieel is voor aerobe ademhaling?
Welk atmosferisch gas is een bijproduct van de lichtreactie-fotosynthese die essentieel is voor aerobe ademhaling?  Tien toepassingen van niet -metalen?
Tien toepassingen van niet -metalen?  Verloren metaalatomen hun valentie-elektronen bij het vormen van ionische verbindingen?
Verloren metaalatomen hun valentie-elektronen bij het vormen van ionische verbindingen?
Metaalatomen verliezen een deel van hun valentie-elektronen door een proces genaamd oxidatie, wat resulteert in een grote verscheidenheid aan ionische verbindin
 Hoeveel kwarts tot een gallon?
Hoeveel kwarts tot een gallon?  Het volgen van eiwitverwijdering kan leiden tot verbeterde therapieën
Het volgen van eiwitverwijdering kan leiden tot verbeterde therapieën
 Hoe planten omgaan met nuttige microben in de bodem
Hoe planten omgaan met nuttige microben in de bodem  Wat voor soort carrières kun je krijgen met een vrijgezellenwetenschap in de milieuwetenschap?
Wat voor soort carrières kun je krijgen met een vrijgezellenwetenschap in de milieuwetenschap?  Wat is uniek aan sfeer?
Wat is uniek aan sfeer?  Ten minste 2% van de openbare watersystemen in de VS zijn als Flints - Amerikanen horen er gewoon niets over
Ten minste 2% van de openbare watersystemen in de VS zijn als Flints - Amerikanen horen er gewoon niets over Wat zijn veronderstellingen die wetenschappers maken over de natuurlijke wereld?
Wat zijn veronderstellingen die wetenschappers maken over de natuurlijke wereld?
Hoofdlijnen
- Wat betekent nadh in de wetenschap?
- Wat doet een generator in wetenschappelijke verdediging?
- Een nieuwe studie geeft een belangrijk inzicht in de manier waarop moleculaire motoreiwitten betrokken zijn bij de overdracht van malaria
- Wat is een virus en hoe wordt het een gevaar voor het menselijk leven?
- Wildfire vormt een grotere bedreiging voor cannabis dan andere Californische gewassen
- Hoe kolonies in de microbiologie te tellen
- Plant die 108 jaar geleden uit Vermont verdween, per ongeluk herontdekt, zeggen botanici
- Wat is de ontwikkeling van verschillende weefsels?
- Welke soorten cellen en organismen ondergaan mitose en meiose?
- Twee-voor-één energie van fotonen, nu beter dan ooit
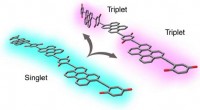
- Ferro-elektrische zelf-geassembleerde moleculaire materialen

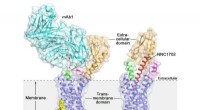
- Glucagon-receptorstructuur biedt nieuwe mogelijkheden voor het ontdekken van geneesmiddelen voor type 2 diabetes
- Wetenschappers ontwikkelen uniek gloeiend eiwit

- Onderzoek wijst op uniek medicijndoelwit in antibioticaresistente bacteriën

 What Is Thermodynamics?
What Is Thermodynamics?  Tibetaanse glaciale ijskern kan aanwijzingen bevatten over klimaatverandering
Tibetaanse glaciale ijskern kan aanwijzingen bevatten over klimaatverandering  Waarom is de binding LiBr covalent?
Waarom is de binding LiBr covalent?  Space smash - simuleren wanneer satellieten botsen
Space smash - simuleren wanneer satellieten botsen Wanneer chemische binding optreedt?
Wanneer chemische binding optreedt?  Hoe gaven oude beschavingen betekenis aan de kosmos, en wat hebben ze goed gedaan?
Hoe gaven oude beschavingen betekenis aan de kosmos, en wat hebben ze goed gedaan? Nieuw onderzoek onthult effect van opwarming van de aarde op het smelten van Groenlandse ijs
Nieuw onderzoek onthult effect van opwarming van de aarde op het smelten van Groenlandse ijs Kenmerken die worden gebruikt om een niet-gefolieerde rots te identificeren?
Kenmerken die worden gebruikt om een niet-gefolieerde rots te identificeren?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

