
Wetenschap
Hoe zijn zowel natrium als chloor?
* Locatie op het periodieke tabel: Natrium is een metaal gevonden in groep 1 (alkali-metalen), terwijl chloor een niet-metaal is gevonden in groep 17 (halogenen).
* Reactiviteit: Natrium is zeer reactief en verliest gemakkelijk één elektron om een positief ion te vormen (Na+). Chloor is ook reactief en krijgt gemakkelijk één elektron om een negatief ion te vormen (Cl-).
* Fysieke toestand: Natrium is een zacht, zilverachtig metaal bij kamertemperatuur. Chloor is een geelgroen, scherp gas.
* reacties: Natrium reageert heftig met water en laat waterstofgas vrij. Chloor kan reageren met metalen om zouten te vormen.
* uiterlijk: Natrium is glanzend en metaalachtig, terwijl chloor een groenachtig geel gas is.
De enige manier waarop ze hetzelfde zijn, is dat ze allebei gemakkelijk ionen vormen, wat de basis is van hun ionische binding wanneer ze combineren tot natriumchloride (NaCl) - tafelzout.
 Hoeveel SCF in een MCF van aardgas?
Hoeveel SCF in een MCF van aardgas?  De technologische uitdaging van antiaanbakpannen:Teflon is nog steeds effectiever dan andere coatings
De technologische uitdaging van antiaanbakpannen:Teflon is nog steeds effectiever dan andere coatings  Wanneer carbonaatmineralen in contact komen met zoutzuur?
Wanneer carbonaatmineralen in contact komen met zoutzuur?  Nieuwe 2D-spectroscopiemethoden
Nieuwe 2D-spectroscopiemethoden Experimenten en analyses laten zien hoe elektronen en protonen samenkomen op een elektrodeoppervlak
Experimenten en analyses laten zien hoe elektronen en protonen samenkomen op een elektrodeoppervlak
 Welke regelt de breedtegraadsklimaatzones in volgorde van toenemende hoeveelheden die zonlicht ontvangen?
Welke regelt de breedtegraadsklimaatzones in volgorde van toenemende hoeveelheden die zonlicht ontvangen?  Orkaan Lorenzo brengt golven van 70 voet naar Azoren
Orkaan Lorenzo brengt golven van 70 voet naar Azoren Wat voor soort voedsel bieden planten ons?
Wat voor soort voedsel bieden planten ons?  Het christendom verandert in Zuid-Afrika terwijl pinksterkerken en inheemse kerken groeien – wat zit er achter deze trend?
Het christendom verandert in Zuid-Afrika terwijl pinksterkerken en inheemse kerken groeien – wat zit er achter deze trend?  COVID-19:Stikstofdioxide boven China
COVID-19:Stikstofdioxide boven China
Hoofdlijnen
- Hoe wordt de studie van planten en dieren in interne onderdelen genoemd?
- Organismen in een ecosysteem zijn verbonden met elkaar verbonden door?
- Hoe maken wat diep waterbacteriën in de oceaan voedsel?
- leg uit waarom hormonen in de bloedbaan alleen doelcellen/organen kunnen beïnvloeden en niet andere cellen/organen?
- In welk seizoen vindt de kieming van planten plaats?
- Wetenschappers willen weten hoe uw genen omgaan met de omgeving ons maken tot wie u bent, dit is de vraag?
- Kunnen ziektetolerantiegenen nieuw leven geven aan Britse essen?
- Wat betekent kwantitatief in de wetenschap?
- Onderzoek levert inzicht op in hoe plantencellen groeien
- Groenere moleculaire tussenproducten kunnen helpen bij het ontwerpen van medicijnen

- Prominente academici pleiten voor meer wetenschap in forensische wetenschap

- Waarom een nieuwsgierige schaaldier het geheim zou kunnen houden om hernieuwbare energie uit hout te maken

- Nieuwe structurele eenheid vereenvoudigt het proces van het op maat ontwerpen van eiwitten
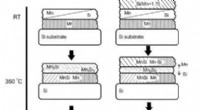
- Natuurkundigen houden toezicht op de vorming van hogere mangaansilicidefilms
 Koolstofuitstoot en boodschappen doen:EV's en thuisbezorging beter, trip chaining en robots het beste
Koolstofuitstoot en boodschappen doen:EV's en thuisbezorging beter, trip chaining en robots het beste Qantas gaat ultralangeafstandsvluchten van Sydney naar NY testen Londen vluchten
Qantas gaat ultralangeafstandsvluchten van Sydney naar NY testen Londen vluchten Hoeveel warmte-energie wordt overgedragen aan warm water?
Hoeveel warmte-energie wordt overgedragen aan warm water?  Hoe beïnvloedt water weerspatronen?
Hoe beïnvloedt water weerspatronen?  Hoe de totale vergroting te berekenen
Hoe de totale vergroting te berekenen Waarom is Horus de god van de lucht?
Waarom is Horus de god van de lucht?  NASA ziet krachtige tropische cycloon Marcus
NASA ziet krachtige tropische cycloon Marcus Jet Airways-aandelen stijgen door speculatie met Tata-investeringen
Jet Airways-aandelen stijgen door speculatie met Tata-investeringen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

