
Wetenschap
Wat gebeurt er als je fosfor combineert met andere elementen?
met metalen:
* fosfiden: Fosfor combineert met veel metalen om fosfiden te vormen. Deze verbindingen hebben een breed scala aan eigenschappen, van het zeer reactief tot de relatief inert.
* Voorbeelden: Aluminium fosfide (ALP), gebruikt als een fumigant; Calciumfosfide (Ca3p2), gebruikt voor het genereren van fosfinegas; Natriumfosfide (NA3P), een zeer reactieve verbinding die wordt gebruikt in chemische synthese.
* metaalfosfiden: Dit zijn over het algemeen niet-metalen, brosse vaste stoffen met verschillende geleidbaarheid.
met niet-metalen:
* oxiden: Fosfor vormt verschillende oxiden, waaronder:
* fosfortrioxide (P4O6): Een witte, kristallijne vaste stof die gemakkelijk reageert met water om fosforzuur te vormen.
* fosfor pentoxide (P4O10): Een zeer reactief, deliquescentwit poeder dat wordt gebruikt als droogmiddel en bij de productie van fosforzuur.
* haliden: Fosfor vormt trihalides (px3) en pentahalides (px5) met halogenen zoals chloor, broom en jodium.
* Voorbeelden: Fosfor trichloride (PCL3), gebruikt als een reagens in organische synthese; Fosfor pentachloride (PCL5), gebruikt bij de productie van andere fosforverbindingen.
* sulfiden: Fosfor kan sulfiden vormen zoals fosfor pentasulfide (p4S10) en fosfor trisulfide (p4S3).
* Phosporus pentasulfide (P4S10): Gebruikt bij de productie van pesticiden en bij de synthese van andere zwavelhoudende verbindingen.
* stikstof: Fosfor kan verbindingen vormen met stikstof, waaronder:
* fosfor nitride (P3N5): Een witte, refractaire vaste stof die wordt gebruikt bij de productie van keramiek op hoge temperatuur.
met organische verbindingen:
* Organofosfor -verbindingen: Fosfor vormt een breed scala aan organische verbindingen, die essentieel zijn in veel gebieden, waaronder:
* fosfaten: Anorganische fosfaten (PO43-) zijn essentieel voor het leven, gevonden in DNA, RNA en ATP.
* fosfines: Organofosfines worden gebruikt in katalyse, als liganden in coördinatiechemie, en als tussenproducten in de synthese van andere organofosforverbindingen.
* Fosfonaten: Gebruikt in pesticiden, vlamvertragers en als additieven in kunststoffen.
* fosfaten esters: Gebruikt in wasmiddelen, weekmakers en als vlamvertragers.
Belangrijke dingen om te onthouden:
* Reactiviteit: Fosfor kan zeer reactief zijn, vooral in zijn witte vorm. Dit komt door de kleine omvang en de aanwezigheid van ongepaarde elektronen.
* Verschillende vormen: Fosfor bestaat in verschillende allotropen, waaronder witte, rode en zwarte fosfor, elk met unieke eigenschappen.
* Belang: Fosforverbindingen zijn cruciaal op veel gebieden, waaronder landbouw, industrie en geneeskunde.
Houd er rekening mee dat het mengen van fosfor met andere elementen gevaarlijk kan zijn en dat de juiste veiligheidsmaatregelen altijd moeten worden genomen.
 Welk orgel duwt er afval door?
Welk orgel duwt er afval door?  Onderzoekers benadrukken de vooruitgang in biomedisch onderzoek met enzymgeactiveerde fluorescerende sondes
Onderzoekers benadrukken de vooruitgang in biomedisch onderzoek met enzymgeactiveerde fluorescerende sondes  Cryo-EM onthult kritisch eiwitmodificerend complex en potentieel medicijndoelwit
Cryo-EM onthult kritisch eiwitmodificerend complex en potentieel medicijndoelwit Welk type gas gebruikt een vliegtuig?
Welk type gas gebruikt een vliegtuig?  Nieuwe technieken onderzoeken vitale en ongrijpbare eiwitten
Nieuwe technieken onderzoeken vitale en ongrijpbare eiwitten
 vulkaan Indonesië barst uit, spuwt gloeiend hete lava
vulkaan Indonesië barst uit, spuwt gloeiend hete lava San Francisco verslikt zich in giftige lucht terwijl bosbranden woeden
San Francisco verslikt zich in giftige lucht terwijl bosbranden woeden Sterke aardbeving treft het Griekse Kreta, geen gewonden gemeld
Sterke aardbeving treft het Griekse Kreta, geen gewonden gemeld In Israël, op zoek naar droogtes in het verleden en de toekomst
In Israël, op zoek naar droogtes in het verleden en de toekomst Een opwarmende planeet heeft gevolgen voor de menselijke gezondheid
Een opwarmende planeet heeft gevolgen voor de menselijke gezondheid
Hoofdlijnen
- Naar welke drie kenmerken bepalen het domein of het koninkrijk waar een organisme tot hoort?
- Moeite met onthouden? Vertel je vrienden om een wandeling te maken
- Hoe beïnvloeden abiotische factoren de reproductie van Cattail?
- De productie van recombinante menselijke groeihormonen door Recombinant DNA Technology
- Wat gebeurt er met de meeste organismen als ze sterven?
- Zijn voedingsmiddelen gemaakt met behulp van biotechnologie veilig om te eten?
- Zijn chlorobium en fotosynthetische bacteriën van Clostridium?
- Wat is de diameter van DNA Double Helix?
- Hoe de snelste spier ter wereld vier unieke vogelsoorten creëerde
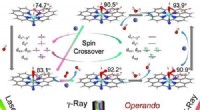
- Wetenschappers identificeren elektronische en structurele dynamiek van katalytische centra in materialen met één Fe-atoom
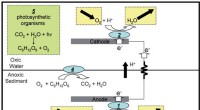
- NRL heeft patent verleend voor microbiële brandstofcel op zonne-energie
- Nieuwe ontdekking opent nieuwe weg voor productie met hoge titer van drop-in biobrandstoffen

- Video:Hoe melk kaas wordt

- Nieuw, duurzame katalysator voor belangrijke brandstofcelreacties kan nuttig zijn in milieuvriendelijke voertuigen

 Zelftwijfel en isolatie, maar ook veerkracht bij nieuwe leraren als gevolg van pandemie, vindt rapport
Zelftwijfel en isolatie, maar ook veerkracht bij nieuwe leraren als gevolg van pandemie, vindt rapport Plasma-elektronen kunnen worden gebruikt om metaalfilms te produceren
Plasma-elektronen kunnen worden gebruikt om metaalfilms te produceren Pakistan gaat tegen de stroom in met kolenstroom
Pakistan gaat tegen de stroom in met kolenstroom Hoe maak je een chemische Light
Hoe maak je een chemische Light Hoe de kubus te berekenen Root
Hoe de kubus te berekenen Root MtGox bitcoin-baron krijgt voorwaardelijke straf voor gegevensmanipulatie
MtGox bitcoin-baron krijgt voorwaardelijke straf voor gegevensmanipulatie Reactie van formaldehyde met kaliumpermanganaat?
Reactie van formaldehyde met kaliumpermanganaat?  Zwarte gaten vuren deeltjesdeeltjes af en veranderen in de loop van de tijd van doelwit
Zwarte gaten vuren deeltjesdeeltjes af en veranderen in de loop van de tijd van doelwit
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

