
Wetenschap
Verandert de temperatuur van een stoffen wanneer deze van status verandert?
Dit is waarom:
* Faseveranderingen vereisen energie: Veranderende toestand omvat het breken of het vormen van bindingen tussen moleculen. Dit vereist energie -input (voor smelten, koken, sublimatie) of energieafgifte (voor bevriezing, condensatie, afzetting).
* Energie gaat in veranderende toestand, niet in temperatuur: In plaats van de kinetische energie van moleculen te vergroten (die de temperatuur zouden verhogen), wordt de energie gebruikt om de krachten te overwinnen die de moleculen in de huidige toestand houden.
* constante temperatuur tijdens faseverandering: De toegevoegde of vrijgegeven energie wordt volledig gebruikt om de toestand van de stof te veranderen, zodat de temperatuur constant blijft tijdens de faseverandering.
Voorbeeld: Wanneer ijs smelt, gaat de geleverde energie in het verbreken van de bindingen tussen watermoleculen, waardoor ze vrijer kunnen bewegen als een vloeistof. De temperatuur blijft bij 0 ° C totdat al het ijs is gesmolten.
Opmerking: Er zijn enkele nuances in deze verklaring, zoals het concept van "latente warmte" en het idee dat zeer kleine temperatuurveranderingen soms kunnen optreden tijdens een faseverandering. Voor de meeste praktische doeleinden blijft de temperatuur van een stof echter constant tijdens een faseverandering.
 Gezichtsmaskers zijn een tikkende plastic tijdbom
Gezichtsmaskers zijn een tikkende plastic tijdbom Mexico veilt zes van de negen grote diepwaterolieblokken
Mexico veilt zes van de negen grote diepwaterolieblokken Factoren die het leven in zee beïnvloeden
Factoren die het leven in zee beïnvloeden Hoe digitale technologie steden groen en aangenaam kan houden
Hoe digitale technologie steden groen en aangenaam kan houden Forel in door mijnen vervuilde rivieren is genetisch geïsoleerd, blijkt uit nieuw onderzoek
Forel in door mijnen vervuilde rivieren is genetisch geïsoleerd, blijkt uit nieuw onderzoek
Hoofdlijnen
- Moleculaire kaart laat zien hoe gevaarlijke biowapens kunnen worden uitgeschakeld
- Waar is een celmembraan in de dierencel?
- Wat is de functie van gewas in een duif?
- Nieuwe aanwijzingen waarom er zo weinig antimaterie in het universum is
- Nieuwe histonmodificaties koppelen metabolisme aan genactiviteit
- Namen van de enzymen in de mond & slokdarm
- Hoe een opkomende ziekte bij honden licht werpt op cystische fibrose
- Meld-en-klauwzeer:de lacunes in de inspanningen van Zuid-Afrika om het onder controle te houden
- Koolstof wordt de basis van het leven genoemd?
- Alternatieve toepassingen voor bioproducten van cannabidiol

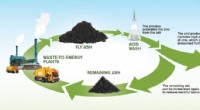
- Kostbaar zink winnen uit afvalas
- Onderzoekers wekken DNA uit bodembacteriën om nieuw zuur antibioticum te ontdekken

- Onderzoekers meten elektronenemissie om het begrip van lasergebaseerd 3D-printen van metaal te verbeteren

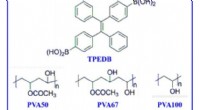
- Grootschalige bereiding van op polymeer gebaseerde fosforescentie bij kamertemperatuur via klikchemie
 Afstembare VO₂-holte maakt multispectrale manipulatie mogelijk van zichtbare tot microgolffrequenties
Afstembare VO₂-holte maakt multispectrale manipulatie mogelijk van zichtbare tot microgolffrequenties  Airbnb gaat alle 7 miljoen accommodaties verifiëren om het vertrouwen te verbeteren
Airbnb gaat alle 7 miljoen accommodaties verifiëren om het vertrouwen te verbeteren Wat hebben bugs te maken met forensische wetenschap?
Wat hebben bugs te maken met forensische wetenschap?  Waarom gaat de oceanische korst onder de continentale korst als ze botsen?
Waarom gaat de oceanische korst onder de continentale korst als ze botsen?  Hoe universiteiten de sociale kloof tussen internationale, binnenlandse studenten kunnen helpen overbruggen
Hoe universiteiten de sociale kloof tussen internationale, binnenlandse studenten kunnen helpen overbruggen  Geneesmiddelen met nanodeeltjes kunnen het voor medicijnen gemakkelijker maken om hun doelen te bereiken
Geneesmiddelen met nanodeeltjes kunnen het voor medicijnen gemakkelijker maken om hun doelen te bereiken Kunnen asteroïden de aarde bombarderen om binnen 10 miljoen jaar een massale uitsterving te veroorzaken?
Kunnen asteroïden de aarde bombarderen om binnen 10 miljoen jaar een massale uitsterving te veroorzaken? Wat is Thomas Edison -bijdrage op het gebied van wetenschap en technologie?
Wat is Thomas Edison -bijdrage op het gebied van wetenschap en technologie?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

