
Wetenschap
Wat is de eenvoudigste vorm van chemische vergelijking voor zelfionisatiewater?
2 H₂o ⇌ H₃o⁺ + oh⁻
Dit is wat het betekent:
* 2 H₂o :Twee watermoleculen zijn betrokken bij de reactie.
* ⇌ :Dit symbool geeft een evenwichtsreactie aan, wat betekent dat de reactie in beide richtingen kan doorgaan.
* h₃o⁺ :Dit is het hydroniumion, gevormd wanneer een watermolecuul een proton accepteert (H⁺).
* oh⁻ :Dit is het hydroxide -ion, gevormd wanneer een watermolecuul een proton verliest (H⁺).
Verklaring:
Watermoleculen kunnen zowel zuren als basen werken. In deze reactie werkt het ene watermolecuul als een zuur en doneert het een proton (H⁺) aan een ander watermolecuul, dat als basis werkt. Dit resulteert in de vorming van hydroniumionen (H₃o⁺) en hydroxide -ionen (OH⁻).
 Is natriummethoxide-oplossing oplosbaar in tolueen?
Is natriummethoxide-oplossing oplosbaar in tolueen?  Waarom hebben atomen met een lage elektronegativiteit zoals lithium een zwakke aantrekkingskracht voor elektronen?
Waarom hebben atomen met een lage elektronegativiteit zoals lithium een zwakke aantrekkingskracht voor elektronen?  Waarom is koeling met ijs effectiever dan water?
Waarom is koeling met ijs effectiever dan water?  Als je 25 g zink en 300 g zwavel hebt, wat is de massale overtollige reactant?
Als je 25 g zink en 300 g zwavel hebt, wat is de massale overtollige reactant?  Het meest nauwkeurige beeld van Zika tot nu toe creëert potentieel voor therapieën
Het meest nauwkeurige beeld van Zika tot nu toe creëert potentieel voor therapieën
 Microben in Atacama-woestijn kunnen aanwijzingen bevatten voor leven op Mars
Microben in Atacama-woestijn kunnen aanwijzingen bevatten voor leven op Mars Hoe dragen levende organismen bij aan de waterkringloop?
Hoe dragen levende organismen bij aan de waterkringloop?  Welke wordt een bloem beter in zout of kraanwater?
Welke wordt een bloem beter in zout of kraanwater?  Door ijs geperste watervoerende lagen kunnen marsbevingen veroorzaken
Door ijs geperste watervoerende lagen kunnen marsbevingen veroorzaken Hoe zou de wereld eruitzien bij een opwarming van 3°C en hoe zou die anders zijn dan 1,5°C?
Hoe zou de wereld eruitzien bij een opwarming van 3°C en hoe zou die anders zijn dan 1,5°C?
Hoofdlijnen
- Wat is het eerste micro -organisme op aarde?
- Waarom moet het voedsel dat u eet, worden gewijzigd voor gebruik door uw cel?
- Weten wat je moet bewaren en weggooien:hoe een enzym cellulaire berichten onderscheidt
- Waarom worden mitrochondria de krachtpatoren van cellen genoemd?
- Britse wetenschapper die voor het eerst cellen onder een microscoop observeerde?
- Uw smartphone is mogelijk gelinkt aan krokodillenaanvallen in Indonesië
- Hoe zijn eetstokjes en wetenschap gerelateerd?
- Wat zijn de voorbeelden van ziekten in planten?
- Als een lichaamscel 22 chromosomen heeft, wat zou de telling voor reproductieve cellen zijn?
- Decennia lang onderzoek mondt uit in een nieuwe manier om links- en rechtshandige moleculen te maken

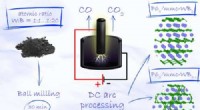
- Superharde materiaalsynthese goedkoper gemaakt
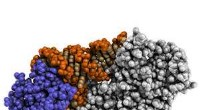
- Sleutel tot uitbreiding van genetische code beschreven
- Nieuw productieproces voor polymeren bespaart 10 ordes van energie

- Nieuwe gelcoatings kunnen leiden tot betere katheters en condooms

 Microalgen zuiveren water en produceren waardevolle verbindingen
Microalgen zuiveren water en produceren waardevolle verbindingen Het geheim om sympathieker te zijn op eerste dates en sollicitatiegesprekken onthuld
Het geheim om sympathieker te zijn op eerste dates en sollicitatiegesprekken onthuld Wat is divergentie in de evolutie?
Wat is divergentie in de evolutie?  Toshiba onthult robot om gesmolten kernbrandstof Fukushima te onderzoeken
Toshiba onthult robot om gesmolten kernbrandstof Fukushima te onderzoeken Er zou buitenaards leven op Mars kunnen zijn, maar zullen onze rovers het kunnen vinden?
Er zou buitenaards leven op Mars kunnen zijn, maar zullen onze rovers het kunnen vinden?  Wat is een cardanische ophanging - en wat heeft het met NASA te maken?
Wat is een cardanische ophanging - en wat heeft het met NASA te maken?  Waarom zijn schermen slecht voor je?
Waarom zijn schermen slecht voor je?  Aarde versus asteroïden:mensen slaan terug
Aarde versus asteroïden:mensen slaan terug
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

