
Wetenschap
Wat is de elektronische configuratie van een atoom met atoomnummer 42?
1. Vulorder:
* Volg het AUFBAU -principe en de heerschappij van Hund om de orbitalen te vullen in volgorde van toenemende energieniveaus.
* De volgorde is:1S, 2S, 2p, 3s, 3p, 4s, 3d, 4p, 5s, 4d, 5p, 6s, 4f, 5d, 6p, 7s, 5f, 6d, 7p ...
2. Aantal elektronen:
* Het atoomnummer (42) vertelt ons dat er 42 elektronen zijn om te distribueren.
3. Elektronische configuratie:
* 1S² 2S² 2P⁶ 3S² 3P⁶ 4S² 3D¹⁰ 4P⁶ 5S¹ 4D⁵
Verklaring:
* De eerste drie schelpen (1s, 2s, 2p, 3s, 3p) zijn volledig gevuld.
* De 4S -subshell is gevuld met 2 elektronen.
* De 3D -subshell is gevuld met 10 elektronen.
* De 4P -subshell is gevuld met 6 elektronen.
* De 5S -subshell heeft 1 elektron.
* De 4D-subshell heeft 5 elektronen (dit is een speciaal geval waarbij de 4D-subshell half gevuld is, wat bijdraagt aan de stabiliteit van het atoom).
Belangrijke opmerking: Dit is de grondtoestand elektronische configuratie. In sommige gevallen kunnen elementen opgewonden toestand hebben Configuraties waarbij elektronen hogere energieniveaus bezetten.
 Nieuwe methode maakt generieke polymeren lichtgevend
Nieuwe methode maakt generieke polymeren lichtgevend Is een tomaat zuur of basisch?
Is een tomaat zuur of basisch?  Hoe wordt de luchtdichtheid gerelateerd aan de druk verklaard?
Hoe wordt de luchtdichtheid gerelateerd aan de druk verklaard?  Wat is een eigenschap die kan worden gebruikt om metalen van niet-metaalhoudende mineralen te onderscheiden?
Wat is een eigenschap die kan worden gebruikt om metalen van niet-metaalhoudende mineralen te onderscheiden?  Waarom fungeert een waterige oplossing van ammoniak als een zwakke base?
Waarom fungeert een waterige oplossing van ammoniak als een zwakke base?
Hoofdlijnen
- Dolfijnengezondheidscontrole toont toestand van onze oceanen
- De celstructuur van een ui
- Wetenschappers tonen moleculaire basis voor mieren die als lijfwachten voor planten fungeren
- Een van 's werelds zeldzaamste walvissen waargenomen voor de kust van Californië
- Ontcijferen hoe virussen ervoor kiezen om al dan niet hun bacteriële gastheer te worden
- Wat is het verschil tussen een protist en een menselijke huidcel?
- Wat is de medische term die een onregelmatigheid betekent in de vorm van rode bloedcellen?
- 85 nieuwe soorten beschreven door de California Academy of Sciences in 2017
- Prehistorische skeletten van vrouwen tonen impact van rigoureuze handenarbeid
- Legerproject kan leiden tot nieuwe klasse hoogwaardige materialen
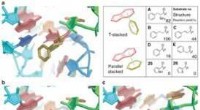
- Hatchet enzym, aanjager van ziekte en gezondheid, blootgesteld door neutronenstralen

- Kleine sensoren ontwikkeld om de geheimen van hersenchemie te bestuderen

- Techniek kan het gemakkelijker maken om mRNA te gebruiken om ziekten te behandelen of vaccins af te leveren

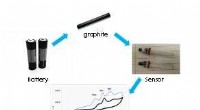
- Van batterijafval tot elektrochemische sensor
 Soepele operator:wanneer winstbeheer een goede zaak is
Soepele operator:wanneer winstbeheer een goede zaak is Wat zou er gebeuren als een druppel bloed zou worden toegevoegd aan oplossingsperstofperoxide?
Wat zou er gebeuren als een druppel bloed zou worden toegevoegd aan oplossingsperstofperoxide?  Wetenschappers leren neuraal netwerk om het geslacht van een schrijver te identificeren
Wetenschappers leren neuraal netwerk om het geslacht van een schrijver te identificeren Wat is het afvalproduct van fotosynthese?
Wat is het afvalproduct van fotosynthese?  Wetenschappers observeren rechtstreeks de overdracht van licht naar energie in nieuwe zonnecelmaterialen
Wetenschappers observeren rechtstreeks de overdracht van licht naar energie in nieuwe zonnecelmaterialen Waarom plotselinge overstromingen zo gevaarlijk zijn
Waarom plotselinge overstromingen zo gevaarlijk zijn  Van pedicure tot de Slechtvalk, paraffinewas bewijst zijn waarde
Van pedicure tot de Slechtvalk, paraffinewas bewijst zijn waarde Hoe voelt een aardwormlicht?
Hoe voelt een aardwormlicht?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

