
Wetenschap
Wat zijn de oplosbaarheidsproducten van loodchloride?
Het oplosbaarheidsproduct is een maat voor de oplosbaarheid van een verbinding in water. Het wordt gedefinieerd als het product van de concentraties van de ionen waaruit de verbinding bestaat, elk verhoogd tot de macht van zijn stoichiometrische coëfficiënt in de uitgebalanceerde chemische vergelijking voor de oplossingsreactie.
Voor loodchloride is de oplossingsreactie:
PbCl2(s) <=> Pb2+(aq) + 2Cl-(aq)
De oplosbaarheidsproductuitdrukking voor loodchloride is:
Ksp =[Pb2+][Cl-]^2
waarbij Ksp het oplosbaarheidsproduct is, is [Pb2+] de concentratie van loodionen in mol/L, en [Cl-] de concentratie van chloride-ionen in mol/L.
Bij evenwicht zijn de concentraties van loodionen en chloride-ionen in een verzadigde oplossing van loodchloride gelijk, dus we kunnen [Pb2+] vervangen door [Cl-] in de uitdrukking van het oplosbaarheidsproduct:
Ksp =[Pb2+]^3
Als we [Pb2+] oplossen, krijgen we:
[Pb2+] =(Ksp)^(1/3) =(1,2 * 10^-5)^(1/3) =1,08 * 10^-2 mol/L
Daarom is de oplosbaarheid van loodchloride in water bij 25°C 1,08 * 10^-2 mol/L.
 Als je elektrolyse uitvoert met koperelektroden in een oplossing van natriumcarbonaat, wat is dan de overgebleven blauwe oplossing?
Als je elektrolyse uitvoert met koperelektroden in een oplossing van natriumcarbonaat, wat is dan de overgebleven blauwe oplossing?  Een tool gebaseerd op het gebruik van koolstofnanodeeltjes maakt detectie van antidepressiva in urinemonsters mogelijk
Een tool gebaseerd op het gebruik van koolstofnanodeeltjes maakt detectie van antidepressiva in urinemonsters mogelijk Dagelijkse activiteiten die chemie met zich meebrengen
Dagelijkse activiteiten die chemie met zich meebrengen Hoeveel moleculen zijn HNO3?
Hoeveel moleculen zijn HNO3?  Er gebeuren vreemde dingen als een kristal in tweeën wordt gesplitst
Er gebeuren vreemde dingen als een kristal in tweeën wordt gesplitst
 Nieuw-Zeeland is het best geplaatst om de ineenstorting te overleven
Nieuw-Zeeland is het best geplaatst om de ineenstorting te overleven Er kan een enorme fout zijn in de hoop op fracking in het VK - de geologie
Er kan een enorme fout zijn in de hoop op fracking in het VK - de geologie Incident op Mauritius was 's werelds eerste grote lekkage van stookolie met een zeer laag zwavelgehalte
Incident op Mauritius was 's werelds eerste grote lekkage van stookolie met een zeer laag zwavelgehalte Het lozen van waswater in de Oostzee is verantwoordelijk voor honderden miljoenen kosten
Het lozen van waswater in de Oostzee is verantwoordelijk voor honderden miljoenen kosten  Hoe China de klimaatverandering aanpakt
Hoe China de klimaatverandering aanpakt
Hoofdlijnen
- Wat is chloorflukoolstof?
- De vorm van het leven:onderzoek werpt licht op hoe cellen nemen
- Een boom die zichzelf bezit, groeit in Athene,
- Binaural beats:kalmeert deze auditieve illusie echt je hersenen?
- Waar worden vezels gefermenteerd in het spijsverteringskanaal van varkens?
- De rol van enzymen bij cellulaire ademhaling
- Hoe videogames de inspiratie vormden voor een strijd tegen mitochondriale ziekten
- Hoe bacteriën resistentie tegen antibiotica ontwikkelen
- DNA-studies tonen micro-evolutie aan bij pinguïns
- Wetenschappers onderzoeken toekomstig gebruik van op bacteriën gebaseerde actieve stoffen

- Van nata de coco tot computerschermen:Cellulose krijgt een kans om te schitteren
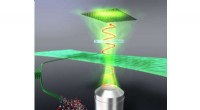
- Raman-picoscopie scannen:een nieuwe methode voor het bepalen van de moleculaire chemische structuur
- Onderzoekers ontwikkelen tool voor snelle diagnose van bacteriële infecties

- Belangrijkste bouwsteen voor organische moleculen ontdekt in meteorieten

 Eerste luchtkwaliteitsprofiel van twee sub-Sahara Afrikaanse steden vindt verontrustend nieuws
Eerste luchtkwaliteitsprofiel van twee sub-Sahara Afrikaanse steden vindt verontrustend nieuws Californië stuurde 12 miljoen mensen een sms-bericht over brandgevaar
Californië stuurde 12 miljoen mensen een sms-bericht over brandgevaar Nieuwe vooruitgang in de richting van op chips gebaseerde spookbeeldvorming
Nieuwe vooruitgang in de richting van op chips gebaseerde spookbeeldvorming Een betrouwbare verwerking van efficiënt zonnecelmateriaal is afhankelijk van de manier waarop oplosmiddel wordt verwijderd
Een betrouwbare verwerking van efficiënt zonnecelmateriaal is afhankelijk van de manier waarop oplosmiddel wordt verwijderd  Onderzoekers ontrafelen de actieve fase in katalytische reductie van kooldioxide tot methanol
Onderzoekers ontrafelen de actieve fase in katalytische reductie van kooldioxide tot methanol Inheemse bosbeschermingen zijn diep gebrekkig, maar kan nog 20 jaar op zijn plaats zijn
Inheemse bosbeschermingen zijn diep gebrekkig, maar kan nog 20 jaar op zijn plaats zijn Nieuwe kleptechnologie belooft goedkoper, groenere motoren
Nieuwe kleptechnologie belooft goedkoper, groenere motoren Polymeren kunnen schade veroorzaakt door stortplaatsen verminderen
Polymeren kunnen schade veroorzaakt door stortplaatsen verminderen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

