
Wetenschap
Waarom zijn Pb IV-verbindingen krachtige oxidatiemiddelen?
Lood(IV)verbindingen zijn krachtige oxidatiemiddelen omdat ze een hoge oxidatietoestand hebben en daarom waarschijnlijker elektronen accepteren. Dit betekent dat ze gemakkelijk kunnen reageren met andere stoffen om deze te verminderen, en daarbij raken ze zelf geoxideerd.
Het oxiderende vermogen van lood(IV)verbindingen is ook te danken aan het feit dat ze relatief onstabiel zijn. Dit betekent dat de kans groter is dat ze ontleden en hun energie vrijgeven in de vorm van warmte en licht. Dit maakt ze nuttig als explosieven en drijfgassen.
Enkele voorbeelden van lood(IV)-verbindingen die krachtige oxidatiemiddelen zijn, zijn onder meer:
* Lood(IV)oxide (PbO2)
* Lood(IV)acetaat (Pb(CH3COO)4)
* Lood(IV)nitraat (Pb(NO3)4)
Deze verbindingen zijn allemaal zeer reactief en kunnen gemakkelijk brand en explosies veroorzaken. Ze moeten met zorg worden behandeld en op een veilige plaats worden bewaard.
 Als een monster van 2,743 g magnesiumsulfaatkristallen sterk zou worden verwarmd, wat zou dan het massagekoelde gedehydrateerde zout zijn?
Als een monster van 2,743 g magnesiumsulfaatkristallen sterk zou worden verwarmd, wat zou dan het massagekoelde gedehydrateerde zout zijn?  groener, snellere en goedkopere manier om metalen patronen te maken voor zonnecellen en elektronica
groener, snellere en goedkopere manier om metalen patronen te maken voor zonnecellen en elektronica Wat is het verschil tussen monobasische en dibasische zuren?
Wat is het verschil tussen monobasische en dibasische zuren?  Hoe leer je een basisschoolkind over toestemming? Met deze boeken kun je beginnen
Hoe leer je een basisschoolkind over toestemming? Met deze boeken kun je beginnen  Wat zijn vijf polymeren in een huis?
Wat zijn vijf polymeren in een huis?
 Hoe de Braziliaanse regering openbaar land privé maakt en de weg vrijmaakt voor ontbossing
Hoe de Braziliaanse regering openbaar land privé maakt en de weg vrijmaakt voor ontbossing Taranakis ongebruikelijke aardbevingen
Taranakis ongebruikelijke aardbevingen Rook uit Afrika bevrucht de Amazone en tropische oceaangebieden met oplosbaar fosfor
Rook uit Afrika bevrucht de Amazone en tropische oceaangebieden met oplosbaar fosfor Onderzoekers vliegen en zeilen naar de meest stormachtige plek op aarde om wolkenprocessen te bestuderen
Onderzoekers vliegen en zeilen naar de meest stormachtige plek op aarde om wolkenprocessen te bestuderen How Big Can a Shark Get?
How Big Can a Shark Get?
Hoofdlijnen
- Hoe wordt de menselijke mannelijke gameet genoemd?
- Britse rundvleesboeren willen overstappen naar netto nul, maar praktische en financiële belemmeringen staan in de weg
- Wie ben ik de wetenschapper die concludeerde dat alle planten uit cellen bestaan?
- Onderzoek suggereert waarom sommige dieren langer leven
- Eiwitten in haaientanden kunnen duiden op wat ze eten
- Ambien
- Hoe mensen uit het stenen tijdperk de glucose in planten ontsloten
- Komt de gemanipuleerde 'Frankenfish' naar de tafel van het land?
- Wat betekent -ose in de wetenschappelijke woordenschat?
- Hydrogel bevordert wondgenezing beter dan traditionele zwachtels, gaasjes
- Materiaalchemici tappen lichaamswarmte af om slimme kleding van stroom te voorzien

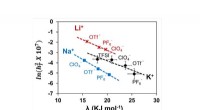
- Geen trial-and-error meer bij het kiezen van een elektrolyt voor metaal-luchtbatterijen
- Onderzoekers ontwikkelen solid-state, vrijstaande supercondensator van koolstofnanovezel

- Aan de lijn:kijken hoe nanodeeltjes vorm krijgen

 Wat zijn zes typen EMR?
Wat zijn zes typen EMR?  Nieuw model vindt dat landen moeten samenwerken om het coronavirus onder controle te houden schadelijke soorten
Nieuw model vindt dat landen moeten samenwerken om het coronavirus onder controle te houden schadelijke soorten Het leven in het water duidelijk gemaakt met zoetwaterlens
Het leven in het water duidelijk gemaakt met zoetwaterlens Het elektrische zand van Titan:de korrels die de maan van Saturnus bedekken, werken als plakkerige pinda's
Het elektrische zand van Titan:de korrels die de maan van Saturnus bedekken, werken als plakkerige pinda's Tandem elektrokatalysator met één atoom realiseert reductie van CO2 tot ethanol
Tandem elektrokatalysator met één atoom realiseert reductie van CO2 tot ethanol  Gebruik chemische reactie en neerslag in dezelfde zin?
Gebruik chemische reactie en neerslag in dezelfde zin?  Vis uit het water:hoe killifish-embryo's hun ontwikkeling aanpassen
Vis uit het water:hoe killifish-embryo's hun ontwikkeling aanpassen  Beeldvorming met hoge resolutie van oppervlaktestructuren van nanodeeltjes is nu mogelijk
Beeldvorming met hoge resolutie van oppervlaktestructuren van nanodeeltjes is nu mogelijk
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

