Wetenschap
Waarom is natriumchloride onoplosbaar in ethylalcohol?
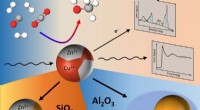
Wanneer natriumchloride in water wordt opgelost, omringen de watermoleculen de ionen en solvateren ze, wat betekent dat ze een laag watermoleculen rond elk ion vormen. Dit solvatatieproces verzwakt de elektrostatische krachten tussen de ionen, waardoor ze zich kunnen scheiden en in het water kunnen oplossen.
Daarentegen is ethylalcohol niet in staat natriumchloride-ionen zo effectief op te lossen als water. Dit komt omdat de ethylalcoholmoleculen niet zo polair zijn als watermoleculen, dus vormen ze niet zo sterke waterstofbruggen met de ionen. Als resultaat worden de elektrostatische krachten tussen de ionen niet voldoende verzwakt om ze te laten scheiden en oplossen in de ethylalcohol.
Daarom is natriumchloride onoplosbaar in ethylalcohol.
 Hoe vloeistofviscositeit de intensiteit van aardbevingen beïnvloedt
Hoe vloeistofviscositeit de intensiteit van aardbevingen beïnvloedt Er hangt zoveel af van een boombeschermer
Er hangt zoveel af van een boombeschermer Nieuwe studie onthult toegenomen sneeuwval op Antarctica in de afgelopen twee eeuwen
Nieuwe studie onthult toegenomen sneeuwval op Antarctica in de afgelopen twee eeuwen Midden in de woestenij van de Salton Sea, een wonderbaarlijke maar uitdagende oase is geboren
Midden in de woestenij van de Salton Sea, een wonderbaarlijke maar uitdagende oase is geboren Atmosferische wetenschappers brengen het verlies van zee-ijs in de Noordpool in verband met sterke El Niño-gebeurtenissen
Atmosferische wetenschappers brengen het verlies van zee-ijs in de Noordpool in verband met sterke El Niño-gebeurtenissen
Hoofdlijnen
- Waarom is water van levensbelang?
- Hoe regelt een cel het herstel van zijn beschadigde DNA?
- Onderzoek identificeert een nieuw mechanisme dat betrokken is bij de voortplantingsfunctie
- Wat is functiebasis in een microscoop?
- Onderzoek laat zien hoe intermitterend vasten veroudering reguleert via autofagie
- Familiebanden geven dieren redenen om te helpen of kwaad te doen naarmate ze ouder worden
- Wat fossielen onthullen over de hybridisatie van vroege mensen
- Wetenschappers ontcijferen hoe planten zonnebrand voorkomen
- Een probioticum voor onze longen? Nieuw onderzoek roept vragen op over de toekomst van de behandeling van COVID-19
 Elektronenemissie van bestraalde biomoleculen meten
Elektronenemissie van bestraalde biomoleculen meten Solar Orbiters-foto's van de zon zijn net zo dramatisch als je had gehoopt
Solar Orbiters-foto's van de zon zijn net zo dramatisch als je had gehoopt Op tekst gebaseerde duwtjes naar middelbare scholieren stimuleren het indienen van financiële hulp, college inschrijving
Op tekst gebaseerde duwtjes naar middelbare scholieren stimuleren het indienen van financiële hulp, college inschrijving De gemiddelde massa van een booratoom is 10,81. Ervan uitgaande dat je er maar één kunt isoleren, is de kans dat dat willekeurig zou gebeuren groot?
De gemiddelde massa van een booratoom is 10,81. Ervan uitgaande dat je er maar één kunt isoleren, is de kans dat dat willekeurig zou gebeuren groot?  Everest is gesloten:gedwongen onderbreking zal het milieu helpen herstellen, maar een miljoen levensonderhoud raken
Everest is gesloten:gedwongen onderbreking zal het milieu helpen herstellen, maar een miljoen levensonderhoud raken Een bio-geïnspireerde mechano-fotonische kunstmatige synaps
Een bio-geïnspireerde mechano-fotonische kunstmatige synaps Hoe bescherming tegen overstromingen paradoxaal genoeg mensen in gevaar kan brengen
Hoe bescherming tegen overstromingen paradoxaal genoeg mensen in gevaar kan brengen Vooruitgang in het begrijpen van de evolutie van maagverlies bij maagvissen
Vooruitgang in het begrijpen van de evolutie van maagverlies bij maagvissen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com