
Wetenschap
Wat zijn de vier soorten chemische bindingen?
1. Covalente bindingen treedt op wanneer twee of meer atomen elektronen delen om een stabiele elektronenconfiguratie te vormen. Dit is het sterkste type chemische binding en wordt aangetroffen in moleculen zoals water (H2O) en methaan (CH4).
2. Ionische bindingen treedt op wanneer een of meer elektronen van het ene atoom naar het andere worden overgebracht, waardoor tegengesteld geladen ionen ontstaan. Dit type binding wordt aangetroffen in verbindingen zoals natriumchloride (NaCl) en kaliumjodide (KI).
3. Waterstofbruggen treedt op wanneer een waterstofatoom gebonden aan een zeer elektronegatief atoom (zoals stikstof, zuurstof of fluor) een dipool vormt met een ander elektronegatief atoom. Dit type binding wordt aangetroffen in watermoleculen en in veel biologische moleculen zoals eiwitten en DNA.
4. Metaalverbindingen treedt op wanneer de buitenste elektronen van metaalatomen worden gedelokaliseerd en gedeeld door alle atomen in het metaal. Dit type binding wordt aangetroffen in metalen zoals koper, ijzer en aluminium.
5. van der Waals-obligaties treedt op wanneer er een zwakke aantrekkingskracht bestaat tussen twee of meer moleculen of atomen. Dit type binding wordt aangetroffen in gassen zoals helium (He) en argon (Ar), maar ook in sommige vaste stoffen zoals grafiet. Van der Waals-bindingen zijn het zwakste type chemische binding en kunnen gemakkelijk worden verbroken.
 Bioaccumulatie van uitgefaseerde brandvertragers neemt langzaam af bij Amerikaanse zeearenden
Bioaccumulatie van uitgefaseerde brandvertragers neemt langzaam af bij Amerikaanse zeearenden Wetenschappers gebruiken mogelijk een gebrekkige strategie om te voorspellen hoe soorten het zullen doen onder de klimaatverandering, suggereert onderzoek
Wetenschappers gebruiken mogelijk een gebrekkige strategie om te voorspellen hoe soorten het zullen doen onder de klimaatverandering, suggereert onderzoek  New Delhi sluit elektriciteitscentrale in strijd tegen smog . Diwali
New Delhi sluit elektriciteitscentrale in strijd tegen smog . Diwali Stijgende zeeën dwingen huiseigenaren onder water te mobiliseren
Stijgende zeeën dwingen huiseigenaren onder water te mobiliseren Experts op het gebied van risicocommunicatie analyseren visuele reacties op afbeeldingen met tornadowaarschuwingen
Experts op het gebied van risicocommunicatie analyseren visuele reacties op afbeeldingen met tornadowaarschuwingen
Hoofdlijnen
- Big data helpt onderzoekers in de strijd om plantenindringers onder controle te krijgen
- Moderne genomica gebruiken om krokodillenschubben in vogelachtige veren te veranderen
- Zijn laboratoriumratten echt vatbaar voor kanker?
- Onderzoekers willen de darmgezondheid van vee verbeteren
- Satellietbeelden van de fluorescentie van planten kunnen de gewasopbrengsten voorspellen
- Nieuw onderzoek laat producenten zien waar en hoe ze cellulosebiobrandstofgewassen kunnen verbouwen
- Neteldieren controleren bacteriën op afstand
- Wat is vogelgriep, de ziekte die de virale TikTok-emu Emmanuel treft?
- Your Brain On: Exam Stress
- Nieuwe synthetische eiwitten wedijveren met hun natuurlijke tegenhangers in protonentransport

- Wetenschappers vinden schadelijke chemicaliën in huishoudstof

- Nieuw katalysatorcomposiet vermindert het gebruik van zeldzame aardelementen
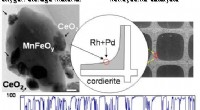
- Bierafval scheiden in eiwitten voor voedingsmiddelen, en vezels voor biobrandstoffen

- Nieuwe katalysatoren verbeteren de efficiëntie van de ureumsynthese bij omgevingsomstandigheden
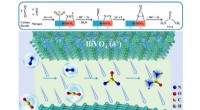
 Pet-tags koppelen veelgebruikte vlamvertragers aan hyperthyreoïdie bij katten
Pet-tags koppelen veelgebruikte vlamvertragers aan hyperthyreoïdie bij katten Nieuwe genen op verslechterend Y-chromosoom
Nieuwe genen op verslechterend Y-chromosoom Kan het opwekken van mammoeten helpen om de uitstoot in het Noordpoolgebied te stoppen?
Kan het opwekken van mammoeten helpen om de uitstoot in het Noordpoolgebied te stoppen? Vlam brandt uit tijdens NASA's langlopende brandexperiment met ruimtevaartuigen
Vlam brandt uit tijdens NASA's langlopende brandexperiment met ruimtevaartuigen  Analyse toont grote afname in strafrechtelijke veroordeling racekloof
Analyse toont grote afname in strafrechtelijke veroordeling racekloof Orbitale variaties van de aarde en synchrone ijstijden op zee-ijs
Orbitale variaties van de aarde en synchrone ijstijden op zee-ijs Hoe te bepalen of matrices enkelvoudig of niet-singulier zijn
Hoe te bepalen of matrices enkelvoudig of niet-singulier zijn  Onderzoek:wijdverbreid gebruik van betere maskers kan helpen om COVID-19 binnenshuis te beteugelen
Onderzoek:wijdverbreid gebruik van betere maskers kan helpen om COVID-19 binnenshuis te beteugelen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

