
Wetenschap
Is PO4 3-polair of niet-polair?
Het molecuul PO4 3− heeft vier zuurstofatomen die een centraal fosforatoom omringen, met een negatieve lading van 3. De elektronegativiteit van zuurstof is 3,44, terwijl die van fosfor 2,19 is. Dit verschil in elektronegativiteit zorgt ervoor dat de elektronen ongelijk verdeeld worden, wat resulteert in polaire bindingen tussen de fosfor- en zuurstofatomen. De geometrie van het molecuul is tetraëdrisch, waarbij de vier zuurstofatomen op de hoeken van een tetraëder zijn gerangschikt. Het fosforatoom bevindt zich in het midden van de tetraëder. De polaire bindingen tussen de fosfor- en zuurstofatomen creëren een netto negatieve lading op het molecuul, waardoor het polair wordt.
 Hoe de geheimen van de tardigrade levensreddende medicijnen zoals insuline kunnen verbeteren
Hoe de geheimen van de tardigrade levensreddende medicijnen zoals insuline kunnen verbeteren 3D-geprinte eiwitten presteren beter dan bestaande flexibele elektronicamaterialen
3D-geprinte eiwitten presteren beter dan bestaande flexibele elektronicamaterialen Catcher van de roggemethode detecteert roggegluteneiwitten in voedingsmiddelen
Catcher van de roggemethode detecteert roggegluteneiwitten in voedingsmiddelen Dunne waterlagen zijn veelbelovend voor de energieopslag van de toekomst
Dunne waterlagen zijn veelbelovend voor de energieopslag van de toekomst Kijk naar de onderstaande woordvergelijking:Glucose + Fructose ---> Sucrose Water Welke zin beschrijft de chemische reactie die plaatsvindt?
Kijk naar de onderstaande woordvergelijking:Glucose + Fructose ---> Sucrose Water Welke zin beschrijft de chemische reactie die plaatsvindt?
 Hoe de lay-outs of texturen van steden extreme weersomstandigheden beïnvloeden
Hoe de lay-outs of texturen van steden extreme weersomstandigheden beïnvloeden  Een wetenschapper en een supercomputer creëren een tornado
Een wetenschapper en een supercomputer creëren een tornado Nieuwe NASA-inzichten in het geheime leven van planten
Nieuwe NASA-inzichten in het geheime leven van planten Klimaatverandering:een veelbelovende toekomst voor katoen in Kameroen?
Klimaatverandering:een veelbelovende toekomst voor katoen in Kameroen?  Klimaatsimulaties project natter, winderige orkanen
Klimaatsimulaties project natter, winderige orkanen
Hoofdlijnen
- Wat is de basis voor uitzonderingen op het Aufbau-principe?
- Zijn religies ontstaan uit ons verkeerde begrip van het menselijk bewustzijn?
- Evolutie van binnenuit:onderzoek laat zien hoe virussen in darmbacteriën in de loop van de tijd veranderen
- Het langverwachte beleid van Chicago doet niet genoeg om trekvogels te beschermen, zeggen voorstanders
- Second Life-gegevens bieden inzicht in hoe trends zich verspreiden
- Hoe schimmels een dodelijke onderwateraanval uitvoeren op Aedes-muggenlarven
- Onderzoekers verduidelijken hoe cellen zichzelf verdedigen tegen virussen
- Veelkleurige planten zijn ineens een must-have in je interieur. Zo houd je ze in leven
- Hoe u invasieve ratten en muizen thuis kunt bestrijden zonder de inheemse fauna te schaden
- Hoe een bepaalde bacterie communiceert en ons ziek maakt
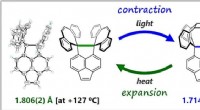
- Covalente koolstof-koolstofbindingen veel flexibeler dan verondersteld
- Mechanistische basis van zuurstofgevoeligheid in titanium

- Het ontsmetten van industrieel plastic afval om de planeet te ontlasten

- Vrijstaande microwire-array maakt flexibel zonnevenster mogelijk

 Parijs zet zich schrap voor recordhitte terwijl Europa opnieuw verschroeide
Parijs zet zich schrap voor recordhitte terwijl Europa opnieuw verschroeide Onderzoek onthult betrouwbaarheidsproblemen voor koolstofnanobuisjes in toekomstige elektronica
Onderzoek onthult betrouwbaarheidsproblemen voor koolstofnanobuisjes in toekomstige elektronica Zelfbewustzijnsles inspireert app voor intentie
Zelfbewustzijnsles inspireert app voor intentie Bij een pandemie, migratie uit dichtbevolkte steden effectiever dan het sluiten van grenzen
Bij een pandemie, migratie uit dichtbevolkte steden effectiever dan het sluiten van grenzen Diepbedroefde New Yorkers tellen de kosten van verwoestende regenval
Diepbedroefde New Yorkers tellen de kosten van verwoestende regenval Waarom de ringvingers van mannen langer zijn dan hun wijsvinger
Waarom de ringvingers van mannen langer zijn dan hun wijsvinger  Experiment laat zien waarom experts onbetrouwbaar kunnen zijn
Experiment laat zien waarom experts onbetrouwbaar kunnen zijn  Ernstige luchtvervuiling kan geboorteafwijkingen veroorzaken, sterfgevallen
Ernstige luchtvervuiling kan geboorteafwijkingen veroorzaken, sterfgevallen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

