
Wetenschap
Wat gebeurt er als natriumcarbonaat wordt verwarmd?
1. Initiële ontleding (rond 250-300°C):
- Natriumcarbonaat verliest watermoleculen (uitdroging) en wordt afgebroken tot natriumbicarbonaat (NaHCO3).
- Deze reactie kan worden weergegeven als:
Na2CO3(s) → NaHCO3(s) + CO2(g)
2. Verdere ontleding (bij hogere temperaturen, rond 850-900°C):
- Natriumbicarbonaat ontleedt verder, waarbij koolstofdioxide (CO2) en waterdamp (H2O) vrijkomen.
- Deze reactie kan worden weergegeven als:
2NaHCO3(s) → Na2CO3(s) + CO2(g) + H2O(g)
3. Vorming van natriumoxide:
- Bij nog hogere temperaturen (rond de 1.200-1.300°C) ontleedt natriumcarbonaat tot natriumoxide (Na2O).
- Bij dit proces komen ook kooldioxide en zuurstofgas vrij.
- Deze reactie kan worden weergegeven als:
Na2CO3(s) → Na2O(s) + CO2(g) + 1/2O2(g)
4. Potentiële vorming van natriumperoxide:
- In aanwezigheid van lucht (zuurstof) kan natriumoxide verder reageren en natriumperoxide (Na2O2) vormen.
- Deze reactie treedt op wanneer natriumoxide bij hogere temperaturen wordt blootgesteld aan zuurstof.
- De reactie kan worden weergegeven als:
2Na2O(s) + O2(g) → 2Na2O2(s)
5. Potentiële vorming van natriumsuperoxide:
- Onder specifieke omstandigheden kan natriumoxide ook reageren met zuurstof om natriumsuperoxide (NaO2) te vormen.
- Deze reactie treedt waarschijnlijker op bij hoge temperaturen en drukken, en in de aanwezigheid van zuivere zuurstof.
- De reactie kan worden weergegeven als:
Na2O(s) + O2(g) → 2NaO2(s)
Het is belangrijk op te merken dat de exacte reacties en gevormde producten kunnen variëren, afhankelijk van de specifieke omstandigheden en temperatuurbereiken.
 Wat voor soort reactie komt er met waterstofchloride en Alka Seltzer?
Wat voor soort reactie komt er met waterstofchloride en Alka Seltzer?  Zuur kan een belangrijk ingrediënt zijn voor een betere kleefkracht, elektronische componenten
Zuur kan een belangrijk ingrediënt zijn voor een betere kleefkracht, elektronische componenten Onderzoek geeft nieuw inzicht in de evolutie van het zenuwstelsel
Onderzoek geeft nieuw inzicht in de evolutie van het zenuwstelsel Waarom is de watercyclus belangrijk voor mensen en planten?
Waarom is de watercyclus belangrijk voor mensen en planten?  Hoe vind je verborgen oceanen op verre werelden? Gebruik chemie
Hoe vind je verborgen oceanen op verre werelden? Gebruik chemie
 De wereld heeft een nieuwe manier van denken nodig om te overleven, zegt Goodall
De wereld heeft een nieuwe manier van denken nodig om te overleven, zegt Goodall NASA's Terra-satelliet gluurt naar het 60-mijls brede oog van Super Typhoon Trami
NASA's Terra-satelliet gluurt naar het 60-mijls brede oog van Super Typhoon Trami Nieuw NASA Earth System Observatory om te helpen aanpakken, klimaatverandering tegengaan
Nieuw NASA Earth System Observatory om te helpen aanpakken, klimaatverandering tegengaan Afrikaans rookwolkverbindingsdoel van NASA-vluchten in de lucht
Afrikaans rookwolkverbindingsdoel van NASA-vluchten in de lucht Wetenschappers tonen aan dat bomen in nattere streken gevoeliger zijn voor droogte
Wetenschappers tonen aan dat bomen in nattere streken gevoeliger zijn voor droogte
Hoofdlijnen
- Beoordelingskader voor de instandhouding en het beheer van peulvruchtenplanten in Oost-Afrika aan de kust
- De reden voor het kleuren van een exemplaar op de microscoop
- Waarom is het belangrijk om lichaamsvet onder controle te houden bij mensen?
- MIT-onderzoeker legt uit hoe ratten denken
- Wetenschappers tonen de sleutelrol aan van de milt en extracellulaire blaasjes bij cryptische malaria-infecties
- Slapen of niet:onderzoekers onderzoeken complex genetisch netwerk achter slaapduur
- Eten of helpen zebramosselen giftige algen?
- Welke sequentie van RNA-basen vormt een paren DNA-streng die TACTGCA leest?
- Kunnen windturbines en trekvogels naast elkaar bestaan?
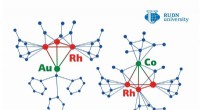
- Chemici suggereren een methode voor het produceren van op metaal gebaseerde katalysatoren met een ongeëvenaarde efficiëntie
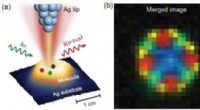
- Raman-picoscopie scannen:een nieuwe methode voor het bepalen van de moleculaire chemische structuur
- Met een meerlagige aanpak, een filter om te voldoen aan de behoeften van de zoetwatervoorziening

- Productie van waterstofperoxide opruimen

- Legeronderzoeker gebruikt wiskunde om nieuwe scheikunde te ontdekken

 Hoe te leren Buoyancy naar basisschoolkinderen
Hoe te leren Buoyancy naar basisschoolkinderen  Ik heb gehoord dat bankovervallers werden verijdeld door een 'kleurstofpakket' dat in hun geldvoorraad werd gestopt. Wat is pak"?
Ik heb gehoord dat bankovervallers werden verijdeld door een 'kleurstofpakket' dat in hun geldvoorraad werd gestopt. Wat is pak"?  BMW verontschuldigt zich voor motorbranden veroorzaakt door hardwareprobleem
BMW verontschuldigt zich voor motorbranden veroorzaakt door hardwareprobleem Atmosferische waterdamp in de stad Tel Aviv is geschikt om te drinken
Atmosferische waterdamp in de stad Tel Aviv is geschikt om te drinken Vraag en antwoord:Microsofts Lili Cheng praat over emotioneel intelligente machines
Vraag en antwoord:Microsofts Lili Cheng praat over emotioneel intelligente machines Afgeleide chauffeurs 29 keer meer kans om te verongelukken in een werkgebied op de snelweg
Afgeleide chauffeurs 29 keer meer kans om te verongelukken in een werkgebied op de snelweg Bank of England-chef veroordeelt cryptocurrencies; dringt aan op actie
Bank of England-chef veroordeelt cryptocurrencies; dringt aan op actie Hoe zuiger te berekenen Force
Hoe zuiger te berekenen Force
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

