
Wetenschap
Waarom zijn elementen uit groep 17 sterke niet-metalen en metalen uit groep 1?
1. Valentie-elektronen:
- Groep 17-elementen hebben zeven valentie-elektronen in hun buitenste schil, waardoor ze zeer elektronegatief zijn. Ze accepteren gemakkelijk één elektron om hun octetconfiguratie te voltooien en een stabiele elektronische configuratie te bereiken.
- Groep 1-elementen hebben daarentegen één valentie-elektron in hun buitenste schil, waardoor ze zeer elektropositief zijn. Ze hebben de neiging dit elektron gemakkelijk te verliezen om een stabiele octetconfiguratie te bereiken.
2. Ionisatie-energie:
- Groep 17-elementen hebben hogere ionisatie-energieën vergeleken met Groep 1-elementen. Dit betekent dat er meer energie nodig is om een elektron uit een halogeenatoom te verwijderen dan uit een alkalimetaalatoom.
- De hogere ionisatie-energie van halogenen maakt het moeilijk voor hen om elektronen te verliezen en positieve ionen te vormen. Dit draagt bij aan hun niet-metalen karakter.
3. Elektronegativiteit:
- Elektronegativiteit meet de aantrekkingskracht van een atoom voor elektronen in een chemische binding. Groep 17-elementen hebben hoge elektronegativiteitswaarden, wat wijst op hun sterke vermogen om elektronen aan te trekken.
- De hoge elektronegativiteit van halogenen stelt hen in staat gemakkelijk elektronen van andere atomen te accepteren, waardoor covalente bindingen worden gevormd.
4. Reactiviteit:
- Groep 17-elementen zijn zeer reactief vanwege hun sterke neiging om hun octet te voltooien. Ze reageren gemakkelijk met metalen, niet-metalen en zelfs organische verbindingen.
- Groep 1-metalen zijn ook zeer reactief, maar op een andere manier. Ze hebben de neiging hun enkele valentie-elektron gemakkelijk te verliezen en vormen ionische bindingen met niet-metalen.
Samenvattend maken de verschillen in het aantal valentie-elektronen, ionisatie-energie, elektronegativiteit en reactiviteit de elementen van Groep 17 tot sterke niet-metalen, terwijl elementen van Groep 1 zeer reactieve metalen zijn. Deze eigenschappen bepalen het chemische gedrag en de kenmerken van deze elementen en beïnvloeden de vorming van verbindingen.
 Ontwikkeling van een nieuwe methode voor het synthetiseren van dialkylethers met behulp van drie katalysatoren die alkenen hydroxyleren
Ontwikkeling van een nieuwe methode voor het synthetiseren van dialkylethers met behulp van drie katalysatoren die alkenen hydroxyleren Gereedschappen en apparatuur gebruikt voor de pluimveehouderij
Gereedschappen en apparatuur gebruikt voor de pluimveehouderij Wetenschapsprojecten: hoe warm en koud water een ballon verandert
Wetenschapsprojecten: hoe warm en koud water een ballon verandert  Hoe zet je 2-pentyn om in 1-penteen?
Hoe zet je 2-pentyn om in 1-penteen?  Microscopisch vibrerend circulair dichroïsme maakt supramoleculaire chiraliteitsmapping mogelijk
Microscopisch vibrerend circulair dichroïsme maakt supramoleculaire chiraliteitsmapping mogelijk
 Ideeën om te doen voor Science Fair voor vijfde klas
Ideeën om te doen voor Science Fair voor vijfde klas  TV-verslaggeving van wielerwedstrijden kan helpen de effecten van klimaatverandering vast te leggen
TV-verslaggeving van wielerwedstrijden kan helpen de effecten van klimaatverandering vast te leggen Het belang van vliegen
Het belang van vliegen  Waarom zien mannetjes en vrouwtjes van sommige soorten er zo verschillend uit?
Waarom zien mannetjes en vrouwtjes van sommige soorten er zo verschillend uit?  Meer sneeuwval compenseert zeespiegelstijging door smeltende Antarctische ijskap
Meer sneeuwval compenseert zeespiegelstijging door smeltende Antarctische ijskap
Hoofdlijnen
- Onderzoek onthult de sleutelrol van de communicatie tussen planten en bacteriën bij de assemblage van een gezond plantenmicrobioom
- Een pinguïn met een onconventionele roep inspireert onderzoekers om de manier waarop ze pinguïns bestuderen te veranderen
- Wat is sterker:nature of nurture?
- Hoeveel verschillende peptiden kunnen worden gevormd door alle aminozuren slechts één keer te gebruiken?
- De code van colibactine kraken:studie onderzoekt hoe de verbinding het DNA beschadigde om het verband met kanker te begrijpen
- Zou u op een Democraat stemmen die zich als Republikein gedraagt?
- Onderzoek onderzoekt energie- en landgebruikspraktijken op Amerikaanse golfbanen
- Wat zijn de verschillen tussen een plant en een dierlijke cel onder een microscoop?
- Kweek vers voedsel in uw huis - verticaal
- Wetenschappers ontdekken dat de chemie van zware elementen kan veranderen bij hoge druk

- Een virtueel substraat opent de weg naar oxidefilms op silicium voor toepassing in 5G, MEMS, sensoren en kwantumberekening

- Nieuw ontdekt enzym gebruikt een ongebruikelijk mechanisme om een molecuul met een vreselijke geur te genereren

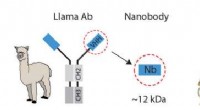
- Van lama afgeleide nanobodies als nieuw hulpmiddel bij het oplossen van kristalstructuur
- Deponeren van ijzersoorten in ZSM-5 om cyclohexaan te oxideren tot cyclohexanon

 Rotsen en edelstenen polijsten zonder een steen Tumbler
Rotsen en edelstenen polijsten zonder een steen Tumbler NASA-ruimtevaartuig breekt record door het dichtst bij Sun . te komen
NASA-ruimtevaartuig breekt record door het dichtst bij Sun . te komen Patronen van de maan
Patronen van de maan  Hoe de St. Louis Arch tegen alle verwachtingen in standhoudt
Hoe de St. Louis Arch tegen alle verwachtingen in standhoudt  Welke impact heeft ozon op een exoplaneet?
Welke impact heeft ozon op een exoplaneet?  Wat is een sterkere waterstofbinding of een chemische binding?
Wat is een sterkere waterstofbinding of een chemische binding?  Nederlandse arrestatie man gekoppeld aan valutamixer Tornado Cash
Nederlandse arrestatie man gekoppeld aan valutamixer Tornado Cash Toepasbaarheid van dynamische facilitatietheorie op binaire harde schijfsystemen
Toepasbaarheid van dynamische facilitatietheorie op binaire harde schijfsystemen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

