
Wetenschap
Wat is de chemische vergelijking voor het verbranden van fossiele brandstoffen?
Koolwaterstof (brandstof) + zuurstof (O2) → Kooldioxide (CO2) + water (H2O) + warmte-energie
Hier is een meer gedetailleerde uitleg:
Wanneer fossiele brandstoffen worden verbrand, reageren ze met zuurstof uit de lucht. Het hoofdbestanddeel van de meeste fossiele brandstoffen is koolstof, dus het primaire verbrandingsproduct is koolstofdioxide (CO2). Waterstof is ook aanwezig in fossiele brandstoffen, dus waterdamp (H2O) is een ander verbrandingsproduct.
De hoeveelheid geproduceerd CO2 en H2O hangt af van de specifieke koolwaterstofbrandstof die wordt verbrand. De verbranding van methaan (CH4), het hoofdbestanddeel van aardgas, produceert bijvoorbeeld één molecuul CO2 en twee moleculen H2O voor elk verbrand molecuul methaan.
Naast CO2 en H2O komen bij de verbranding van fossiele brandstoffen ook andere verontreinigende stoffen in de atmosfeer terecht, waaronder stikstofoxiden (NOx), zwaveloxiden (SOx) en fijnstof.
De chemische vergelijking voor de volledige verbranding van methaan is:
CH4 + 2O2 → CO2 + 2H2O + Warmte-energie
Over het geheel genomen is de verbranding van fossiele brandstoffen een chemisch proces waarbij koolwaterstoffen met zuurstof reageren om kooldioxide, waterdamp en andere verontreinigende stoffen te produceren, samen met het vrijkomen van warmte-energie.
 Wat is het verwachte reactieproduct tussen KOH plus NI?
Wat is het verwachte reactieproduct tussen KOH plus NI?  Een zeer goedkope zelfgemaakte fotovoltaïsche zonnecel maken
Een zeer goedkope zelfgemaakte fotovoltaïsche zonnecel maken Onderzoekers onthullen een geheim van sterkere metalen
Onderzoekers onthullen een geheim van sterkere metalen Stijve, pijnlijke knieën? In het laboratorium gemaakte kraakbeengel presteert beter dan het echte werk
Stijve, pijnlijke knieën? In het laboratorium gemaakte kraakbeengel presteert beter dan het echte werk Gebruik maken van generatieve AI om krachtige en selectieve MYT1-remmers te identificeren voor de behandeling van kanker
Gebruik maken van generatieve AI om krachtige en selectieve MYT1-remmers te identificeren voor de behandeling van kanker
 Verborgen dreiging:enorme methaanlekken versnellen klimaatverandering
Verborgen dreiging:enorme methaanlekken versnellen klimaatverandering Cycloontol bereikt 95 terwijl Bangladesh en India beginnen op te dweilen
Cycloontol bereikt 95 terwijl Bangladesh en India beginnen op te dweilen Onderzoekers ontdekken hoe kleine plastics door het milieu glippen
Onderzoekers ontdekken hoe kleine plastics door het milieu glippen Hoe kunnen Tyfoons voorkomen?
Hoe kunnen Tyfoons voorkomen?  Agroforestry kan het VK helpen de verplichtingen inzake klimaatverandering na te komen zonder de veestapel te verminderen
Agroforestry kan het VK helpen de verplichtingen inzake klimaatverandering na te komen zonder de veestapel te verminderen
Hoofdlijnen
- De Saguaro Cactus is een iconisch symbool van het Amerikaanse zuidwesten
- Kan genetische verbetering de mensheid uiteindelijk dommer maken?
- Het vastleggen van de waardeketen leidt tot toekomstige bezorgdheid over de duurzaamheid van bossen
- Onderzoek werpt licht op hoe antibiotica klittenband bacteriën doodt
- Hoe DNA-reparatie kanker helpt voorkomen
- Zou de ontdekking van een sleutelgensysteem de laatste zucht van koralen kunnen verstikken?
- Waarom wordt gramkleuring meestal niet toegepast op eukaryoten?
- Onderzoekers tonen aan dat de besmetting met pesticiden verder gaat dan alleen de schil van de appel
- CRISPR-dragende nanodeeltjes bewerken het genoom
- Team ontwikkelt eenvoudige hydrogel-modificatiemethode voor rekbare en transparante elektronica
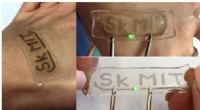
- Polymeer maakt sterkere recyclebare thermoplasten mogelijk

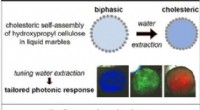
- Zelfassemblage van responsieve fotonische biobased materialen in vloeibare knikkers
- Computerwetenschappers en materiaalonderzoekers werken samen om staalclassificatie te optimaliseren

- Metabolische activiteit van bruin vetweefsel gemakkelijker te verifiëren met nieuwe methode

 Hoe bacteriën resistentie tegen antibiotica ontwikkelen
Hoe bacteriën resistentie tegen antibiotica ontwikkelen  Klein fragment van een komeet gevonden in een meteoriet
Klein fragment van een komeet gevonden in een meteoriet Fysica van gigantische bellen barst geheim van vloeistofmechanica
Fysica van gigantische bellen barst geheim van vloeistofmechanica CO2 belasten klinkt misschien als een goed idee, maar werkt het?
CO2 belasten klinkt misschien als een goed idee, maar werkt het? Hoe de oorlog in Soedan de gevolgen van de klimaatcrisis in Hoorn-Afrika zou kunnen verergeren
Hoe de oorlog in Soedan de gevolgen van de klimaatcrisis in Hoorn-Afrika zou kunnen verergeren  NASA volgde kleine asteroïde voordat hij uiteenviel in de atmosfeer
NASA volgde kleine asteroïde voordat hij uiteenviel in de atmosfeer Koraaltrucs voor aanpassing aan oceaanverzuring
Koraaltrucs voor aanpassing aan oceaanverzuring Puerto Rico is vatbaar voor meer overstromingen dan het eiland aankan
Puerto Rico is vatbaar voor meer overstromingen dan het eiland aankan
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

