
Wetenschap
CRISPR-dragende nanodeeltjes bewerken het genoom
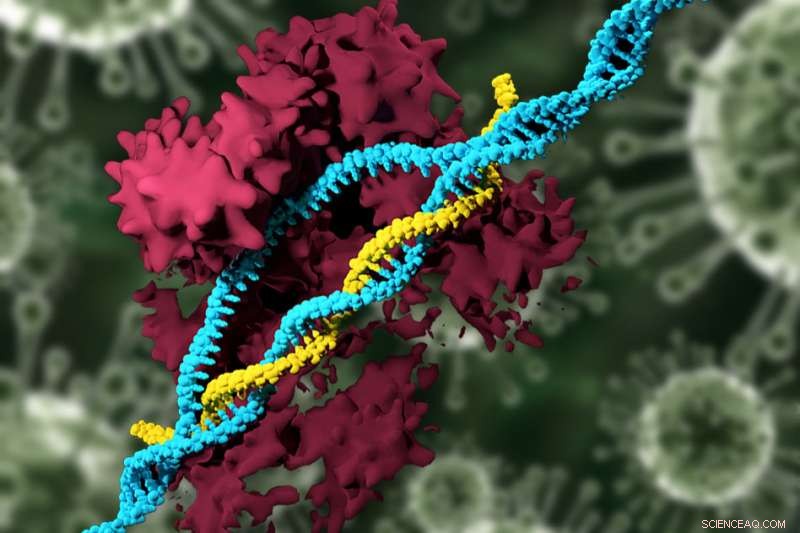
In een nieuwe studie, MIT-onderzoekers hebben nanodeeltjes ontwikkeld die het CRISPR-genoombewerkingssysteem kunnen leveren en specifiek genen kunnen wijzigen, het elimineren van de noodzaak om virussen te gebruiken voor levering. Krediet:MIT
In een nieuwe studie, MIT-onderzoekers hebben nanodeeltjes ontwikkeld die het CRISPR-genoombewerkingssysteem kunnen leveren en specifiek genen in muizen kunnen wijzigen. Het team gebruikte nanodeeltjes om de CRISPR-componenten te vervoeren, het elimineren van de noodzaak om virussen te gebruiken voor levering.
Met behulp van de nieuwe bezorgtechniek, konden de onderzoekers bepaalde genen uitsnijden in ongeveer 80 procent van de levercellen, het beste succespercentage ooit behaald met CRISPR bij volwassen dieren.
"Wat hier echt opwindend is, is dat we hebben laten zien dat je een nanodeeltje kunt maken dat kan worden gebruikt om permanent en specifiek het DNA in de lever van een volwassen dier te bewerken, " zegt Daniël Anderson, een universitair hoofddocent bij het MIT's Department of Chemical Engineering en een lid van het Koch Institute for Integrative Cancer Research en het Institute for Medical Engineering and Science (IMES) van MIT.
Een van de genen waarop dit onderzoek is gericht, bekend als Pcsk9, reguleert het cholesterolgehalte. Mutaties in de menselijke versie van het gen zijn geassocieerd met een zeldzame aandoening die dominante familiaire hypercholesterolemie wordt genoemd, en de FDA keurde onlangs twee antilichaamgeneesmiddelen goed die Pcsk9 remmen. Echter, deze antilichamen moeten regelmatig worden ingenomen, en voor de rest van het leven van de patiënt, therapie te geven. De nieuwe nanodeeltjes bewerken het gen permanent na een enkele behandeling, en de techniek biedt ook belofte voor de behandeling van andere leveraandoeningen, volgens het MIT-team.
Anderson is de senior auteur van de studie, die verschijnt in het nummer van 13 november van Natuur Biotechnologie . De hoofdauteur van het artikel is onderzoeker Hao Yin van het Koch Institute. Andere auteurs zijn onder meer David H. Koch Institute Professor Robert Langer van MIT, professoren Victor Koteliansky en Timofei Zatsepin van het Skolkovo Instituut voor Wetenschap en Technologie, en professor Wen Xue van de medische faculteit van de Universiteit van Massachusetts.
Ziekte als doelwit
Veel wetenschappers proberen veilige en efficiënte manieren te ontwikkelen om de componenten te leveren die nodig zijn voor CRISPR, dat bestaat uit een DNA-knippend enzym genaamd Cas9 en een kort RNA dat het enzym naar een specifiek gebied van het genoom leidt, regisseren Cas9 waar het moet worden gesneden.
In de meeste gevallen, onderzoekers vertrouwen op virussen om het gen voor Cas9 te dragen, evenals de RNA-gidsstreng. In 2014, Anderson, Yin, en hun collega's ontwikkelden een niet-viraal toedieningssysteem in de allereerste demonstratie van het genezen van een ziekte (de leveraandoening tyrosinemie) met CRISPR bij een volwassen dier. Echter, dit type levering vereist een hogedrukinjectie, een methode die ook enige schade aan de lever kan veroorzaken.
Later, de onderzoekers toonden aan dat ze de componenten zonder de hogedrukinjectie konden afleveren door messenger-RNA (mRNA) dat voor Cas9 codeert, te verpakken in een nanodeeltje in plaats van een virus. Met behulp van deze aanpak, waarbij het gids-RNA nog werd afgeleverd door een virus, de onderzoekers waren in staat om het doelgen in ongeveer 6 procent van de hepatocyten te bewerken, wat voldoende is om tyrosinemie te behandelen.
Hoewel die bezorgtechniek veelbelovend is, in sommige situaties zou het beter zijn om een volledig niet-viraal toedieningssysteem te hebben, zegt Anderson. Een overweging is dat als een bepaald virus eenmaal is gebruikt, de patiënt zal er antilichamen tegen ontwikkelen, zodat het niet meer gebruikt kon worden. Ook, sommige patiënten hebben reeds bestaande antilichamen tegen de virussen die worden getest als CRISPR-bezorgingsvehikels.
In de nieuwe Nature Biotechnology-paper, de onderzoekers kwamen met een systeem dat zowel Cas9 als de RNA-gids levert met behulp van nanodeeltjes, zonder dat er virussen nodig zijn. Om de gids-RNA's te leveren, ze moesten eerst het RNA chemisch modificeren om het te beschermen tegen enzymen in het lichaam die het normaal zouden afbreken voordat het zijn bestemming kon bereiken.
De onderzoekers analyseerden de structuur van het complex gevormd door Cas9 en de RNA-gids, of sgRNA, om erachter te komen welke secties van de gids-RNA-streng chemisch kunnen worden gemodificeerd zonder de binding van de twee moleculen te verstoren. Op basis van deze analyse, ze hebben veel mogelijke combinaties van aanpassingen gemaakt en getest.
"We gebruikten de structuur van het Cas9- en sgRNA-complex als richtlijn en deden tests om erachter te komen dat we maar liefst 70 procent van het gids-RNA kunnen wijzigen. " zegt Yin. "We zouden het sterk kunnen wijzigen en de binding van sgRNA en Cas9 niet beïnvloeden, en deze verbeterde wijziging verhoogt echt de activiteit."
De lever herprogrammeren
De onderzoekers verpakten deze gemodificeerde RNA-gidsen (die ze verbeterde sgRNA noemen) in lipidenanodeeltjes, die ze eerder hadden gebruikt om andere soorten RNA aan de lever af te geven, en injecteerde ze in muizen samen met nanodeeltjes die mRNA bevatten dat codeert voor Cas9.
Ze experimenteerden met het uitschakelen van een paar verschillende genen die door hepatocyten tot expressie worden gebracht, maar richtten de meeste van hun aandacht op het cholesterolregulerende Pcsk9-gen. De onderzoekers konden dit gen in meer dan 80 procent van de levercellen elimineren, en het Pcsk9-eiwit was niet detecteerbaar in deze muizen. Ze vonden ook een daling van 35 procent in het totale cholesterolgehalte van de behandelde muizen.
De onderzoekers werken nu aan het identificeren van andere leverziekten die baat kunnen hebben bij deze aanpak, en het bevorderen van deze benaderingen in de richting van gebruik bij patiënten.
"Ik denk dat het hebben van een volledig synthetisch nanodeeltje dat genen specifiek kan uitschakelen een krachtig hulpmiddel kan zijn, niet alleen voor Pcsk9, maar ook voor andere ziekten, " Zegt Anderson. "De lever is een heel belangrijk orgaan en is ook een bron van ziekte voor veel mensen. Als u het DNA van uw lever kunt herprogrammeren terwijl u het nog gebruikt, we denken dat er veel ziekten zijn die kunnen worden aangepakt."
"We zijn erg verheugd om te zien dat deze nieuwe toepassing van nanotechnologie nieuwe wegen opent voor genbewerking, ’ voegt Langer toe.
 Wetenschappers vinden nieuwe manieren om chemicaliën voor bioraffinage te gebruiken
Wetenschappers vinden nieuwe manieren om chemicaliën voor bioraffinage te gebruiken Neutronenspectroscopie onthult dat een gewone zuurstofsponskatalysator ook waterstof opneemt
Neutronenspectroscopie onthult dat een gewone zuurstofsponskatalysator ook waterstof opneemt Biofysici richten zich op het mechanisme dat het Zika-virus zo gevaarlijk maakt
Biofysici richten zich op het mechanisme dat het Zika-virus zo gevaarlijk maakt Hoe zuur zijn atomen?
Hoe zuur zijn atomen? Onderzoekers verbeteren de beschrijving van defecte oxiden met de eerste principes-berekening
Onderzoekers verbeteren de beschrijving van defecte oxiden met de eerste principes-berekening
 Colombia verbiedt sportjacht
Colombia verbiedt sportjacht Marine krijgt concurrentievoordeel met onderzoek naar biologische oceaanzwermen
Marine krijgt concurrentievoordeel met onderzoek naar biologische oceaanzwermen Kunnen steden slimmer omgaan met extreem weer?
Kunnen steden slimmer omgaan met extreem weer? Het COVID-19-herstel in Afrika moet de voordelen van natuur en natuurbehoud benutten
Het COVID-19-herstel in Afrika moet de voordelen van natuur en natuurbehoud benutten Onzekerheden over de ijskap kunnen betekenen dat de zeespiegel meer stijgt dan voorspeld
Onzekerheden over de ijskap kunnen betekenen dat de zeespiegel meer stijgt dan voorspeld
Hoofdlijnen
- Algen kunnen planeet voeden en voeden met behulp van nieuwe hightech tool
- Wat gebeurt er als je een lijk ontdooit?
- De ontwerpprincipes van celcompartimenten blootleggen
- Studie identificeert knelpunten in vroege zeegrasgroei
- 85 nieuwe soorten beschreven door de California Academy of Sciences in 2017
- Welk type RNA draagt aminozuren naar de vertaalsite?
- 6 soorten vrij beweegbare gewrichten
- Theorie van de evolutie van geslachten getest met algen
- Een bijtend rapport:onderzoek toont aan dat klimaatverandering een grote bedreiging vormt voor hommels
- Voedingsvormen van bacteriën
- Verklaring van celspecialisatie

- Diversiteit van grote dieren speelt een belangrijke rol in koolstofcyclus

- Opwarming van het klimaat zou de bacteriële impact op Chesapeake Bay-schelpdieren kunnen vergroten, recreatie
- Iran verhuist om laatste mascotte Aziatische cheeta's te redden

 Kleine op chips gebaseerde methaanspectrometer kan de uitstoot van broeikasgassen helpen verminderen
Kleine op chips gebaseerde methaanspectrometer kan de uitstoot van broeikasgassen helpen verminderen Afbeeldingen laten zien waar lava door de muur van een krater op Mars brak en deze begon te vullen
Afbeeldingen laten zien waar lava door de muur van een krater op Mars brak en deze begon te vullen Ja, Australië is een land van overstromende regens, maar klimaatverandering kan het erger maken
Ja, Australië is een land van overstromende regens, maar klimaatverandering kan het erger maken Welke gevolgen hebben chloorfluorkoolwaterstoffen op mensen?
Welke gevolgen hebben chloorfluorkoolwaterstoffen op mensen?  Oude zwembaden in de buurt van Jeruzalem klaar voor renovatie
Oude zwembaden in de buurt van Jeruzalem klaar voor renovatie Onderzoekers om te ontwerpen, instrument bouwen om metalen asteroïde te verkennen
Onderzoekers om te ontwerpen, instrument bouwen om metalen asteroïde te verkennen Fatale horizon, gedreven door verzuring, sluit zich aan bij mariene organismen in de Zuidelijke Oceaan
Fatale horizon, gedreven door verzuring, sluit zich aan bij mariene organismen in de Zuidelijke Oceaan Neutronen onderzoeken Einstein-diffusie om de hoop op een revolutie in koolstofnanotechnologie te ondersteunen
Neutronen onderzoeken Einstein-diffusie om de hoop op een revolutie in koolstofnanotechnologie te ondersteunen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Portuguese | Swedish | German | Dutch | Danish | Norway | Spanish |

-
Wetenschap © https://nl.scienceaq.com

