
Wetenschap
Duitse wetenschappers ontwikkelen een nieuwe mutasynthese-aanpak voor de derivatisering van antibiotica
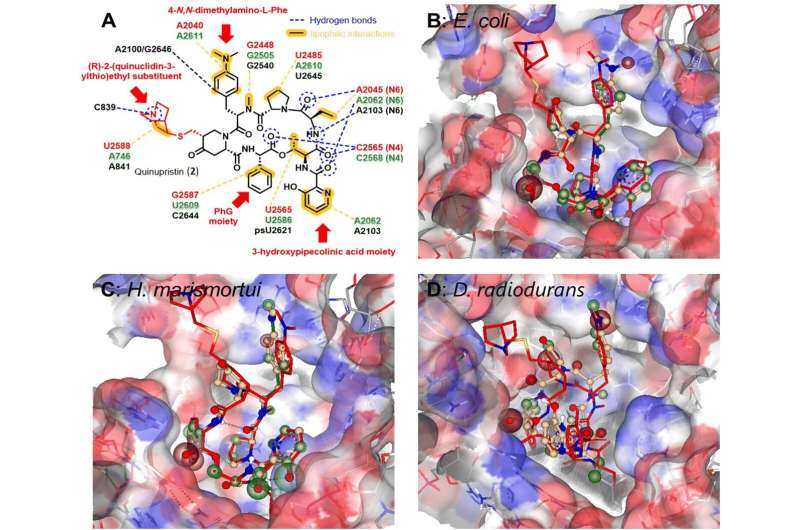
Een nieuwe methode voor de derivatisering van antibiotica is ontwikkeld door professor dr. Yvonne Mast, hoofd van de afdeling Bioresources for Bioeconomy and Health Research, en haar werkgroep bij het Leibniz Instituut DSMZ-Duitse verzameling van micro-organismen en celculturen.
P>Antibiotica zijn medicinaal belangrijke verbindingen die vaak door micro-organismen worden geproduceerd. Dergelijke natuurlijke stoffen hebben vaak een chemisch complexe structuur en kunnen daarom moeilijk of zelfs onmogelijk zijn om chemisch te synthetiseren of te modificeren door middel van semi-synthese. Het aanpassen van deze stoffen is echter vaak nodig om de werkzaamheid te verbeteren of, zoals in het geval van antibiotica, om resistentiebrekende eigenschappen te verlenen.
Mutasynthese biedt een alternatief voor de chemische modificatie of "derivatisering" van stoffen. Deze aanpak genereert mutanten van antibioticaproducerende micro-organismen, waarbij de genen voor de antibioticaprecursor(s) worden geïnactiveerd, zodat het micro-organisme deze niet langer kan produceren.
Door mutanten te "voeden" met gemodificeerde voorproducten (de voorloperderivaten), worden deze vervolgens opgenomen in het voorlopermolecuul van het antibioticum, wat resulteert in de productie van nieuwe antibiotische derivaten.
Mutasynthese:een aanpak om antibiotica aan te passen
In een onderzoek dat onlangs is gepubliceerd in RSC Chemical Biology beschrijft de werkgroep van prof. Mast een nieuwe mutasynthesebenadering voor de derivatisering van het antibioticum pristinamycine I. Pristinamycine is een streptogramine-antibioticum dat wordt gebruikt als noodmedicijn tegen resistente pathogenen.
"We hebben pristinamycine I aangepast op basis van de aminozuurvoorloper fenylglycine door middel van mutasynthese", legt antibioticaonderzoeker Yvonne Mast uit.
"Dit was alleen mogelijk omdat we eerder de biosynthesegenen voor fenylglycine hadden geïdentificeerd en functioneel gekarakteriseerd, waardoor we in onze huidige studie twee nieuwe gehalogeneerde bioactieve pristinamycine I-derivaten konden genereren."
"De nieuwigheid van deze studie ligt in het feit dat we een biotransformatieproces hebben gekoppeld aan mutasynthese, waarbij de voorloper van het fenylglycinederivaat wordt geleverd door een genetisch gemodificeerde bacteriestam (E. coli-stam). Tot nu toe is dit het enige biotechnologische proces van zijn soort, die we mutasynthese 2.0 hebben genoemd", zegt prof. Mast.
Meer informatie: Oliver Hennrich et al, Biotransformatie-gekoppelde mutasynthese voor de generatie van nieuwe pristinamycinederivaten door het fenylglycineresidu te engineeren, RSC Chemical Biology (2023). DOI:10.1039/D3CB00143A
Aangeboden door Leibniz-Institut DSMZ-Deutsche Sammlung von Mikroorganismen und Zellkulturen GmbH
 Een robuust materiaal voor de opname en opslag van ammoniak met dichtheden die dicht bij die van het vloeibaar gemaakte gas liggen
Een robuust materiaal voor de opname en opslag van ammoniak met dichtheden die dicht bij die van het vloeibaar gemaakte gas liggen Molare-oplossingen maken
Molare-oplossingen maken Hoe de geheimen van de tardigrade levensreddende medicijnen zoals insuline kunnen verbeteren
Hoe de geheimen van de tardigrade levensreddende medicijnen zoals insuline kunnen verbeteren Samenwerking vormt de strategie voor het vasthouden van extracellulaire blaasjes
Samenwerking vormt de strategie voor het vasthouden van extracellulaire blaasjes Wetenschappers kijken voor het eerst naar het geometrische fase-effect in een chemische reactie
Wetenschappers kijken voor het eerst naar het geometrische fase-effect in een chemische reactie
 Waarom Plant Intelligence Real
Waarom Plant Intelligence Real Tropische bomen behouden hoge koolstofaccumulatie tot op hoge leeftijd
Tropische bomen behouden hoge koolstofaccumulatie tot op hoge leeftijd Studie vindt chloroformemissies, in opkomst in Oost-Azië, kan het herstel van ozon tot acht jaar vertragen
Studie vindt chloroformemissies, in opkomst in Oost-Azië, kan het herstel van ozon tot acht jaar vertragen Droger, warmere nachtlucht maakt sommige westerse bosbranden 's nachts actiever
Droger, warmere nachtlucht maakt sommige westerse bosbranden 's nachts actiever NASA bekeek regenval in tropische storm Merbok voor aanlanding
NASA bekeek regenval in tropische storm Merbok voor aanlanding
Hoofdlijnen
- De levenscyclus van Gymnosperms
- Worden we geboren met een moreel kompas?
- Welk deel van de hersenen controleert emoties?
- Onderzoekers houden onderzoek naar de houding ten opzichte van stadsdieren en waar mensen willen dat ze leven
- Druk in de baarmoeder kan de gezichtsontwikkeling beïnvloeden
- Tropische bodems zeer gevoelig voor opwarming van de aarde, waarschuwen onderzoekers
- Hedendaagse bosbranden zijn niet ernstiger dan historisch gezien in de droge bossen in het westen van de VS:studie
- Hoe sabeltandtijgers hun lange bovenste hoektanden kregen
- Voorbeelden van diffusie in organen
- Gewasafval omzetten in hoogwaardige modeproducten

- De houdbaarheid van voedsel verlengen met nanomaterialen

- Microfluïdisch systeem met celscheidende krachten kan ontrafelen hoe nieuwe pathogenen aanvallen
- Onderzoek onthult hoe een klein molecuul de verwijdering van overtollig cholesterol bevordert
- Schuimbruis

 Wat is een prehistorische toolkit en hoe zou het de menselijke geschiedenis kunnen herschrijven?
Wat is een prehistorische toolkit en hoe zou het de menselijke geschiedenis kunnen herschrijven?  Zou het volgende hoofdstuk van AI het ontwerp van voelmachines kunnen brengen?
Zou het volgende hoofdstuk van AI het ontwerp van voelmachines kunnen brengen? Binaire evolutie van de milliseconde pulsar SAX J1808.4–3658 onderzocht door onderzoekers
Binaire evolutie van de milliseconde pulsar SAX J1808.4–3658 onderzocht door onderzoekers Een licht werpen op de verborgen eigenschappen van kwantummaterialen
Een licht werpen op de verborgen eigenschappen van kwantummaterialen  2018 begint met recordkou in delen van het Midwesten
2018 begint met recordkou in delen van het Midwesten Zoeken naar geluidsgolven in de superfluïde volgordeparameter
Zoeken naar geluidsgolven in de superfluïde volgordeparameter Dunne lagen sediment wijzen op vroege aankomst van leven op het land
Dunne lagen sediment wijzen op vroege aankomst van leven op het land Noord-blootgestelde ijskliffen versnellen het smelten van gletsjers
Noord-blootgestelde ijskliffen versnellen het smelten van gletsjers
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

