
Wetenschap
Belangrijke mijlpaal op weg naar overgangsmetaalkatalyse met aluminium
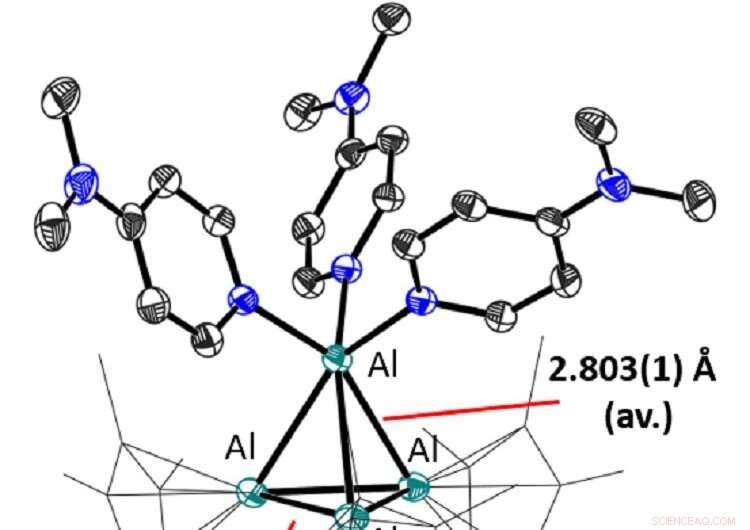
Credit:Albert-Ludwigs-Universität Freiburg im Breisgau
Chemici Philipp Dabringhaus, Julie Willrett en Prof. Dr. Ingo Krossing van het Instituut voor Anorganische en Analytische Chemie aan de Universiteit van Freiburg zijn erin geslaagd het laagwaardige kationische aluminiumcomplex [Al(AlCp*)3 ] + door een metathesereactie. Het team presenteert hun onderzoekswerk in het tijdschrift Nature Chemistry .
"In de chemie zijn kationische laagwaardige aluminiumverbindingen zeer gewild vanwege hun potentiële overgangsmetaalachtige ambifiele reactiviteit. Talloze eerdere pogingen om kationische laagwaardige aluminiumverbindingen te synthetiseren door oxidatieve of reductieve methoden zijn echter grotendeels mislukt," Krossing legt uit. Tot dusver, zei hij, is er slechts één voorbeeld geweest van een kationische, laagwaardige aluminiumverbinding, maar deze kan niet worden bereid door rationele synthese. "We laten nu zien dat er toch een onverwacht gemakkelijke toegang is tot laagwaardige aluminiumcomplexen met metathese", zegt Krossing. Bij metathese worden deelstructuren eenvoudig uitgewisseld tussen de reactiepartners.
Aluminium als goedkoper alternatief voor katalyse
De scheikundigen van Freiburg maakten het zout [Al(AlCp*)3 ] + [Al(OC{CF3 .) )3 }4 ] – van de Schnöckel-tetrameer (AlCp*)4 , waarin aluminium al aanwezig is in de +1 oxidatietoestand. De (AlCp*)4 reageerde met Li[Al{OC(CF3 .) )3 }4 ] en het reactiemengsel veranderde onmiddellijk van geel in rood. Toen het reactiemengsel was gekristalliseerd, verkregen de wetenschappers de [Al(AlCp*)3 ] + [Al(OC{CF3 .) )3 }4 ] – zout als donkerpaarse kristallen. "Röntgenkristallografische, UV-spectrometrische en computationele studies wijzen op de aanwezigheid van de dimere structuur zowel in de vaste toestand als in oplossing bij hoge concentratie en lage temperatuur, maar bij lage concentratie en kamertemperatuur vormt het monomeer. Dit duidt duidelijk op ambifiele reactiviteit van het kation," zei Dabringhaus.
"Daarom kan dit zout potentieel worden gebruikt als bouwsteen voor een [:Al(L)3 ] + zout dat, vanwege zijn kationische aard, in staat zou kunnen zijn om omkeerbare oxidatieve toevoegingen en reductieve eliminaties van kleine moleculen uit te voeren", legt Krossing uit. "Dit brengt ons een stap dichter bij ons langetermijndoel om katalyse te bereiken - momenteel gedaan met dure en zeldzame overgangsmetalen - met aluminium. Aluminium is het op één na meest voorkomende element in de aardkorst en is daartoe in principe in staat, zoals ons werk laat zien. Maar helaas zal het waarschijnlijk nog minstens 20 jaar duren voordat ons onderzoek hierop wordt toegepast." + Verken verder
Chemici ontwikkelen nieuw reagens voor de-elektronisatie
 Rood, groente, en blauw licht kan worden gebruikt om genexpressie in gemanipuleerde E. coli te regelen
Rood, groente, en blauw licht kan worden gebruikt om genexpressie in gemanipuleerde E. coli te regelen Veiliger nastreven, goedkopere geneesmiddelen via elektromagnetische controle op atomair niveau
Veiliger nastreven, goedkopere geneesmiddelen via elektromagnetische controle op atomair niveau Opschalen naar nieuwe hoogten met gekko-geïnspireerde lijm
Opschalen naar nieuwe hoogten met gekko-geïnspireerde lijm Een platform om fluorescent gelabelde eiwitten te bereiden en hun natuurlijke omgeving te simuleren
Een platform om fluorescent gelabelde eiwitten te bereiden en hun natuurlijke omgeving te simuleren Hoe de hoeveelheid reactant in overmaat
Hoe de hoeveelheid reactant in overmaat
 Wetenschappers vinden manier om mineraal te maken dat CO2 uit de atmosfeer kan verwijderen
Wetenschappers vinden manier om mineraal te maken dat CO2 uit de atmosfeer kan verwijderen Dalende zeespiegel zorgde ervoor dat vulkanen overstroomden
Dalende zeespiegel zorgde ervoor dat vulkanen overstroomden Onderzoekers simuleren processen die heersen in vroege magma-oceanen
Onderzoekers simuleren processen die heersen in vroege magma-oceanen Klimaat in het verleden een betere voorspeller van koolstof in de bodem dan het huidige klimaat
Klimaat in het verleden een betere voorspeller van koolstof in de bodem dan het huidige klimaat Wat het klimaatsysteem van de aarde en topologische isolatoren gemeen hebben?
Wat het klimaatsysteem van de aarde en topologische isolatoren gemeen hebben?
Hoofdlijnen
- Een geheim wapen voor muggen:een lichte aanraking en sterke vleugels
- Harpoenkoppen, zwaaiende staarten:hoe roofzuchtige muggenlarven een prooi vangen
- Boomklimmende gekko's die smallere zitstokken gebruiken, hebben langere ledematen dan verwacht
- Paarden kunnen onze lichaamstaal lezen, zelfs als ze ons niet kennen
- Overeenkomsten van mitose en meiose
- Iraakse dierenliefhebbers gaan online om zwerfdieren in Bagdad te redden
- Archaea: Structure, Characteristics & Domain
- Neem een dosis Dickinson:poëzie als therapie
- Hoe werkt ureum denatureiwitten?
- Chemici verkrijgen nieuw materiaal voor antibacteriële voedselcoatings
- Screening op ziekte of toxines in een druppel bloed

- Chemici gebruiken licht om biologisch actieve verbindingen te bouwen

- Gefunctionaliseerde oppervlakken:cilindrische micellaire borstels met op maat gemaakte chemische opties met gecontroleerde lengte

- Wetenschappers ontdekken hoe oppervlakken het vroege leven op aarde hebben kunnen helpen beginnen

 Gericht op verborgen zak voor behandeling van beroerte en epileptische aanvallen
Gericht op verborgen zak voor behandeling van beroerte en epileptische aanvallen Pandemie, oorlog, klimaatverandering wakkert voedselangsten aan
Pandemie, oorlog, klimaatverandering wakkert voedselangsten aan Amazon zegt dat sommige e-mailadressen van klanten zijn vrijgegeven
Amazon zegt dat sommige e-mailadressen van klanten zijn vrijgegeven Toegankelijkheid mobiele telefoons verbetert, maar er blijven gaten studie vondsten
Toegankelijkheid mobiele telefoons verbetert, maar er blijven gaten studie vondsten Een supersnel proces voor machinale bewerking op nanoschaal
Een supersnel proces voor machinale bewerking op nanoschaal Wolken observeren in vier dimensies
Wolken observeren in vier dimensies Mysterie-object veroorzaakt door spontane symmetriebreking onthuld
Mysterie-object veroorzaakt door spontane symmetriebreking onthuld Alfabetten DeepMind beheerst Atari-spellen
Alfabetten DeepMind beheerst Atari-spellen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

