
Wetenschap
Verkennen hoe cellen sterk kunnen zijn op de juiste plaats en tijd
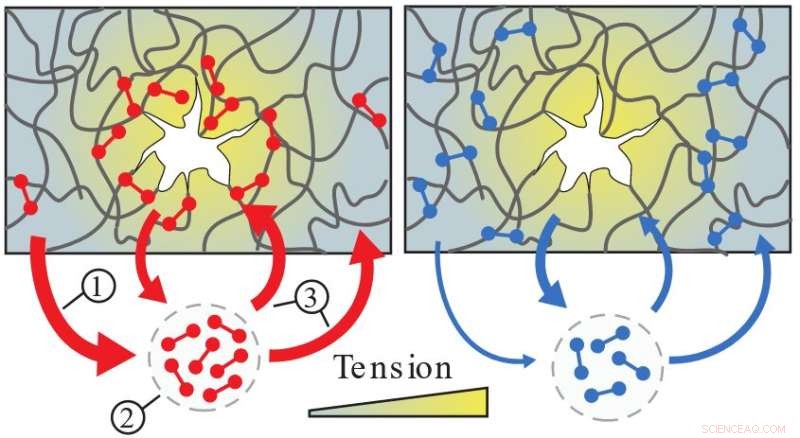
Vangbindingen (rood) zijn zwak in gebieden met lage spanning (1) en ontbinden daarom snel (2). Deze ongebonden verbindingen binden op willekeurige plaatsen in het netwerk opnieuw, maar binden alleen stevig vast in gebieden met hoge spanning (3), waardoor het netwerk wordt versterkt waar dit het meest nodig is. Normale bindingen (blauw) daarentegen blijven vastzitten in gebieden met lage spanning. Credit:de onderzoekers
Onderzoekers van de TU Delft en NWO-instituut AMOLF ontdekten hoe bepaalde moleculaire bindingen levende cellen zowel flexibel maken om te bewegen als sterk om krachten te weerstaan. Paradoxaal genoeg blijkt dat deze krachtgevoelige vangbindingen meestal zwak en inactief zijn, maar naar specifieke plaatsen reizen waar en wanneer cellen beschadigd raken. Deze ontdekking is gepubliceerd in Nature Materials .
Moleculaire catch bond-eiwitten kunnen in veel verschillende weefsels worden gevonden, zowel binnen als tussen cellen. Deze bindingen vallen regelmatig uit elkaar, zoals de meeste biologische bindingen doen, maar ze hebben een eigenaardige eigenschap:als je hard aan een catch-bond trekt, begint deze eigenlijk strakker te binden. Onderzoekers ontdekten dat dit vermogen het materiaal versterkt op specifieke plaatsen waar de binding stress ervaart. De ontdekking is een doorbraak, 20 jaar na de eerste vondst van dergelijke obligaties. Dit is ook de eerste keer dat de onderzoekers getuige zijn geweest van samenwerking tussen vangstbanden in biologische materialen.
Zowel flexibel als sterk
Voormalig AMOLF-onderzoeker Yuval Mulla legt uit dat "we meestal op twee manieren definiëren hoe sterk iets is:een materiaal kan ofwel goed vervormen - heel ver uitrekken zonder te breken, zoals rubber - of het materiaal kan veel kracht dragen, bijvoorbeeld een baksteen; hoewel het sterk is, kan het maar een beetje uitrekken voordat het zal breken. Toen we de aard van vangbindingen bestudeerden, ontdekten we dat deze moleculaire bindingen in staat waren om beide te doen:flexibel en sterk zijn, ook al zijn hun moleculaire bindingen zwak. En dan we hebben overwogen:kunnen hechtingen verklaren waarom levende cellen de rekbaarheid van rubber combineren met de sterkte van een baksteen?"
Om deze ideeën te testen, hebben de onderzoekers de mechanische eigenschappen gemeten van cytoskeletnetwerken die ze in het laboratorium hebben gereconstrueerd, in samenwerking met de Biophysics-groep om aan enkele bindingen te trekken. Ze ontdekten dat veel van de bindingen gewoon rondzweven, kort binden om vervolgens weer los te laten. Toen de onderzoekers de netwerken echter vervormden, ontdekten ze dat veel bindingen naar bijzonder beschadigde plaatsen reizen om te binden. Mulla zegt dat "omdat de catch bonds zich ophopen op zwakke plekken waar en wanneer ze nodig zijn om het netwerk erg sterk te maken."
Relatie met ziekten
De studie omvatte een gemuteerde versie van hetzelfde eiwit, waarvan bekend is dat het voorkomt bij een genetische ziekte die leidt tot nierfalen. In tegenstelling tot een gewone vangst, ontdekten de onderzoekers dat deze gemuteerde versie altijd actief was. Deze verhoogde bindingssterkte maakt het moeilijk voor de mutant om zich te verplaatsen, maar maakt paradoxaal genoeg ook de netwerken zwakker omdat de bindingen zich niet ophopen waar nodig, zegt groepsleider Gijsje Koenderink:"Door het mutante eiwit beter te begrijpen, kunnen we in de toekomst kan ook het proces van nierfalen begrijpen. Daarnaast hopen we te begrijpen hoe catch-bonds een rol spelen in hoe invasief kankercellen zijn."
Materiaal perspectief op het leven
De onderzoeksgroep van hoogleraar Koenderink van de TU Delft is vooral geïnteresseerd in materiaaleigenschappen van levende materie. Een centraal thema in haar groep is dat levende cellen en weefsels dynamisch en flexibel moeten zijn, maar ook sterk:"Deze eigenschap is anders dan alle synthetische materialen die we kennen", zegt Koenderink. "Onze ambitie is om nieuwe ontwerpprincipes te leren van levende materialen om synthetische materialen te maken die tegelijkertijd flexibel en sterk kunnen zijn. Sterker nog, we werken momenteel samen met chemici en biofysici zoals Sander Tans van AMOLF om te proberen dergelijke synthetische vangstobligaties." + Verder verkennen
Lanthanide-lanthanidebindingen gebruiken om krachtigere permanente magneten te creëren
 Zijn moleculen rechtshandig of linkshandig? Eigenschappen van chirale moleculen op attoseconde niveau
Zijn moleculen rechtshandig of linkshandig? Eigenschappen van chirale moleculen op attoseconde niveau Onderzoekers ontwikkelen nieuwe, niet-gerichte screeningsmethode voor voedselveiligheid afkomstig van dieren
Onderzoekers ontwikkelen nieuwe, niet-gerichte screeningsmethode voor voedselveiligheid afkomstig van dieren Een goedkope, hoogwaardige multinaire intermetallische verbinding als actieve elektrokatalysator voor waterstofproductie
Een goedkope, hoogwaardige multinaire intermetallische verbinding als actieve elektrokatalysator voor waterstofproductie Op katoen gebaseerde hybride biobrandstofcel kan implanteerbare medische apparaten van stroom voorzien
Op katoen gebaseerde hybride biobrandstofcel kan implanteerbare medische apparaten van stroom voorzien Chemische biologen ontdekken oorzaak van zeldzame hersenaandoening
Chemische biologen ontdekken oorzaak van zeldzame hersenaandoening
Hoofdlijnen
- Coniferencommunicatie is complex en kan worden gewijzigd door luchtvervuiling
- Genoomsequencing onthult uitgebreide inteelt bij Scandinavische wolven
- Wat is een bijtmiddel in de microbiologie?
- Beschrijving van gen-splitsing als een DNA-techniek
- Wat is de functie van een eicel?
- Burgerwetenschap kan trends in de vlinderpopulatie voorspellen
- Onderzoek bevestigt het:we worden echt dommer
- Dengue Achilleshiel inzicht biedt hoop op betere vaccins
- Decoderen hoe bacteriën met elkaar praten
- Zeer stabiele waterelektrolysekatalysator voor de productie van waterstof en zuurstof

- Rood of geel? Een eenvoudige papieren test detecteert valse of ondermaatse antibiotica

- Wat is het witte spul op mijn paaschocolade, en kan ik het nog steeds eten?

- Quantum wapening:Quantum dots verbeteren de stabiliteit van perovskietkristallen die zonne-energie oogsten

- Kunstbloed maken voor transfusies
 Afzwakkende tropische storm Xavier waargenomen door NASA
Afzwakkende tropische storm Xavier waargenomen door NASA Kleine lichtgevende sondes geven onderzoekers een betere optie voor niet-invasieve beeldvorming van levend weefsel
Kleine lichtgevende sondes geven onderzoekers een betere optie voor niet-invasieve beeldvorming van levend weefsel Orkaan Ian verplettert Florida en laat miljoenen in het duister
Orkaan Ian verplettert Florida en laat miljoenen in het duister Onderzoekers onderzoeken hoe de levering van drones in de detailhandel logistieke netwerken kan veranderen
Onderzoekers onderzoeken hoe de levering van drones in de detailhandel logistieke netwerken kan veranderen Hoe de Ph of Water te berekenen met behulp van pKa
Hoe de Ph of Water te berekenen met behulp van pKa  Betaalbaar multiferroïsch materiaal
Betaalbaar multiferroïsch materiaal Analyse maakt de weg vrij voor gevoeligere kwantumsensoren
Analyse maakt de weg vrij voor gevoeligere kwantumsensoren Missie naar de zon zal ons beschermen tegen verwoestende zonnestormen en ons helpen dieper de ruimte in te reizen
Missie naar de zon zal ons beschermen tegen verwoestende zonnestormen en ons helpen dieper de ruimte in te reizen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

