Wetenschap
Het uithongeren van tuberculose van suikers kan een nieuwe manier zijn om het te bestrijden
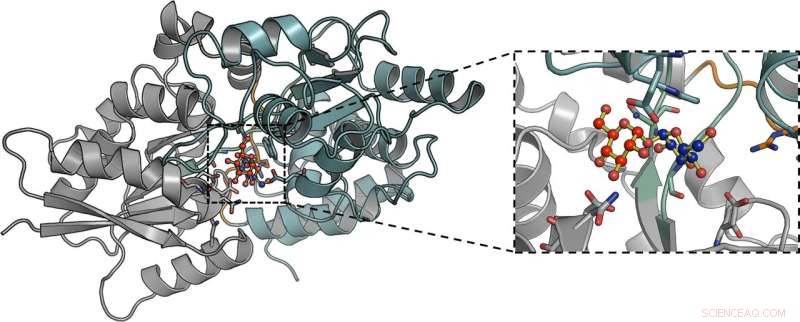
Detail op moleculair niveau van de interactie van trehalose gebonden aan de mycobacteriële LpqY-transporter. Krediet:Universiteit van Warwick
Tuberculose is een verwoestende ziekte die jaarlijks meer dan 1,5 miljoen levens kost. Door de toename van tbc-gevallen die resistent zijn tegen de huidige antibiotica, zijn er dringend nieuwe medicijnen nodig om Mycobacterium tuberculosis (Mtb) te doden. Onderzoekers van de Universiteit van Warwick hebben met succes ontdekt hoe Mycobacterium tuberculosis een essentiële suiker gebruikt die trehalose wordt genoemd, die een platform biedt voor het ontwerpen van nieuwe en verbeterde tbc-medicijnen en diagnostische middelen.
Tuberculose (tbc), veroorzaakt door de bacteriële ziekteverwekker Mycobacterium tuberculosis (Mtb) is de belangrijkste doodsoorzaak door een enkele infectieuze agens wereldwijd die jaarlijks meer dan 1,5 miljoen levens eist.
Mycobacterium tuberculosis (Mtb) is een zeer unieke ziekteverwekker en kan tientallen jaren in het menselijk lichaam overleven. Een manier waarop Mtb overleeft is door schaarse energiebronnen te 'eten' voor voeding, terwijl tegelijkertijd de menselijke gastheer probeert het beschikbare voedsel te beperken.
Echter, we hebben een beter begrip nodig van het intracellulaire dieet van Mtb, omdat het remmen van de routes die Mtb toegang geven tot essentiële voedselbronnen en deze gebruiken, een goed doelwit zou kunnen zijn voor de ontwikkeling van nieuwe antituberculosemiddelen.
Een energiebron die Mtb gebruikt, is een suiker die in zijn eigen celwand wordt gevonden, trehalose genoemd. Het lijkt erop dat Mtb een unieke strategie heeft ontwikkeld om deze suiker te recyclen en opnieuw te gebruiken om ervoor te zorgen dat er geen potentiële energiebronnen worden verspild, die schaars zijn.
Het transporteiwit, die verantwoordelijk is voor de opname van trehalose, genaamd LpqY, is essentieel voor Mtb om infectie vast te stellen. Als het LpqY-eiwit wordt verwijderd en niet meer kan functioneren, kan Mtb zichzelf niet meer van trehalose voorzien en wordt het minder pathogeen.
In de krant, "Structurele basis van trehalose-herkenning door de mycobacteriële LpqY-SugABC-transporter, " gepubliceerd in de Tijdschrift voor biologische chemie , onderzoekers van de School of Life Sciences aan de Universiteit van Warwick, hebben de moleculaire basis ontrafeld van hoe Mtb trehalose gebruikt en transporteert, een proces dat specifiek is voor Mtb en niet voorkomt bij mensen.
Het team gebruikte röntgenkristallografie om de driedimensionale structuur van LpqY te bepalen en analyseerde hoe dit belangrijke transporteiwit trehalose kan binden en herkennen. Vervolgens gebruikten ze een aantal experimentele technieken die aantoonden dat LpqY zeer specifiek is voor trehalose, kan ook suikers herkennen die vergelijkbaar zijn met trehalose met kleine aanpassingen en belangrijke herkenningsfuncties in kaart brengen.
Dr. Elizabeth Fullam, die een Sir Henry Dale Fellow is van de School of Life Sciences aan de Universiteit van Warwick, zei, "Het is van vitaal belang dat we nieuwe innovatieve strategieën vinden om tbc te bestrijden. De LpqY-trehalosetransporter is een potentieel doelwit voor geneesmiddelen, want als het niet functioneert, wordt Mtb minder virulent. Nu we precies begrijpen hoe trehalose wordt herkend, zullen we in staat zijn om specifieke moleculen te ontwerpen waarmee we tbc kunnen doden. een andere mogelijkheid is dat we de LpqY-transporter in ons voordeel kunnen gebruiken en manieren kunnen vinden om verbindingen te leveren voor de diagnose van tbc."
 Metaalinnovatie biedt een unieke, kosteneffectieve optie voor sanitair en productie-industrieën
Metaalinnovatie biedt een unieke, kosteneffectieve optie voor sanitair en productie-industrieën Roestige polymeren maken voor energieopslag
Roestige polymeren maken voor energieopslag Nieuwe vondst legers verlaagt onbedoelde ontploffing van voorraden
Nieuwe vondst legers verlaagt onbedoelde ontploffing van voorraden Nieuw type glas geïnspireerd door de natuur is beter bestand tegen schokken
Nieuw type glas geïnspireerd door de natuur is beter bestand tegen schokken De ecologische voetafdruk van een chemische stof in alledaagse voorwerpen verkleinen
De ecologische voetafdruk van een chemische stof in alledaagse voorwerpen verkleinen
Hoofdlijnen
- Soorten lijken bedrieglijk veerkrachtig tegen klimaatverandering
- Een eiwitduo zorgt ervoor dat de chromosomen in de voortplantingscellen hun significante andere vinden
- Stijgende CO2 zorgt ook voor overlast in zoetwater, studie suggereert:
- Wetenschappers stellen efficiëntieregels voor om het gebruik van nieuwe technologie voor het bewerken van genen te verbeteren
- Hoe maak je een 3D-plant eukaryotisch celmodel
- Verwarde walvis blokkeert de jachthaven van Marseille
- Wat is een markermolecuul?
- Video:studenten insectenbiologie leren kunst van op insecten gebaseerde kleurstoffen
- Microbeads zorgen ervoor dat ultrasone golven cellen veiliger kunnen stimuleren
 Boeing voltooit software-update voor geaard vliegtuig
Boeing voltooit software-update voor geaard vliegtuig Brachiopoden die bestand zijn tegen veranderingen in het milieu in het verleden
Brachiopoden die bestand zijn tegen veranderingen in het milieu in het verleden Hoe doping next-gen zonnecellen naar commercialisering stimuleert?
Hoe doping next-gen zonnecellen naar commercialisering stimuleert? Het pad naar onze evolutie
Het pad naar onze evolutie Communiceren dolfijnen echt met elkaar en met mensen?
Communiceren dolfijnen echt met elkaar en met mensen?  Hoe werkt een kas?
Hoe werkt een kas?  Klimaatverandering slaat hard toe in heel Nieuw-Zeeland, officieel rapport vindt
Klimaatverandering slaat hard toe in heel Nieuw-Zeeland, officieel rapport vindt Bepalen of een Caterpillar mannelijk of vrouwelijk is
Bepalen of een Caterpillar mannelijk of vrouwelijk is
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway | French |

-
Wetenschap © https://nl.scienceaq.com