
Wetenschap
Omzetting van CO2 naar CO op kamertemperatuur:een nieuwe manier om koolwaterstoffen te synthetiseren

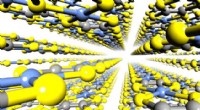
Illustratie van een nieuw proces bij kamertemperatuur om koolstofdioxide (CO .) te verwijderen 2 ) door het molecuul om te zetten in koolmonoxide (CO). In plaats van warmte te gebruiken, de methode op nanoschaal is gebaseerd op de energie van oppervlakteplasmonen (paarse tint) die worden geëxciteerd wanneer een elektronenstraal (verticale straal) aluminium nanodeeltjes raakt die op grafiet rusten, een kristallijne vorm van koolstof. In aanwezigheid van het grafiet, geholpen door de energie afkomstig van de plasmonen, kooldioxidemoleculen (zwarte stip gebonden aan twee rode stippen) worden omgezet in koolmonoxide (zwarte stip gebonden aan één rode stip. Het gat onder de violette bol stelt het grafiet voor dat weggeëtst is tijdens de chemische reactie CO 2 + C =2CO. Krediet:NIST
Onderzoekers van het National Institute of Standards and Technology (NIST) en hun collega's hebben een methode bij kamertemperatuur gedemonstreerd die de kooldioxidegehaltes in de uitlaatgassen van fossiele brandstoffen aanzienlijk zou kunnen verlagen. een van de belangrijkste bronnen van koolstofemissies in de atmosfeer.
Hoewel de onderzoekers deze methode op kleine schaal demonstreerden, sterk gecontroleerde omgeving met afmetingen van slechts nanometers, ze hebben al concepten bedacht om de methode op te schalen en praktisch te maken voor toepassingen in de echte wereld.
Naast het bieden van een potentiële nieuwe manier om de effecten van klimaatverandering te verzachten, het chemische proces dat door de wetenschappers wordt gebruikt, zou ook de kosten en energievereisten voor de productie van vloeibare koolwaterstoffen en andere chemicaliën die door de industrie worden gebruikt, kunnen verminderen. Dat komt omdat de bijproducten van de methode de bouwstenen bevatten voor het synthetiseren van methaan, ethanol en andere op koolstof gebaseerde verbindingen die bij industriële verwerking worden gebruikt.
Het team gebruikte een nieuwe energiebron uit de nanowereld om een alledaagse chemische reactie op gang te brengen die koolstofdioxide elimineert. Bij deze reactie vaste koolstof hecht zich aan een van de zuurstofatomen in kooldioxidegas, reduceren tot koolmonoxide. De conversie vereist normaal gesproken aanzienlijke hoeveelheden energie in de vorm van hoge temperaturen - een temperatuur van ten minste 700 graden Celsius, heet genoeg om aluminium te smelten bij normale atmosferische druk.
In plaats van warmte, het team vertrouwde op de energie die werd geoogst uit reizende elektronengolven, bekend als gelokaliseerde oppervlakteplasmonen (LSP's), die op individuele aluminium nanodeeltjes surfen. Het team activeerde de LSP-oscillaties door de nanodeeltjes te prikkelen met een elektronenstraal met een instelbare diameter. Een smalle straal, ongeveer een nanometer in diameter, bombardeerde individuele aluminium nanodeeltjes terwijl een straal van ongeveer duizend keer breder LSP's genereerde tussen een groot aantal nanodeeltjes.
In het experiment van het team, de aluminium nanodeeltjes werden afgezet op een laag grafiet, een vorm van koolstof. Hierdoor konden de nanodeeltjes de LSP-energie overbrengen naar het grafiet. In aanwezigheid van kooldioxidegas, die het team in het systeem heeft geïnjecteerd, het grafiet diende de rol van het plukken van individuele zuurstofatomen uit kooldioxide, reduceren tot koolmonoxide. De aluminium nanodeeltjes werden op kamertemperatuur bewaard. Op deze manier, het team heeft een grote prestatie geleverd:het verwijderen van de kooldioxide zonder de noodzaak van een bron van hoge hitte.
Eerdere methoden voor het verwijderen van kooldioxide hebben beperkt succes gehad omdat de technieken hoge temperatuur of druk vereisten, gebruikte kostbare edele metalen, of had een slechte efficiëntie. In tegenstelling tot, de LSP-methode bespaart niet alleen energie, maar maakt gebruik van aluminium, een goedkoop en overvloedig metaal.
Hoewel de LSP-reactie een giftig gas genereert - koolmonoxide - combineert het gas gemakkelijk met waterstof om essentiële koolwaterstofverbindingen te produceren, zoals methaan en ethanol, die vaak worden gebruikt in de industrie, zei NIST-onderzoeker Renu Sharma.
Zij en haar collega's, waaronder wetenschappers van de Universiteit van Maryland in College Park en DENSsolutions, te Delft, Nederland, rapporteerden hun bevindingen in Natuur materialen.
"We hebben voor het eerst aangetoond dat deze koolstofdioxidereactie, die anders alleen bij 700 graden C of hoger zal gebeuren, kan worden geactiveerd met behulp van LSP's bij kamertemperatuur, " zei onderzoeker Canhui Wang van NIST en de Universiteit van Maryland.
De onderzoekers kozen voor een elektronenstraal om de LSP's te exciteren, omdat de straal ook kan worden gebruikt om structuren in het systeem in beeld te brengen van slechts enkele miljardsten van een meter. Hierdoor kon het team inschatten hoeveel koolstofdioxide was verwijderd. Ze bestudeerden het systeem met behulp van een transmissie-elektronenmicroscoop (TEM).
Omdat zowel de concentratie kooldioxide als het reactievolume van het experiment zo klein waren, het team moest speciale maatregelen nemen om de hoeveelheid geproduceerde koolmonoxide direct te meten. Dat deden ze door een speciaal aangepaste gascelhouder van de TEM te koppelen aan een gaschromatograaf massaspectrometer, waardoor het team deeltjes-per-miljoen concentraties koolstofdioxide kan meten.
Sharma en haar collega's gebruikten ook de beelden die door de elektronenstraal werden geproduceerd om de hoeveelheid grafiet te meten die tijdens het experiment werd weggeëtst. een proxy voor hoeveel koolstofdioxide was weggenomen. Ze ontdekten dat de verhouding van koolmonoxide tot kooldioxide gemeten aan de uitlaat van de gascelhouder lineair toenam met de hoeveelheid koolstof die door etsen werd verwijderd.
Beeldvorming met de elektronenstraal bevestigde ook dat het grootste deel van het koolstofetsen - een proxy voor koolstofdioxidereductie - plaatsvond in de buurt van de aluminium nanodeeltjes. Aanvullende studies toonden aan dat wanneer de aluminium nanodeeltjes afwezig waren in het experiment, slechts ongeveer een zevende zoveel koolstof werd geëtst.
Beperkt door de grootte van de elektronenstraal, het experimentele systeem van het team was klein, slechts ongeveer 15 tot 20 nanometer in doorsnee (de grootte van een klein virus).
Om het systeem op te schalen zodat het kooldioxide uit de uitlaat van een commerciële elektriciteitscentrale kan verwijderen, een lichtstraal kan een betere keuze zijn dan een elektronenstraal om de LSP's te exciteren, zei Wang. Sharma stelt voor om een transparante behuizing met los verpakte koolstof- en aluminiumnanodeeltjes over de schoorsteen van een elektriciteitscentrale te plaatsen. Een reeks lichtstralen die op het raster vallen, zou de LSP's activeren. Wanneer de uitlaat door het apparaat gaat, de door licht geactiveerde LSP's in de nanodeeltjes zouden de energie leveren om koolstofdioxide te verwijderen.
De aluminium nanodeeltjes, die in de handel verkrijgbaar zijn, moet gelijkmatig worden verdeeld om het contact met de koolstofbron en het binnenkomende koolstofdioxide te maximaliseren, merkte het team op.
Het nieuwe werk suggereert ook dat LSP's een manier bieden voor een hele reeks andere chemische reacties die nu een grote infusie van energie vereisen om door te gaan bij gewone temperaturen en drukken met behulp van plasmonische nanodeeltjes.
"Het verminderen van kooldioxide is een groot probleem, maar het zou een nog grotere deal zijn, enorme hoeveelheden energie besparen, als we veel chemische reacties bij kamertemperatuur kunnen beginnen die nu moeten worden verwarmd, ' zei Sharma.
 Erosiesnelheden bepalen via schilderen
Erosiesnelheden bepalen via schilderen Verspillende gebouwen van staal en glas voeden wereldwijd klimaatonrecht, zegt klimaatexpert
Verspillende gebouwen van staal en glas voeden wereldwijd klimaatonrecht, zegt klimaatexpert Michigan spant zich in om chemische verontreinigingen in water aan te pakken
Michigan spant zich in om chemische verontreinigingen in water aan te pakken De redenen achter aerosolvervuiling boven de oostelijke helling van het Tibetaanse plateau
De redenen achter aerosolvervuiling boven de oostelijke helling van het Tibetaanse plateau Namen van planten die in graslanden leven
Namen van planten die in graslanden leven
Hoofdlijnen
- Celstructuren en hun drie belangrijkste functies
- Australische hagedissen eisen tol van schildpadeieren
- Hoe MRNA naar TRNA te vertalen
- De beste manieren om bacteriën te kweken op agar
- Leven gelukkige mensen langer?
- Minimale zuurstofconcentratie voor menselijke ademhaling
- Wat is de fysieke expressie van een allel?
- Hoeveel weegt het leven?
- Welke soorten cellen zijn bacteriën?
- Wetenschappers vinden moleculaire vernietigingscode voor enzym dat betrokken is bij cholesterolproductie

- Elektronische vaste stof kan de CO2-uitstoot in koelkasten en airconditioners verminderen

- Wat is het verschil tussen elektronische geometrie en moleculaire vorm?

- Potentieel van polymeervermogen
- Echografie kan sterkere 3D-geprinte legeringen maken

 Onderwaterkwekerijen helpen de mediterrane visbestanden nieuw leven in te blazen
Onderwaterkwekerijen helpen de mediterrane visbestanden nieuw leven in te blazen Planetair pact:China en Rusland lanceren ruimtestation op de maan
Planetair pact:China en Rusland lanceren ruimtestation op de maan Voorspellers:orkaanseizoen wordt drukker dan eerst gedacht
Voorspellers:orkaanseizoen wordt drukker dan eerst gedacht Biodistributie van koolstofnanobuisjes in het lichaam
Biodistributie van koolstofnanobuisjes in het lichaam Legeringssamenstellingen kunnen de elektronische toestanden van deeltjes beïnvloeden
Legeringssamenstellingen kunnen de elektronische toestanden van deeltjes beïnvloeden Waarom veel conservatieven een moeilijke relatie hebben met de wetenschap
Waarom veel conservatieven een moeilijke relatie hebben met de wetenschap Nieuwe studie suggereert dat raadselachtige hominoïde niet rechtop liep en geen boomklimmer was
Nieuwe studie suggereert dat raadselachtige hominoïde niet rechtop liep en geen boomklimmer was Boeing-vliegtuig glijdt in rivier Florida bij noodlanding geen dodelijke slachtoffers
Boeing-vliegtuig glijdt in rivier Florida bij noodlanding geen dodelijke slachtoffers
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Spanish | Portuguese | Italian | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

