
Wetenschap
Kankercellen van patiënten groeien betrouwbaar op nieuwe 3D-steiger, veelbelovend voor precisiegeneeskunde
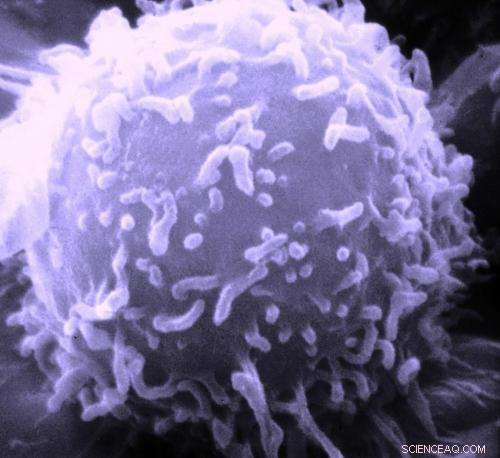
Elektronenmicroscopisch beeld van een enkele menselijke lymfocyt. Krediet:Dr. Triche National Cancer Institute
Een nieuwe 3D-structuur voor het kweken van celculturen zou artsen in staat kunnen stellen medicijnen te testen op modeltumoren die uit de eigen cellen van een patiënt zijn gegroeid. volgens resultaten van een team van ingenieurs en kankeronderzoekers aan de Universiteit van Michigan.
In tegenstelling tot eerdere apparaten, de nieuwe structuur is gemaakt van eiwitvezels die cellen weten te wijzigen.
"We kunnen de culturen mogelijk gebruiken om dingen te doen zoals het testen van medicijnen of eencellige analyse, die ons kunnen helpen bij het identificeren van de beste behandelingen voor de kanker van een patiënt, " zei Gary Luker, U-M hoogleraar radiologie.
Momenteel, sommige patiënten hebben monsters van hun kankercellen die in muizen zijn gekweekt voor het testen en analyseren van geneesmiddelen, maar de kankercellen groeien niet altijd en het proces duurt maanden, zei Luker.
Een geavanceerde petrischaal, bekend als een 3D-steiger, zou artsen in staat kunnen stellen om binnen dagen of weken antwoorden te krijgen over de effectiviteit van medicijnen. Maar eerdere steigers, proberen de structuur en samenstelling na te bootsen van het gelachtige netwerk dat een verzameling cellen in een weefsel bindt, hebben ook gemengde records.
"In plaats van te proberen te raden wat de micro-omgeving van de tumorcellen zou moeten zijn, we hebben een ruimte gemaakt waar ze hun eigen celniche kunnen creëren, zoals ze in het lichaam doen, " zei Stacy Jordahl, een recente chemische technologie Ph.D. afgestudeerd aan U-M en eerste auteur op het papier in Geavanceerde materialen .
Het team creëerde een netwerk van fibronectine, een eiwit dat cellen hecht aan de bindgel. Cellen in weefsels strekken het fibronectine uit, het een beetje gebruiken als de twee-bij-vieren van een huisframe. Echter, fibronectine heeft de neiging op te rollen als het niet open wordt gehouden. Terwijl onderzoekers lagen van opgerold fibronectine hebben gebruikt om cellen te helpen hechten aan eerdere steigers, het eiwit is niet ten volle benut.
Eerder, het was moeizaam om fibronectinestrengen uit te rekken - eraan trekken met pipetten, bijvoorbeeld, maar de nieuwe methode die door het UM-team is ontdekt, produceert een coating van uitgerekte fibronectine zonder het harde werk.
Onder leiding van Jörg Lahann, de Wolfgang Pauli Collegiate Professor of Chemical Engineering en directeur van het Biointerfaces Institute aan de U-M, de ingenieurs bouwden een raster van hokjes op microschaal, elk een halve millimeter opzij. Vervolgens, ze goten herhaaldelijk een oplossing met fibronectine over dat oppervlak met behulp van een buis die langzaam over het uiteinde heen draaide. Het trekken van de bewegende vloeistof was voldoende om het fibronectine naar buiten te trekken in netwerken van vezels die door de hele structuur verweven waren.
"Met deze gemanipuleerde manier om eiwitten in een netwerk van vezels te trekken, we kunnen een meer natuurlijke omgeving creëren voor het kweken van kankercelculturen die ons in staat stellen medicijnen te testen of kankerbiologie te begrijpen, ' zei Lahan.
Het team van Lahann droeg de structuren over aan twee kankeronderzoekers, Luker en Max Wicha, de Madeline en Sidney Forbes hoogleraar oncologie. Ze gebruikten de structuren om cellen te kweken die waren verwijderd van borstkankerpatiënten door vochtzakken af te tappen die zich in de buik en borst kunnen ophopen naarmate de ziekte vordert.
Hoewel kankercellen slechts ongeveer 5% van de cellen in deze vloeistoffen uitmaken, ze domineerden de celpopulatie na een paar dagen tot een week op het fibronectinenetwerk. En de kankeronderzoekers waren onder de indruk.
"Er zijn veel technologieën en benaderingen bedacht om te proberen kankercellen in cultuur te laten groeien die niet zo goed hebben gewerkt. De meeste kankercellen sterven uit wanneer ze in kunstmatige omstandigheden worden gekweekt, " zei Luker. "In dit systeem, we zouden de culturen in ieder geval voor korte tijd vrij constant kunnen laten groeien."
In aanvulling, de cellen leken te veranderen terwijl ze groeiden op het fibronectinenetwerk, steeds meer gaan lijken op het soort cellen waarvan wordt aangenomen dat ze kanker verspreiden naar andere delen van het lichaam. Dit kan een voordeel zijn voor het testen van kankermedicijnen, omdat die cellen het meest noodzakelijk zijn om te doden.
Echter, deze vooringenomenheid zou een belemmering vormen voor experimenten die de biologie van kanker onderzoeken, bijvoorbeeld het identificeren van de invloeden die ertoe leiden dat cellen agressiever of goedaardiger worden. In de toekomst, het team kan onderzoeken of veranderingen in de manier waarop het fibronectinenetwerk is gestructureerd deze vooringenomenheid kunnen wegnemen.
De studie is gepubliceerd in het tijdschrift Geavanceerde materialen .
 Rapport dringt er bij Californië op aan actie te ondernemen om mariene ecosystemen te beschermen tegen microplastics
Rapport dringt er bij Californië op aan actie te ondernemen om mariene ecosystemen te beschermen tegen microplastics In het Caribisch gebied, kolonialisme en ongelijkheid betekenen dat orkanen harder toeslaan
In het Caribisch gebied, kolonialisme en ongelijkheid betekenen dat orkanen harder toeslaan Onderzoek suggereert dat vlees- en zuivelindustrie op schema ligt om oliemaatschappijen te overtreffen als grootste uitstoters van broeikasgassen
Onderzoek suggereert dat vlees- en zuivelindustrie op schema ligt om oliemaatschappijen te overtreffen als grootste uitstoters van broeikasgassen Nieuw geïdentificeerde atmosferische circulatie versterkt hittegolven en bosbranden rond het noordpoolgebied
Nieuw geïdentificeerde atmosferische circulatie versterkt hittegolven en bosbranden rond het noordpoolgebied Video:Hoe verifiëren we klimaatverdragen?
Video:Hoe verifiëren we klimaatverdragen?
Hoofdlijnen
- De verpakking van DNA in chromosomen
- Theory of Evolution: Definition, Charles Darwin, Evidence & Voorbeelden
- Soorten redeneren in geometrie
- DNA-onderzoek in de Stille Oceaan onthult een toename van 2000 procent in onze kennis van de biodiversiteit van weekdieren
- Darmbacteriën veroorzaken indirect symptomen door het microbioom van fruitvliegen te veranderen
- Een epigenetische sleutel om gedragsverandering te ontgrendelen
- Hoe de gecorrigeerde WBC-telling te berekenen
- Soorten in het noorden zijn kwetsbaarder voor klimaatverandering
- Type energie geproduceerd door fotosynthese
- Onderzoekers kunnen gevaarlijke chemicaliën uit fastfoodverpakkingen in het lichaam volgen

- Het creëren van lithium-ionbatterijen met een hogere energiedichtheid voor toepassingen op het gebied van hernieuwbare energie

- Kenmerken van waterstofbinding
- Wanneer hiv-medicijnen niet meewerken
- Ammoniakvorming bij lagere temperaturen katalyseren met ruthenium

 Afbeelding:Lake George, Oeganda
Afbeelding:Lake George, Oeganda NASA onderzoekt gebruik van baanbrekend materiaal voor nieuwe sensoren
NASA onderzoekt gebruik van baanbrekend materiaal voor nieuwe sensoren Vorming van gefunctionaliseerde nanodraden door controle van zelfassemblage met behulp van meerdere gemodificeerde amyloïde peptiden
Vorming van gefunctionaliseerde nanodraden door controle van zelfassemblage met behulp van meerdere gemodificeerde amyloïde peptiden De Olympische Spelen van Tokyo kunnen bekend worden als de Robot Games
De Olympische Spelen van Tokyo kunnen bekend worden als de Robot Games AI-leertechniek kan de functie van beloningspaden in de hersenen illustreren
AI-leertechniek kan de functie van beloningspaden in de hersenen illustreren Waterstofenergie maken met het gewone nikkel
Waterstofenergie maken met het gewone nikkel Astronomen ontdekken bij toeval metaalarme bolvormige sterrenhoop
Astronomen ontdekken bij toeval metaalarme bolvormige sterrenhoop Wanneer natuurkunde financiële netwerken ontmoet
Wanneer natuurkunde financiële netwerken ontmoet
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

