
Wetenschap
In het laboratorium gemaakte eiwit chomps co-factor als een grote ol gator
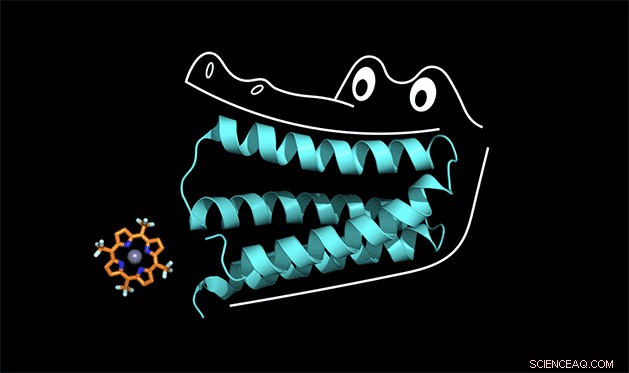
Het synthetische eiwit klemt zich vast aan de porfyrine als de kaken van een alligator. Krediet:Nicholas Polizzi
Eiwitten hebben de kracht om biochemische reacties in het lichaam te stimuleren.
Zonder de hulp van soorten eiwitten die enzymen worden genoemd, de reactie die DNA opbouwt kan meer dan 130 vergen, 000 jaar te voltooien. Enzymen verkorten die tijd tot slechts enkele milliseconden.
Om chemische reacties op gang te brengen, veel eiwitten werken samen met kleinere moleculen of metalen die cofactoren worden genoemd. Chemici willen eiwitten ontwerpen die binden aan niet-biologische cofactoren om chemische reacties te versnellen die in de natuur niet voorkomen. Maar eerst, ze moeten uitzoeken hoe ze door de mens gemaakte eiwitten kunnen maken die zich op precies de juiste manier aan nieuwe cofactoren hechten, en dat is geen gemakkelijke opgave.
Een team van chemici van Duke en UC San Francisco is de eerste die deze eiwitontwerppuzzel oplost. Het team creëerde een synthetisch eiwit dat een niet-biologische katalysator stevig bindt, een type molecuul genaamd porfyrine dat in staat is elektronen van andere moleculen te stelen wanneer het licht absorbeert.
"Als je door de mens gemaakte katalysatoren met eiwitten zou kunnen combineren, zou dat heel groot zijn in de chemie, want dan zou je de kracht van een enzym kunnen combineren met die van een reactie die niet in de natuur voorkomt, " zei voormalig Duke-afgestudeerde student Nicholas Polizzi, die nu een postdoctoraal onderzoeker is in het laboratorium van William DeGrado aan de UCSF.
"We waren in staat om de ontwerpcriteria te achterhalen die nodig zijn om dat porfyrine in een eiwit te plaatsen met een zeer hoge nauwkeurigheid, "Zei Polizzi. "Dat was echt een grote opstap om nieuwe eiwit-cofactorcombinaties te kunnen ontwerpen die niet in de natuur voorkomen."
Eiwitten zijn gemaakt van ketens van honderden of duizenden kleinere aminozuren die draaien en lussen in complexe 3D-vormen die in elkaar kunnen grijpen met andere moleculen, zoals stukjes van een legpuzzel. Om chemische reacties te katalyseren, eiwit-cofactorcombinaties houden twee of meer moleculen vast in precies gevormde holtes die de moleculen op precies de juiste posities houden, en zorgen voor de juiste omgeving, om een chemische reactie te laten plaatsvinden.
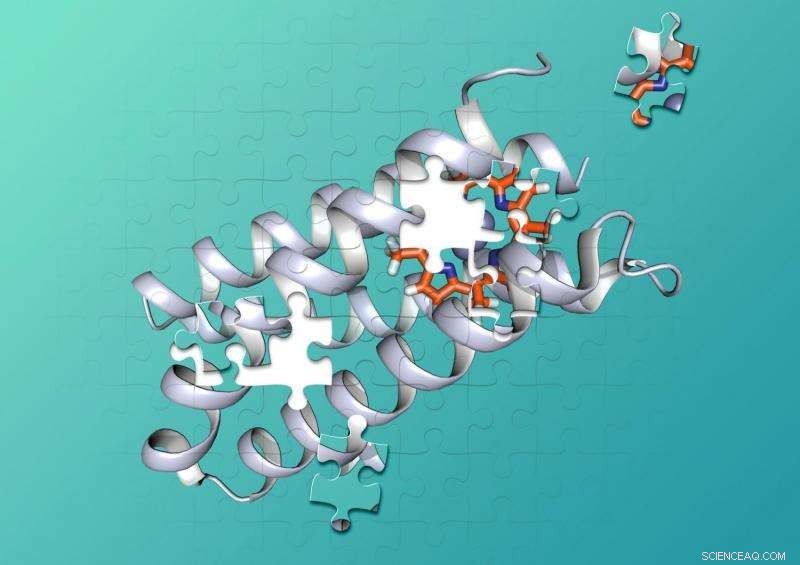
Chemici van Duke en UCSF ontwierpen een synthetisch eiwit dat een niet-biologisch molecuul stevig bindt. Krediet:Nicholas Polizzi
Miljoenen jaren van evolutie hebben eiwitten gecreëerd die zich in de vormen vouwen die specifieke cofactoren stevig vastgrijpen en de perfecte omgeving bieden om chemische reacties te katalyseren.
Al meer dan 25 jaar, scheikundigen hebben wat ze weten over eiwitvouwing gebruikt om synthetische aminozuursequenties te ontwerpen die zich in bruikbare vormen verdraaien. Maar tot nu toe, ze zijn er niet in geslaagd een eiwit te ontwerpen dat een niet-biologische cofactor bindt met de precisie die nodig is om complexe nieuwe chemische reacties aan te sturen.
Polizzi zei dat dit kan zijn omdat deze ontwerpen zich voornamelijk richtten op de "bindingsplaats" waar cofactoren en reagerende moleculen in het eiwit passen, terwijl de rest van de structuur wordt genegeerd. "Wat ik anders deed, is dat ik in wezen het hele inwendige van eiwit beschouwde als de bindingsplaats voor het porfyrine, in tegenstelling tot slechts een paar aminozuren die de porfyrine raken, ' zei Polizzi.
Om te begrijpen hoe dit werkt, je kunt het eiwit zien als de mond van een alligator, zei Michael Therien, William R. Kenan Jr. Professor in de chemie aan Duke. Het eiwit klampt zich vast aan een cofactor op dezelfde manier als een alligator zijn voortanden gebruikt om tijdens het avondeten te kauwen. Maar om de voortanden een stevige grip te geven, de kaak en de achterste tanden moeten ook correct zijn ontworpen.
"Het nieuwe concept hier is dat het niet-bindende gebied van het eiwit in een vorm wordt gehouden waardoor het bindende gebied kan werken, ' zei Therien.
"We noemden het eiwit 'gator' in het lab, ' zei Polizzi.
De kaken van het gator-eiwit klemmen de porfyrine-cofactor zo hard vast dat de hele structuur te rigide is om een reactie te katalyseren. zei Polizzi. Maar met een paar aanpassingen om de structuur losser te maken, hij denkt dat hij het kan laten werken.
"Bij deze reactie vaak heb je een beetje bewegingsruimte in het eiwit nodig om te bewegen. En er was geen speelruimte in ons eiwit, alles past te perfect, ' zei Polizzi.
 Ontwerpaanpak ontwikkeld voor nieuwe katalysatoren voor energieconversie en -opslag
Ontwerpaanpak ontwikkeld voor nieuwe katalysatoren voor energieconversie en -opslag Smelt ijs sneller in water of frisdrank?
Smelt ijs sneller in water of frisdrank?  Residuen in vingerafdrukken bevatten aanwijzingen voor hun leeftijd
Residuen in vingerafdrukken bevatten aanwijzingen voor hun leeftijd Nieuwe katalysatoren verwijderen BPA efficiënt en snel uit water
Nieuwe katalysatoren verwijderen BPA efficiënt en snel uit water Elektrolytboost verbetert de prestaties van waterige dual-ion-batterijen
Elektrolytboost verbetert de prestaties van waterige dual-ion-batterijen
 Kwantumfaseovergang gedetecteerd op wereldwijde schaal diep in de aarde
Kwantumfaseovergang gedetecteerd op wereldwijde schaal diep in de aarde Honderdduizenden vluchten Amerikaanse kust voor orkaan Laura
Honderdduizenden vluchten Amerikaanse kust voor orkaan Laura Kunnen computerspellen boeren helpen zich aan te passen aan klimaatverandering?
Kunnen computerspellen boeren helpen zich aan te passen aan klimaatverandering? Verboden pesticiden in Europese rivieren
Verboden pesticiden in Europese rivieren Mongoolse mijnbouwexplosie bedreigt traditionele hoeden
Mongoolse mijnbouwexplosie bedreigt traditionele hoeden
Hoofdlijnen
- Wat is het verschil tussen een bacteriële en virale infectie?
- Bloed afnemen met de push-pull-methode levert nauwkeurige resultaten op met minder porren
- Nieuwe vissoorten vertonen opvallend kleurverschil tussen mannetjes en vrouwtjes
- Wetenschappers vinden ontbrekende aanwijzing over hoe hiv cellen hackt om zichzelf te verspreiden
- Hoe lucide dromen werkt
- Wat zijn enkele kenmerken van DNA?
- Roept op tot einde aan Mexico's vangst van bedreigde bruinvis
- Wetenschappers onderzoeken de gevolgen voor de nationale veiligheid van genbewerking
- Bioreactoren op een chip vernieuwen beloften voor algenbiobrandstoffen
- Een nieuwe fluorescerende sonde die B-cellen van T-cellen kan onderscheiden

- Unieke organische lichtemitterende moleculaire emitters
- De vraag naar chemische zuurstof berekenen

- Een zwaargewicht oplossing voor lichtere gevechtsvoertuigen

- Reductie door reductie:nieuwe aanpak om chroomverontreiniging in afvalwater te verminderen
 Hoe negatief geladen water te maken
Hoe negatief geladen water te maken Onderzoekers geven radar nieuwe mogelijkheden met behulp van optische gegevens over meteoren
Onderzoekers geven radar nieuwe mogelijkheden met behulp van optische gegevens over meteoren Three Types of Buoyancy
Three Types of Buoyancy Exoplaneten hebben zowel continenten als oceanen nodig om complex leven te vormen
Exoplaneten hebben zowel continenten als oceanen nodig om complex leven te vormen De groei van nanodeeltjes belichten met röntgenstralen
De groei van nanodeeltjes belichten met röntgenstralen Hoogtevrees in de ruimte:NASA-astronaut details vlucht
Hoogtevrees in de ruimte:NASA-astronaut details vlucht Het gebruik van H-1B steeg enorm onder techreuzen in de Bay Area
Het gebruik van H-1B steeg enorm onder techreuzen in de Bay Area Multinationals treden op tegen plastic dat de oceanen verstopt
Multinationals treden op tegen plastic dat de oceanen verstopt
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

