
Wetenschap
Computermodellen bieden nieuw begrip van sikkelcelziekte
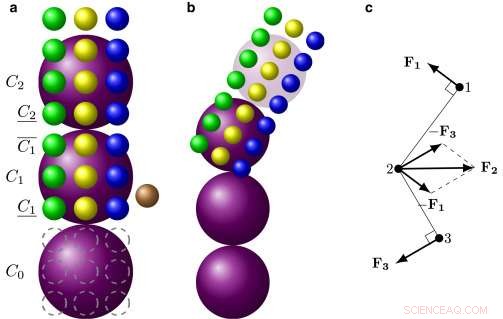
Een nieuwe modelleringstechniek stelt onderzoekers in staat om te zien wat er gebeurt in rode bloedcellen die zijn aangetast door sikkelcelziekte. Krediet:Karniadakis-lab / Brown University
Computermodellen ontwikkeld door wiskundigen van de Brown University laten nieuwe details zien van wat er gebeurt in een rode bloedcel die is aangetast door sikkelcelziekte. De onderzoekers zeiden dat ze hopen dat hun modellen, beschreven in een artikel in de Biofysisch tijdschrift , zal helpen bij het beoordelen van drugsstrategieën om de genetische bloedziekte te bestrijden, die wereldwijd miljoenen mensen treft.
Sikkelcelziekte tast hemoglobine aan, moleculen in rode bloedcellen die verantwoordelijk zijn voor het transport van zuurstof. In normale rode bloedcellen, hemoglobine wordt gelijkmatig door de cel verspreid. In sikkelrode bloedcellen, gemuteerd hemoglobine kan polymeriseren als het geen zuurstof krijgt, zich assembleren tot lange polymeervezels die tegen de membranen van de cellen duwen, waardoor ze uit vorm raken. de stijve, slecht gevormde cellen kunnen vast komen te zitten in kleine haarvaten door het hele lichaam, wat leidt tot pijnlijke episodes die bekend staan als sikkelcelcrisis.
"Het doel van ons werk is om zowel de vorming van deze sikkelhemoglobinevezels als de mechanische eigenschappen van die vezels te modelleren, " zei Lu Lu, een doctoraat student in de Brown Division of Applied Mathematics en de hoofdauteur van de studie. "Er waren afzonderlijke modellen voor elk van deze dingen die door ons afzonderlijk waren ontwikkeld, maar dit brengt die samen in één alomvattend model."
Het model maakt gebruik van gedetailleerde biomechanische gegevens over hoe sikkelhemoglobinemoleculen zich gedragen en met elkaar binden om de assemblage van een polymeervezel te simuleren. Voorafgaand aan dit werk, het probleem was geweest dat naarmate de vezel groeit, dat geldt ook voor de hoeveelheid gegevens die het model moet verwerken. Het modelleren van een volledige polymeervezel op cellulaire schaal met behulp van de details van elk molecuul was simpelweg te rekenkundig duur.
"Zelfs 's werelds snelste supercomputers zouden het niet aankunnen, " zei George Karniadakis, hoogleraar toegepaste wiskunde aan Brown en de senior auteur van de krant. "Er gebeurt gewoon te veel en het is onmogelijk om het allemaal rekenkundig vast te leggen. Dat is wat we met dit werk hebben kunnen overwinnen."
De oplossing van de onderzoekers was het toepassen van wat zij een mesoscopisch adaptief resolutieschema of MARS noemen. Het MARS-model berekent de gedetailleerde dynamiek van elk individueel hemoglobinemolecuul alleen aan elk uiteinde van polymeervezels, waar nieuwe moleculen in de vezel worden gerekruteerd. Zodra vier lagen van een vezel zijn vastgesteld, het model kiest automatisch de resolutie terug waarmee het die sectie vertegenwoordigt. Het model behoudt de belangrijke informatie over hoe de vezel zich mechanisch gedraagt, maar verdoezelt de fijne details van elk samenstellend molecuul.
"Door de fijne details te elimineren waar we ze niet nodig hebben, we ontwikkelen een model dat dit hele proces en de effecten ervan op een rode bloedcel kan simuleren, ' zei Karniadakis.
Met behulp van de nieuwe MARS-simulaties, de onderzoekers konden laten zien hoe verschillende configuraties van groeiende polymeervezels cellen met verschillende vormen kunnen produceren. Hoewel de ziekte zijn naam dankt omdat het ervoor zorgt dat veel rode bloedcellen een sikkelachtige vorm aannemen, er zijn eigenlijk verschillende abnormale celvormen aanwezig. Deze nieuwe modelleringsaanpak toonde nieuwe details over hoe verschillende vezelstructuren in de cel verschillende celvormen produceren.
"We zijn in staat om een polymerisatieprofiel te produceren voor elk van de celtypen die met de ziekte zijn geassocieerd, " zei Karniadakis. "Het doel is nu om deze modellen te gebruiken om manieren te zoeken om het begin van de ziekte te voorkomen."
Er is slechts één medicijn op de markt dat door de FDA is goedgekeurd voor de behandeling van sikkelcelziekte, zegt Karniadakis. dat medicijn, genaamd hydroxyureum, wordt verondersteld te werken door de hoeveelheid foetaal hemoglobine - het soort hemoglobine waarmee baby's worden geboren - in het bloed van een patiënt te verhogen. Foetaal hemoglobine is bestand tegen polymerisatie en, indien aanwezig in voldoende hoeveelheid, wordt verondersteld de polymerisatie van sikkelcelhemoglobine te verstoren.
Met behulp van deze nieuwe modellen, Karniadakis en zijn collega's kunnen nu simulaties uitvoeren met foetale hemoglobine. Die simulaties kunnen helpen bevestigen dat foetaal hemoglobine inderdaad de polymerisatie verstoort, evenals helpen om vast te stellen hoeveel foetaal hemoglobine nodig is. Dat zou kunnen helpen bij het opstellen van betere doseringsrichtlijnen of bij het ontwikkelen van nieuwe en effectievere medicijnen, zeggen de onderzoekers.
"De modellen geven ons een manier om voorlopige tests uit te voeren op nieuwe benaderingen om deze ziekte te stoppen, "Zei Karniadakis. "Nu we het hele polymerisatieproces kunnen simuleren, we denken dat de modellen veel nuttiger zullen zijn."
 Wetenschappers ontdekken mechanismen achter thermo-elektrisch materiaal
Wetenschappers ontdekken mechanismen achter thermo-elektrisch materiaal Welke soorten rotsen heb je nodig om een vuurtje te maken?
Welke soorten rotsen heb je nodig om een vuurtje te maken?  Video:Hond versus machine:wie is een betere bomdetector?
Video:Hond versus machine:wie is een betere bomdetector? Elektroforese proces
Elektroforese proces  Ultra-efficiënte verwijdering van koolmonoxide met behulp van gouden nanodeeltjes op een moleculaire drager
Ultra-efficiënte verwijdering van koolmonoxide met behulp van gouden nanodeeltjes op een moleculaire drager
 Wetenschappers stellen oplossing voor Gaia-puzzel voor
Wetenschappers stellen oplossing voor Gaia-puzzel voor Wetenschappers zeggen dat de kosten van het afvangen van CO2 afnemen
Wetenschappers zeggen dat de kosten van het afvangen van CO2 afnemen Hoe een enorm schip te recyclen – veilig en duurzaam
Hoe een enorm schip te recyclen – veilig en duurzaam Wat is de EPA, en waarom zit hij in de hot seat?
Wat is de EPA, en waarom zit hij in de hot seat? Onderzoekers documenteren de oudst bekende bomen in het oosten van Noord-Amerika
Onderzoekers documenteren de oudst bekende bomen in het oosten van Noord-Amerika
Hoofdlijnen
- Antiverouderingsbehandelingen - The Science of Living Longer
- Eiwit beperkt de opname van sap door bladluizen
- Onderzoekers beschrijven allereerste hybride vogelsoorten uit de Amazone
- Onderzoekers verkrijgen gegevens over de ontwikkeling van kippenembryo's
- Waarom is de trekduif uitgestorven?
- Deze pijnbomen leunen bijna altijd naar de evenaar
- Waarom zijn mensen altruïstisch?
- Soorten instrumenten die worden gebruikt voor het meten van lichaamstemperaturen
- Een door kracht aangedreven mechanisme voor het vaststellen van celpolariteit
- Video:Hoe pittige peperhitte te verslaan (hint:melk is niet de beste)

- Atomen plaatsen voor optimale katalysatoren
- Doorbraak in moleculaire machines

- Microscoop met elektroden wijst naar beter ontworpen apparaten die brandstof maken uit zonlicht

- Het creëren van lithium-ionbatterijen met een hogere energiedichtheid voor toepassingen op het gebied van hernieuwbare energie

 Mercurius:snel,
Mercurius:snel,  Een pagina uit de natuur om betere nanomaterialen te bouwen
Een pagina uit de natuur om betere nanomaterialen te bouwen Geschiedenis van Northwest Passages gekenmerkt door gevaren, dood
Geschiedenis van Northwest Passages gekenmerkt door gevaren, dood Fermilab-wetenschappers gaan op zoek naar donkere materie met behulp van kwantumtechnologie
Fermilab-wetenschappers gaan op zoek naar donkere materie met behulp van kwantumtechnologie Afbeelding:sectie van Hubble-zonnevleugel
Afbeelding:sectie van Hubble-zonnevleugel Wat beïnvloedt de slingeringsnelheid van een slinger?
Wat beïnvloedt de slingeringsnelheid van een slinger?  Afbeelding:Nevel aan de horizon van Saturnus
Afbeelding:Nevel aan de horizon van Saturnus Activiteiten op geleidbaarheid
Activiteiten op geleidbaarheid
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

