
Wetenschap
Travelling-wave ion mobility massaspectrometrie verheldert structuren van gouden vingers
Geneesmiddelen die goud bevatten, worden al eeuwenlang gebruikt om aandoeningen zoals reumatoïde artritis te behandelen. In aanvulling, ze kunnen effectief zijn tegen kanker en hiv. Eén mechanisme waarmee ze werken, kan optreden omdat goudionen de zinkionen uit zinkvingers dwingen - in een lus, nucleïnezuurbindende eiwitdomeinen. Amerikaanse onderzoekers hebben dergelijke "gouden vingers" gekarakteriseerd met behulp van massaspectrometrie met ionenmobiliteit. Zoals gerapporteerd in het journaal Angewandte Chemie , ze identificeerden de exacte goudbindingsplaatsen.
"De zinkionen in zinkvingers binden aan vier zwavel- of stikstofatomen van de cysteïne- en histidineresiduen van het eiwit, " legt Nicholas P. Farrell van Virginia Commonwealth University (Richmond, VS). "Goudionen binden aan slechts twee aminozuurfragmenten en veranderen de conformatie van het eiwit. De "gouden vingers" kunnen niet langer binden aan nucleïnezuren, die therapeutisch nuttig kunnen zijn."
Hoewel er verschillende potentiële bindingsplaatsen zijn voor metaalionen, elk metalloproteïne geeft meestal de voorkeur aan een enkele conformatie. Het was voorheen niet mogelijk om te bepalen waar de specifieke bindingsplaatsen waren in een mengsel van conformeren. Farrell en zijn team hebben nu twee gouden vingers nauwkeurig onderzocht. Volgens Farrell, "het vervangen van het zink in zinkvinger 3 van Sp1-transcriptiefactor leidt tot slechts één enkele gouden vingersoort." De onderzoekers identificeerden dit als een lineaire Cys-Au-His-binding. In het geval van het HIV-nucleocapside-eiwit, die een cruciale rol speelt bij de replicatie van het virus, "goud plaatsen in de zinkvinger 2 van het eiwit (NCp7-F2), leidt tot drie verschillende soorten gouden vingers met lineaire Cys-Au-Cys-motieven, waarvan er één duidelijk overheerst."
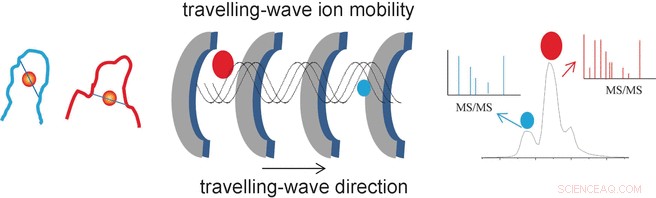
Het succes van de onderzoekers komt voort uit hun gebruik van een speciale analytische methode, de zogenaamde travelling-wave ion mobility mass spectrometry (TWIM-MS). Bij deze techniek, de te analyseren moleculen worden geïoniseerd en de ionen worden versneld door een elektrisch veld in een gas. Botsingen met de gasmoleculen zorgen ervoor dat de ionen worden afgeremd. Groot, volumineuze moleculen worden meer vertraagd dan kleine, compacte omdat ze vaker botsen. Dit maakt het mogelijk om ook isomeren te differentiëren en te scheiden, want hoewel ze dezelfde massa hebben, hun verschillende geometrieën resulteren in verschillende mobiliteit. Eenmaal gescheiden volgens hun mobiliteit, de individuele ionen kunnen nu worden gefragmenteerd door middel van botsingsgeïnduceerde dissociatie (CID) en de fragmenten kunnen opnieuw worden gemeten met massaspectrometrie. Dit maakt het mogelijk om kortere peptiden te karakteriseren die aan goud gebonden blijven.
"Op deze manier, we waren in staat om de specifieke bindingsplaatsen en modi voor de met goud gemodificeerde zinkvingers NCp7-F2 en Sp1-F3 te identificeren, ", zegt Farrell. "Ionenmobiliteitsmassaspectrometrie levert dus belangrijke informatie op over de veranderingen in de geometrie veroorzaakt door de uitwisseling van zink in de zinkvingereiwitten, evenals de selectiviteit en reactiviteit van dergelijke reacties. Dit zou van pas kunnen komen bij het zoeken naar nieuwe op metalen gebaseerde antivirale en antitumormiddelen."
 De vorm van water ontsluiten in mechanismen van antibioticaresistentie
De vorm van water ontsluiten in mechanismen van antibioticaresistentie Nieuw onderzoek maakt de weg vrij voor het simuleren van katalysatoren onder reactieomstandigheden
Nieuw onderzoek maakt de weg vrij voor het simuleren van katalysatoren onder reactieomstandigheden Visslijm:een onaangeboorde bron van potentiële nieuwe antibiotica
Visslijm:een onaangeboorde bron van potentiële nieuwe antibiotica Grote stap in de productie van CO2-neutrale brandstof:zilverdifosfide
Grote stap in de productie van CO2-neutrale brandstof:zilverdifosfide Gebruik voor een temperatuursensor
Gebruik voor een temperatuursensor
 Nieuw product voor biologische bestrijding van aflatoxine verlaagt besmetting van aardnoten en maïs in Senegal
Nieuw product voor biologische bestrijding van aflatoxine verlaagt besmetting van aardnoten en maïs in Senegal Klassen van Nematoden
Klassen van Nematoden  Ontbossing van Guyana Shield zal gevolgen hebben voor heel Zuid-Amerika, wetenschappers waarschuwen
Ontbossing van Guyana Shield zal gevolgen hebben voor heel Zuid-Amerika, wetenschappers waarschuwen 2017 wordt waarschijnlijk het derde warmste jaar ooit
2017 wordt waarschijnlijk het derde warmste jaar ooit Experiment met koffiefilters om te verklaren hoe een nier werkt
Experiment met koffiefilters om te verklaren hoe een nier werkt
Hoofdlijnen
- Wat is de schijfachtige structuur aan de zijde van chloroplasten?
- Is er een zaak tegen geluk?
- BigH1 - de belangrijkste histon voor mannelijke vruchtbaarheid
- Geheimen van vetplanten water-wijs manieren onthuld
- Waarom liegen mensen over dingen die gemakkelijk weerlegd kunnen worden?
- Daling van huismus in verband met luchtvervuiling en slechte voeding
- Stadia van meiose met een beschrijving
- Antibioticaresistente infecties bij huisdieren
- Buiktyfustoxine heeft een zoetekauw
- Moleculaire chirurgie hervormt levend weefsel met elektriciteit maar zonder incisies

- Onderzoekers pionieren met machine learning om chemische ontdekkingen te versnellen, afval verminderen

- Wetenschappers zorgen voor doorbraak vitamine B12

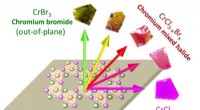
- Gemengde halogenidechemie kan worden gebruikt om magnetisme in ultradunne magnetische apparaten te beheersen
- Draagbare zoetwateroogstmachine kan tot 10 gallons per uur uit de lucht halen

 Amylase Activity in the Stomach
Amylase Activity in the Stomach  Waterstof bevordert het gebruik van grafeen
Waterstof bevordert het gebruik van grafeen Linnaean-classificatie: definitie, niveaus en voorbeelden (met grafiek)
Linnaean-classificatie: definitie, niveaus en voorbeelden (met grafiek)  Shampoo-ingrediënt kan diesel uit de grond wassen
Shampoo-ingrediënt kan diesel uit de grond wassen Onderzoekers onderzoeken manieren om antibiotica te verwijderen die meren en rivieren vervuilen
Onderzoekers onderzoeken manieren om antibiotica te verwijderen die meren en rivieren vervuilen Wat geeft een drie meter lange Amazone-vis enkele van de zwaarste schubben op aarde?
Wat geeft een drie meter lange Amazone-vis enkele van de zwaarste schubben op aarde? Unieke olie-etende bacteriën gevonden in diepste oceaangeul ter wereld
Unieke olie-etende bacteriën gevonden in diepste oceaangeul ter wereld Natuurkundigen ontdekken overeenkomsten tussen klassiek en kwantummachine learning
Natuurkundigen ontdekken overeenkomsten tussen klassiek en kwantummachine learning
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

