
Wetenschap
Ontdekking van kraakbeengenezing in diermodellen zou kunnen leiden tot nieuwe menselijke therapieën
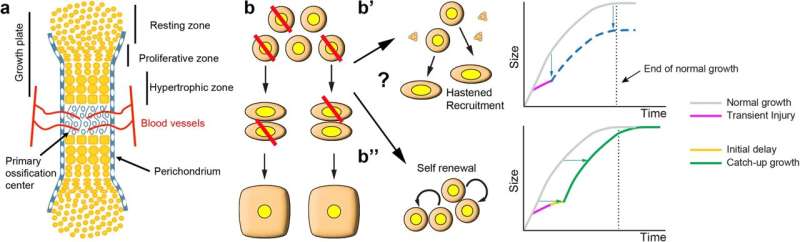
Onderzoekers hopen dat hun ontdekking over de genezende eigenschappen van foetale kraakbeencellen bij muizen de basis zal leggen voor nieuwe behandelingen voor menselijke groeistoornissen en degeneratieve ziekten.
Gepubliceerd in Natuurcommunicatie Uit het door Monash University geleide project bleek dat wanneer de kraakbeencellen van sommige foetale muizen afstierven, het kraakbeengebied binnen een week kon genezen. Het identificeerde ook een celcommunicatiesysteem dat de genezing vergemakkelijkte en een potentieel therapiedoel zou kunnen zijn.
Eerste auteur Dr. Chee Ho H'ng, een postdoctoraal onderzoeker aan het Australian Regenerative Medicine Institute van Monash University, legde uit dat het kraakbeen dat normaal gesproken de botgroei stimuleert en menselijke gewrichten bekleedt, een van de weefsels is met de slechtste herstelmogelijkheden van alle volwassen mensen. weefsel.
Hij zei dat onderzoekers met muizen hebben waargenomen dat kraakbeengebieden zich herstelden nadat sommige cellen waren afgestorven.
"We ontdekten dat het kraakbeen binnen een week geneest, waardoor de botgroei normaal kan hervatten," zei Dr. H'ng. "Dit wordt bereikt door eerst een verzameling cellen aan te vullen met het potentieel om de rest van het kraakbeen te regenereren, en vervolgens hun progressie naar de vorming van meer kraakbeen te versnellen.
"We hebben verder een cel-celcommunicatiesysteem gevonden dat nodig is voor deze gedragsverandering, waardoor een potentieel doelwit voor toekomstige therapieën wordt onthuld."
Senior auteur Dr. Alberto Rosello-Diez vergeleek de ontdekking met het omgaan met een lekkende brandstoftank. "Stel je voor dat je meedoet aan een rallyautorace en dat je brandstoftank wordt doorboord en een deel van de brandstof verliest", zei hij.
“Als je het gewoon opknapt en doorgaat met racen, zul je zonder brandstof komen te zitten voordat je het einde bereikt. Als je echter wat tijd besteedt aan het tanken uit een reservetank, kun je, wanneer je weer gaat racen, langer rijden en de achterstand inhalen. ."
Het is de eerste keer dat een genetisch model is gebruikt om voorbijgaande eenzijdige celdood in het kraakbeen van de ledematen te veroorzaken, waardoor potentiële herstelmechanismen aan het licht komen.
"Het biedt een cellulaire en moleculaire verklaring voor een klassiek fenomeen dat bekend staat als inhaalgroei:het herstel van een normaal groeitraject na een tijdelijke groeivertraging", aldus Dr. Rosello-Diez.
Dr. Rosello-Diez zei dat er meer onderzoek nodig is met behulp van menselijke kraakbeenorganoïden, en uiteindelijk ook proeven op mensen, maar dat de resultaten een model kunnen bieden voor therapieën die het herstel van kraakbeen bij menselijke groeischijfletsels kunnen helpen stimuleren.
Hij zei dat dit waarschijnlijk nog tien tot vijftien jaar zal duren, omdat ze gecombineerd moeten worden met cellulaire therapieën om groeistoornissen aan te pakken.
"Therapieën voor kraakbeenherstel zouden uiteindelijk kunnen leiden tot behandelingen voor groeistoornissen zoals dwerggroei en degeneratieve ziekten zoals artrose," zei hij.