
Wetenschap
Hoe dodelijke parasieten ervoor kiezen mannelijk te zijn:Onderzoekers onthullen genexpressie gedurende de levenscyclus van Cryptosporidium
Er zijn geen effectieve medicijnen of vaccins, waardoor dit een belangrijk organisme is om te bestuderen. De parasiet infecteert de cellen die de darmen bekleden en houdt zich bezig met zowel aseksuele als seksuele replicatie, waarvan onderzoekers vermoeden dat deze beide van cruciaal belang zijn voor aanhoudende infectie en overdracht.
Maar het mechanisme waardoor de parasiet mannelijk of vrouwelijk wordt, is onbekend. "Deze parasieten hebben geen geslachtschromosomen, zoals de menselijke X of Y", zegt Katelyn A. Walzer, een postdoctoraal onderzoeker in het Striepen Lab van Penn's School of Veterinary Medicine. "Het onthullen van hoe ze een geslacht kiezen is van fundamenteel biologisch belang en biedt een nieuw belangrijk doelwit om overdracht en infectie te blokkeren."
Walzer is de hoofdauteur van een onderzoek, gepubliceerd in Nature , dat het genexpressieprogramma van de gehele levenscyclus van Cryptosporidium onthult.
Met behulp van RNA-sequencing hebben de onderzoekers meer dan 9.000 parasieten geprofileerd (uit geïnfecteerde celculturen en muizen) en de Cryptosporidium eencellige atlas ontwikkeld, die onthult welke genen op welke punten in de levenscyclus tot expressie komen.
In een tweede belangrijke bevinding identificeerden onderzoekers de vroegste determinant van mannelijkheid, een gen genaamd Myb-M.
"We laten in dit en ander werk zien dat het seksuele deel van deze levenscyclus van cruciaal belang is voor infecties, en het blokkeren ervan door middel van anticonceptie tegen parasieten zal de infectie blokkeren", zegt senior auteur Boris Striepen. Hij zegt dat we, door seks te ontwrichten, "de ziekte kunnen genezen of de parasiet kunnen verzwakken om een vaccin te ontwikkelen, dus ik denk dat er een heel sterk translationeel potentieel is."
Dit bouwt voort op eerder onderzoek dat de levenscyclus heeft herzien naar een levenscyclus met slechts drie stadia – een enkele aseksuele vorm, mannen en vrouwen – terwijl de heersende literatuur een extra, tussenstadium voorstelde.
Walzer legt uit dat Cryptosporidium mensen infecteert, vaak via vervuild water, in een sporenachtige vorm, een oöcyst genaamd, die resistent is tegen waterchlorering. Eenmaal in de darm komen parasieten uit de sporen tevoorschijn om de epitheelcellen binnen te dringen die de darm bekleden en zich in die cellen te vermenigvuldigen voordat ze vertrekken en nieuwe darmcellen binnendringen.
Deze aseksuele cyclus van invasie, replicatie en uitgang vindt drie keer plaats voordat de parasieten differentiëren in mannelijke en vrouwelijke gameten, waarna bevruchting leidt tot nieuwe oöcysten.
Walzer zegt dat we door dit nieuwe onderzoek "een volledig begrip hebben van alle genen die betrokken zijn bij elk van deze processen, van invasie tot groei en deling tot het opnieuw vormen van de invasieve vorm."
Ze zegt dat deze atlas een gedetailleerde blauwdruk biedt van elk aspect van de biologie van de parasiet en zijn potentiële kwetsbaarheden. Cryptosporidium maakt veel eiwitten die nodig zijn om de gastheer binnen te dringen en te manipuleren, en het werk van het team ontleedt deze verschillende eiwitten op basis van de timing waarmee hun genen worden gelezen.
"De invasieve vormen van de parasiet worden geleverd met een batterij wapens waarmee ze onze cellen kunnen binnendringen en inhalen, en dit arsenaal is met opmerkelijke tijdsprecisie samengesteld", zegt Striepen. Hij vergelijkt het met de assemblagelijn van een autofabriek waar nieuwe componenten precies op tijd worden gemaakt, en Walzer heeft een lijst opgesteld met alle onderdelen en wanneer ze samenkomen.
Walzer zegt dat onderzoekers op dit gebied enthousiast zijn over de Cryptosporidium eencellige atlas omdat ze de context kunnen opzoeken waarin de genen die ze bestuderen tot expressie komen. Dit is zeer nuttige informatie voor mensen die op zoek zijn naar doelwitten voor medicijnen en vaccins, omdat het helpt bij het voorspellen van de infectiefasen waarin de parasiet het meest kwetsbaar kan zijn.
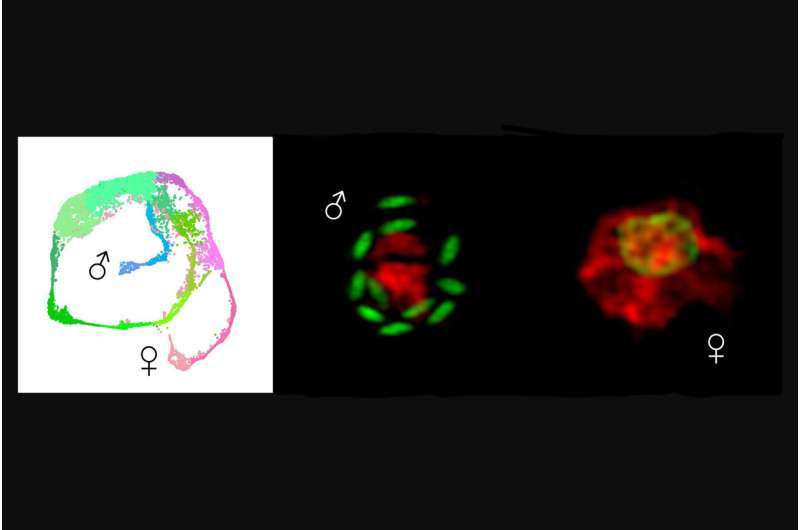
Door parasieten te ontwikkelen die fluorescentie tot expressie brengen, kwamen de onderzoekers ook tot hun tweede belangrijke bevinding:de ontdekking van de transcriptiefactor, dat wil zeggen een eiwit dat genexpressie reguleert en verantwoordelijk is voor mannelijkheid, Myb-M.
"Toen we de parasiet op enig moment dwongen deze factor te maken, werd elke parasiet mannelijk, en toen we deze weghaalden ontwikkelden zich geen mannetjes. Belangrijk is dat beide manipulaties de infectie blokkeerden", zegt Walzer.
Striepen zegt dat deze bevinding de waarde van parasietenseks als doelwit voor interventie onderstreept, en Walzer zegt dat deze studie ons ook "leidt naar het kennen van de volledige catalogus van genen die nodig zijn voor parasietenseks, en belangrijke aanwijzingen geeft voor mechanismen en translationele doelen." P>
Walzer zegt dat ze in toekomstig onderzoek geïnteresseerd is in het opvolgen van de manier waarop Myb-M het lot van mannen bepaalt en in het meer in het algemeen begrijpen hoe regulatie van transcriptie stadiumspecifieke verschillen aanstuurt om de complexe levenscyclus te orkestreren.