
Wetenschap
Onderzoekers breiden de kracht van genbewerking uit door een nieuwe klasse van DNA-basiseditors te ontwikkelen
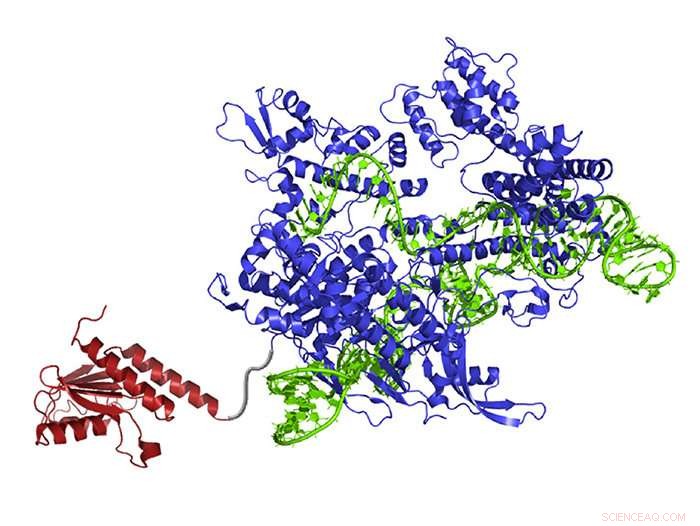
Een nieuw gecreëerde DNA-base-editor bevat een atoomherschikkend enzym (rood) dat adenine kan veranderen in inosine (lees en gekopieerd als guanine), gids RNA (groen) dat het molecuul naar de juiste plek leidt, en Cas9 nickase (blauw), die de tegenoverliggende DNA-streng knipt en de cel bedriegt om de complementaire base te verwisselen. Krediet:Gaudelli et al./ Natuur 2017
Wetenschappers van Harvard University en het Broad Institute of MIT en Harvard hebben een nieuwe klasse van genoombewerkingstools ontwikkeld. Deze nieuwe "basis-editor" kan het type enkelletterige veranderingen in het menselijk genoom, die verantwoordelijk zijn voor ongeveer de helft van de met menselijke ziekten geassocieerde puntmutaties, direct herstellen. Deze mutaties zijn geassocieerd met aandoeningen variërend van genetische blindheid tot sikkelcelanemie tot stofwisselingsstoornissen tot cystische fibrose.
Het onderzoeksteam, onder leiding van David Liu, hoogleraar scheikunde en chemische biologie aan de Harvard University, kerninstituutslid bij het Broad Institute, en een onderzoeker van het Howard Hughes Medical Institute (HHMI), een moleculaire machine ontwikkeld die het DNA-basenpaar A* T kan omzetten in G* C, zonder de dubbele helix te snijden, met een hoog rendement en vrijwel geen ongewenste producten. De ontwikkeling is een belangrijke aanvulling op de groeiende reeks genoombewerkingstools.
Het nieuwe systeem wordt beschreven in een artikel dat vandaag is gepubliceerd in Natuur . Naast Liu, de studie werd geleid door Nicole Gaudelli, een postdoctoraal onderzoeker in het lab van Liu; Alexis Komor, een voormalig postdoctoraal fellow in Liu's lab die nu een assistent-professor is bij UCSD; afgestudeerde studente Holly Rees; voormalige afgestudeerde studenten Michael Packer en Ahmed Badran, en voormalig postdoctoraal fellow David Bryson.
Het nieuwe systeem, genaamd Adenine Base Editor, of ABE, kan worden geprogrammeerd om zich te richten op een specifiek basenpaar in een genoom met behulp van een gids-RNA en een gemodificeerde vorm van CRISPR-Cas9. Het werkt door de atomen in een doel-adenine (A) - een van de vier basen waaruit DNA bestaat - te herschikken om in plaats daarvan op guanine (G) te lijken. en vervolgens de cellen te misleiden om de andere DNA-streng te fixeren om de basenpaarconversie te voltooien, de verandering blijvend maken. Als resultaat, wat vroeger een A* T-basenpaar was, wordt een G* C-basenpaar.
Het systeem is niet alleen zeer efficiënt in vergelijking met andere genome editing technieken voor het corrigeren van puntmutaties, maar er zijn vrijwel geen detecteerbare bijproducten zoals willekeurige inserties, schrappingen, translocaties, of andere basis-naar-basis conversies.
Het maken van deze specifieke verandering is belangrijk omdat ongeveer de helft van de 32, 000 ziektegerelateerde puntmutaties die al door onderzoekers zijn geïdentificeerd, zijn een verandering van G* C naar A* T.
"We hebben een nieuwe basiseditor ontwikkeld - een moleculaire machine - die in een programmeerbare, onomkeerbaar, efficiënt, en schone manier deze mutaties in het genoom van levende cellen kunnen corrigeren, " zei Liu, die ook de Richard Merkin-professor en directeur is van het Merkin Institute of Transformative Technologies in Healthcare at the Broad. "Wanneer gericht op bepaalde plaatsen in menselijk genomisch DNA, deze conversie keert de mutatie om die wordt geassocieerd met een bepaalde ziekte."
ABE voegt zich bij andere basisbewerkingssystemen die zijn ontwikkeld in Liu's lab, zoals BE3 en zijn verbeterde variant, BE4. Met behulp van deze basiseditors, onderzoekers kunnen nu alle zogenaamde "overgangs"-mutaties corrigeren - C naar T, T tot C, A tot G, of G tot A - die samen goed zijn voor bijna tweederde van alle ziekteveroorzakende puntmutaties, waaronder vele die ernstige ziekten veroorzaken waarvoor momenteel geen behandeling bestaat. Er is aanvullend onderzoek nodig, Liu merkt op, om ABE in staat te stellen zoveel mogelijk van het genoom te targeten, zoals Liu en zijn studenten eerder bereikten door technische varianten van BE3.
De ontwikkeling van de nieuwe basiseditor begon toen het team een jaar lang aan een inspanning begon om een nieuw enzym te ontwikkelen dat adenine kan omzetten in inosine (I), een nucleotide dat zich tijdens DNA- of RNA-synthese op dezelfde manier gedraagt als G. Het project, onder leiding van Gaudelli, heeft uiteindelijk geleid tot hoogwaardige, ABE's van de zevende generatie.
"De belangrijkste uitdaging voor mij tijdens het ontwikkelen van ABE was het overwinnen van de psychologische hindernis of ABE al dan niet van concept naar realiteit kon gaan, aangezien het belangrijkste onderdeel van de editor niet van nature bestond en in ons laboratorium moest worden ontwikkeld, " zei Gaudelli. "Het was belangrijk om het vertrouwen te behouden dat we niet alleen konden dromen van zo'n moleculaire machine, maar ook bouwen."
Om het potentieel van ABE te demonstreren, Liu en collega's gebruikten eerst ABE om direct een mutatie te corrigeren die erfelijke hemochromatose (HHC) in menselijke cellen veroorzaakt.
Ze gebruikten ABE ook om een mutatie in menselijke cellen aan te brengen die een ziekte onderdrukt, het opnieuw creëren van de zogenaamde "Britse mutatie" die wordt aangetroffen bij gezonde personen die normaal bloedziekten zoals sikkelcelanemie zouden ontwikkelen, maar in plaats daarvan een mutatie hebben die ervoor zorgt dat foetale hemoglobinegenen na de geboorte actief blijven, hen te beschermen tegen de bloedziekten.
Hoewel de ontwikkeling van ABE een opwindende stap voorwaarts is in de basisbewerking, er is nog meer werk voordat basisbewerking kan worden gebruikt om patiënten met genetische ziekten te behandelen, inclusief veiligheidstests, werkzaamheid, en bijwerkingen.
"Het creëren van een machine die de genetische verandering maakt die je nodig hebt om een ziekte te behandelen, is een belangrijke stap voorwaarts, maar het is slechts een deel van wat nodig is om een patiënt te behandelen, "zei Liu. "We moeten die machine nog afleveren, we moeten de veiligheid ervan testen, we moeten de gunstige effecten ervan bij dieren en patiënten beoordelen en ze afwegen tegen eventuele bijwerkingen - we moeten nog veel meer dingen doen."
"Maar het hebben van de machine is een goed begin."
 NASA ziet verticale windschering van invloed op tropische storm Muifa
NASA ziet verticale windschering van invloed op tropische storm Muifa Mysterieuze geomagnetische spike 3, 000 jaar geleden stelt ons begrip van het binnenste van de aarde op de proef
Mysterieuze geomagnetische spike 3, 000 jaar geleden stelt ons begrip van het binnenste van de aarde op de proef Robots die rondzwerven in Antarctische wateren onthullen waarom Ross Ice Shelf in de zomer snel smelt
Robots die rondzwerven in Antarctische wateren onthullen waarom Ross Ice Shelf in de zomer snel smelt regeringen, onderzoekers onderschatten impact van inefficiënt landgebruik op klimaatverandering
regeringen, onderzoekers onderschatten impact van inefficiënt landgebruik op klimaatverandering Nieuwe studie helpt stille aardbevingen langs het Noordereiland van Nieuw-Zeeland te verklaren
Nieuwe studie helpt stille aardbevingen langs het Noordereiland van Nieuw-Zeeland te verklaren
Hoofdlijnen
- Schoonmaken van microscoopglaasjes
- Hoe moleculaire scharen ziekten kunnen oplossen en DNA kunnen bewerken
- Pesticiden en slechte voeding schaden de diergezondheid
- Wetenschappers controleren cellen met licht,
- Je lichaamscellen gebruiken en verzetten zich tegen kracht, en ze bewegen. Zijn mechanobiologie
- Genotype: definitie, allelen en voorbeelden
- Voedingsgewoonte van Maleisische fruitvleermuizen
- Wat is de rol van glucose in het lichaam?
- Bacteriën krijgen resistentie van concurrenten
 Snapchat sluit zich aan bij EU-groep die haatzaaien bestrijdt
Snapchat sluit zich aan bij EU-groep die haatzaaien bestrijdt Afbeelding:Plasma-aandrijving voor kleine satellieten
Afbeelding:Plasma-aandrijving voor kleine satellieten Onderzoek naar de betekenis van oude geometrische grondwerken in het zuidwesten van Amazonië
Onderzoek naar de betekenis van oude geometrische grondwerken in het zuidwesten van Amazonië Feiten over de aanpassing van duiven voor kinderen
Feiten over de aanpassing van duiven voor kinderen Ultrakorte periode bruine dwerg ontdekt
Ultrakorte periode bruine dwerg ontdekt Kleine belletjes die grote invloed hebben op medische echografie
Kleine belletjes die grote invloed hebben op medische echografie Dodental hittegolf Canada bereikt 70
Dodental hittegolf Canada bereikt 70 Boeing maakt 96 vluchten om software te testen op onrustige Max-jet
Boeing maakt 96 vluchten om software te testen op onrustige Max-jet
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Spanish | Portuguese | German | Dutch | Danish | Norway | Italian | Swedish |

-
Wetenschap © https://nl.scienceaq.com






