
Wetenschap
Kunstmatig DNA kan de afgifte van actieve ingrediënten uit medicijnen regelen
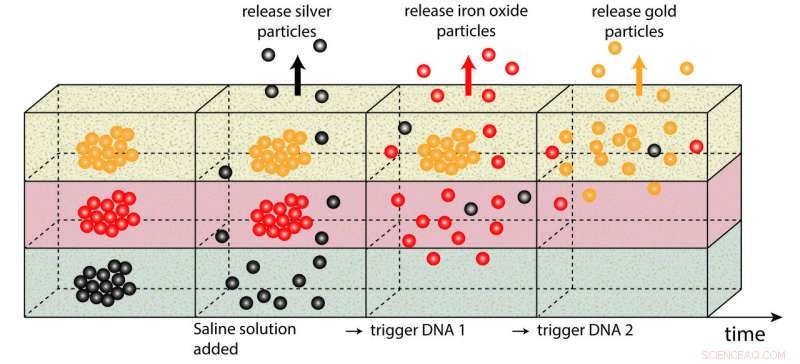
Verschillende soorten nanodeeltjes worden aan elkaar gebonden door DNA-fragmenten en Ceren Kimna komt op bepaalde tijdstippen vrij. Dergelijke verbindingen kunnen de basis worden van medicijnen die hun actieve ingrediënten in volgorde afgeven. Krediet:Ceren Kimna / TUM
Een team van de Technische Universiteit van München (TUM) ontwikkelt een medicijn met drie actieve ingrediënten die achtereenvolgens op specifieke tijdstippen worden vrijgegeven. Wat ooit de droom van een farmacoloog was, komt nu veel dichter bij de realiteit. Met een combinatie van hydrogels en kunstmatig DNA, nanodeeltjes kunnen achtereenvolgens worden vrijgegeven onder omstandigheden die vergelijkbaar zijn met die in het menselijk lichaam.
Het komt steeds vaker voor dat patiënten worden behandeld met verschillende medicijnen die met vaste tussenpozen worden ingenomen - een beperking die het dagelijks leven van patiënten bemoeilijkt en het risico op gemiste doses verhoogt.
Oliver Lieleg, een professor in de biomechanica en lid van de Munich School of BioEngineering aan de TUM, en promovendus Ceren Kimna hebben nu een proces ontwikkeld dat als basis zou kunnen dienen voor medicijnen die meerdere actieve ingrediënten bevatten die deze op betrouwbare wijze in een vooraf gedefinieerde volgorde op bepaalde tijden vrijgeven. "Bijvoorbeeld, een zalf die op een chirurgische incisie wordt aangebracht, kan eerst pijnmedicatie afgeven, gevolgd door een ontstekingsremmend medicijn en vervolgens een medicijn om zwelling te verminderen, " legt Oliver Lieleg uit.
De ene werkzame stof na de andere
"Zalven of crèmes die hun actieve ingrediënten met een vertraging vrijgeven, zijn op zich niet nieuw, " zegt Oliver Lieleg. Met de medicijnen die momenteel in gebruik zijn, echter, er is geen garantie dat twee of meer actieve ingrediënten niet tegelijkertijd in het organisme worden vrijgegeven.
Om het principe achter hun idee te testen, Oliver Lieleg en Ceren Kimna gebruikten zilver van nanometerformaat, ijzeroxide en gouddeeltjes ingebed in een hydrogel. Ze gebruikten een spectroscopische methode om de uitgang van de deeltjes uit de gel te volgen. De door de onderzoekers geselecteerde deeltjes hebben vergelijkbare bewegingskenmerken in de gel als de deeltjes die worden gebruikt om echte actieve ingrediënten te transporteren, maar zijn makkelijker en goedkoper te maken.
Het speciale ingrediënt dat de nanodeeltjes controleert, is kunstmatig DNA. In de natuur, DNA is vooral de drager van genetische informatie. Echter, onderzoekers maken steeds vaker gebruik van een andere eigenschap:het vermogen van DNA-fragmenten om met grote nauwkeurigheid te combineren, zowel wat betreft de soorten bindingen als hun sterkte, bijvoorbeeld om machines te bouwen op nanometerschaal.
De DNA-cascade:comprimeren en op het juiste moment loslaten
De zilverdeeltjes kwamen als eerste vrij. In de begintoestand, de deeltjes werden aan elkaar gebonden door DNA-fragmenten die door Lieleg en Kimna waren ontworpen met behulp van speciale software. De resulterende deeltjesclusters zijn zo groot dat ze niet in de hydrogel kunnen bewegen. Echter, wanneer een zoutoplossing wordt toegevoegd, ze scheiden van het DNA. Ze kunnen nu in de gel bewegen en naar de oppervlakte drijven. "Omdat de zoutoplossing ongeveer hetzelfde zoutgehalte heeft als het menselijk lichaam, we waren in staat om omstandigheden te simuleren waarin de actieve ingrediënten niet zouden worden vrijgegeven totdat de medicatie is aangebracht, " legt Ceren Kimna uit.
De gaasachtige DNA-structuur die de ijzeroxidedeeltjes omringt, bestaat uit twee soorten DNA:het eerste heeft een uiteinde bevestigd aan de ijzeroxidedeeltjes. Het tweede type is bevestigd aan de losse eindjes van het eerste type. Deze structuren worden niet beïnvloed door de zoutoplossing. De ijzeroxidedeeltjes kunnen pas vrijkomen als de eerste clusters zijn opgelost. Bij dit evenement komen niet alleen de zilveren nanodeeltjes vrij, maar ook DNA, die het "verbindings-DNA" van het tweede cluster elimineert zonder zelf verbindingen te vormen. Als resultaat, de ijzeroxidedeeltjes kunnen scheiden. Hierbij komen DNA-fragmenten vrij die op hun beurt de sleutel vormen tot de derde DNA-nanodeeltjescombinatie.
"De consistentie van zalven maakt ze de meest voor de hand liggende oplossing voor een op hydrogel gebaseerde aanpak. dit principe kan ook worden gebruikt in tabletten die verschillende effectieve ingrediënten in een specifieke volgorde in het lichaam kunnen afgeven, " legt prof. Lieleg uit.
 Veranderingen op zeeniveau in het verleden kunnen aanwijzingen voor de toekomst opleveren
Veranderingen op zeeniveau in het verleden kunnen aanwijzingen voor de toekomst opleveren Er zijn maar weinig werknemers in de publieke sector die een significante bijdrage kunnen leveren aan het bereiken van duurzaamheidsdoelstellingen
Er zijn maar weinig werknemers in de publieke sector die een significante bijdrage kunnen leveren aan het bereiken van duurzaamheidsdoelstellingen NASA volgt tropische storm Pablo . in het late seizoen van de oostelijke Atlantische Oceaan
NASA volgt tropische storm Pablo . in het late seizoen van de oostelijke Atlantische Oceaan Dringende noodzaak om langetermijneffecten van extreem weer op de gezondheid aan te pakken
Dringende noodzaak om langetermijneffecten van extreem weer op de gezondheid aan te pakken NASA geeft orkaan Fernanda een close-up
NASA geeft orkaan Fernanda een close-up
Hoofdlijnen
- Otzi the Iceman at een vetrijke laatste maaltijd
- Waarom is water belangrijk voor levende organismen?
- Waarom is de studie van de histologie belangrijk in uw algehele begrip van anatomie en fysiologie?
- Wat veroorzaakt het uitsterven van planten en dieren?
- Ontmoet Afrika's vogelmeester van vocale imitatie
- Temperatuur kan de pollenkleur beïnvloeden
- Wereldprimeur gebruikt satellieten en oceaanmodellen om de biodiversiteit op de Antarctische zeebodem te verklaren
- Welk proces voeren Ribosomes uit?
- Een genetische opstand in het vroege leven voorkomen
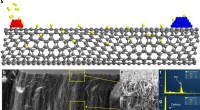
- Onderzoekers bepalen katalytische actieve plaatsen met behulp van koolstofnanobuisjes
- Wetenschappers onthullen nieuwe technologie om kleine clusters van atomen beter te begrijpen

- Ingenieurs verhogen de output van het zonne-ontziltingssysteem met 50%

- Hoe maak je een beter waterfilter? Keer het binnenstebuiten

- Grafeen en DNA:Wondermateriaal kan de sleutel zijn tot vasten, goedkope genetische sequencing

 Onderzoek peilt naar interculturele opvattingen over duurzaamheid
Onderzoek peilt naar interculturele opvattingen over duurzaamheid Zonne-energie omzetten in waterstofbrandstof, met hulp van fotosynthese
Zonne-energie omzetten in waterstofbrandstof, met hulp van fotosynthese Nanostructuren van elektrokatalysatoren sleutel tot verbeterde brandstofcellen, elektrolyzers
Nanostructuren van elektrokatalysatoren sleutel tot verbeterde brandstofcellen, elektrolyzers Vuursteen, De loodcrisis in Michigan had de stad in waterflessen moeten begraven. Dus, waarom niet?
Vuursteen, De loodcrisis in Michigan had de stad in waterflessen moeten begraven. Dus, waarom niet? Waarom de binnenkant van een tornado superkoud wordt,
Waarom de binnenkant van een tornado superkoud wordt,  Wiskundige modellering werpt nieuw licht op hoe continenten gevormd kunnen zijn
Wiskundige modellering werpt nieuw licht op hoe continenten gevormd kunnen zijn Oude Noord-Amerikaanse reptielen leefden op een eilandenarchipel in Zuid-Wales
Oude Noord-Amerikaanse reptielen leefden op een eilandenarchipel in Zuid-Wales Tweewielige transporter verandert in slimme sidekick
Tweewielige transporter verandert in slimme sidekick
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

