
Wetenschap
Een enkele dosis door ureum aangedreven nanorobots vermindert blaastumoren met 90% in muisonderzoek
Blaaskanker heeft een van de hoogste incidentiecijfers ter wereld en staat op de vierde plaats van meest voorkomende tumoren bij mannen. Ondanks het relatief lage sterftecijfer komt bijna de helft van de blaastumoren binnen vijf jaar weer boven water, waardoor voortdurende monitoring van de patiënt noodzakelijk is. Frequente ziekenhuisbezoeken en de noodzaak van herhaalde behandelingen dragen ertoe bij dat dit type kanker een van de duurste is om te genezen.
Hoewel de huidige behandelingen waarbij geneesmiddelen rechtstreeks in de blaas worden toegediend goede overlevingspercentages laten zien, blijft hun therapeutische werkzaamheid laag. Een veelbelovend alternatief omvat het gebruik van nanodeeltjes die therapeutische middelen rechtstreeks aan de tumor kunnen afleveren. Vooral nanorobots (nanodeeltjes die het vermogen hebben om zichzelf in het lichaam voort te bewegen) zijn opmerkelijk.
Dat blijkt uit een studie gepubliceerd in het tijdschrift Nature Nanotechnology onthult hoe een onderzoeksteam met succes de omvang van blaastumoren bij muizen met 90% heeft verminderd door middel van een enkele dosis door ureum aangedreven nanorobots.
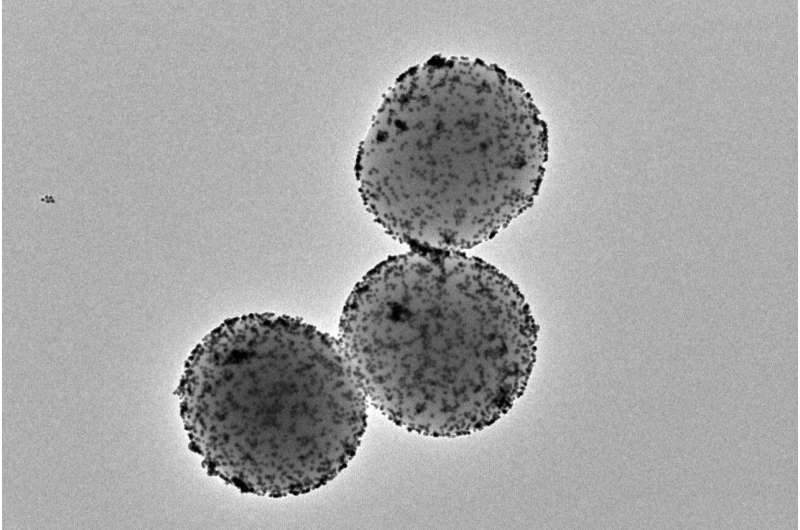
Deze kleine nanomachines bestaan uit een poreuze bol gemaakt van silica. Hun oppervlakken bevatten verschillende componenten met specifieke functies. Daartoe behoort het enzym urease, een eiwit dat reageert met ureum in de urine, waardoor het nanodeeltje zichzelf kan voortstuwen. Een ander cruciaal onderdeel is radioactief jodium, een radio-isotoop die vaak wordt gebruikt voor de plaatselijke behandeling van tumoren.
Het onderzoek, geleid door het Instituut voor Bio-engineering van Catalonië (IBEC) en CIC biomaGUNE in samenwerking met het Instituut voor Onderzoek in Biogeneeskunde (IRB Barcelona) en de Autonome Universiteit van Barcelona (UAB), maakt de weg vrij voor innovatieve behandelingen van blaaskanker. Deze verbeteringen zijn bedoeld om de duur van de ziekenhuisopname te verkorten, wat lagere kosten en meer comfort voor patiënten impliceert.
"Met een enkele dosis hebben we een afname van het tumorvolume met 90% waargenomen. Dit is aanzienlijk efficiënter gezien het feit dat patiënten met dit type tumor doorgaans 6 tot 14 ziekenhuisafspraken hebben met de huidige behandelingen. Een dergelijke behandelaanpak zou de efficiëntie vergroten en de de duur van de ziekenhuisopname en de behandelingskosten”, legt Samuel Sánchez, ICREA-onderzoeksprofessor bij IBEC en leider van het onderzoek uit.
De volgende stap, die al gaande is, is bepalen of deze tumoren na de behandeling terugkeren.
Een fantastische reis naar de blaas
In eerder onderzoek bevestigden de wetenschappers dat het zelfvoortstuwingsvermogen van nanorobots hen in staat stelde alle blaaswanden te bereiken. Dit kenmerk is voordelig in vergelijking met de huidige procedure waarbij de patiënt, na toediening van de behandeling rechtstreeks in de blaas, elk half uur van positie moet veranderen om ervoor te zorgen dat het medicijn alle wanden bereikt.
Deze nieuwe studie gaat nog verder door niet alleen de mobiliteit van nanodeeltjes in de blaas aan te tonen, maar ook hun specifieke accumulatie in de tumor. Deze prestatie werd mogelijk gemaakt door verschillende technieken, waaronder medische positronemissietomografie (PET) beeldvorming van de muizen, evenals microscopiebeelden van de weefsels die na voltooiing van het onderzoek werden verwijderd. Deze laatste werden vastgelegd met behulp van een fluorescentiemicroscopiesysteem dat speciaal voor dit project bij IRB Barcelona werd ontwikkeld. Het systeem scant de verschillende lagen van de blaas en zorgt voor een 3D-reconstructie, waardoor observatie van het hele orgaan mogelijk is.
"Het innovatieve optische systeem dat we hebben ontwikkeld, heeft ons in staat gesteld het door de tumor zelf gereflecteerde licht te elimineren, waardoor we nanodeeltjes door het hele orgaan kunnen identificeren en lokaliseren zonder voorafgaande labeling, met een ongekende resolutie. We hebben waargenomen dat de nanorobots niet alleen de tumor bereikten maar kwam er ook in terecht, waardoor de werking van het radiofarmaceutische middel werd versterkt", legt Julien Colombelli uit, leider van het Advanced Digital Microscopy-platform bij IRB Barcelona.
Het ontcijferen waarom nanorobots de tumor kunnen binnendringen vormde een uitdaging. Nanorobots missen specifieke antilichamen om de tumor te herkennen, en tumorweefsel is doorgaans stijver dan gezond weefsel.
"We hebben echter waargenomen dat deze nanorobots de extracellulaire matrix van de tumor kunnen afbreken door de pH lokaal te verhogen via een zelfrijdende chemische reactie. Dit fenomeen bevorderde een grotere tumorpenetratie en was gunstig bij het bereiken van preferentiële accumulatie in de tumor", legt Meritxell uit. Serra Casablancas, co-eerste auteur van de studie en IBEC-onderzoeker.
De wetenschappers concludeerden dus dat de nanorobots tegen het urotheel botsen alsof het een muur is, maar dat ze in de tumor, die sponsachtiger is, de tumor binnendringen en zich daarbinnen ophopen. Een sleutelfactor is de mobiliteit van de nanobots, waardoor de kans groter wordt dat ze de tumor bereiken.
Bovendien, volgens Jordi Llop, onderzoeker bij CIC biomaGUNE en medeleider van de studie:“verkleint de gelokaliseerde toediening van de nanorobots die de radio-isotoop dragen de kans op het genereren van nadelige effecten, en de hoge accumulatie in het tumorweefsel bevordert de radiotherapeutische werking.” gevolgen."
"De resultaten van dit onderzoek openen de deur naar het gebruik van andere radio-isotopen met een groter vermogen om therapeutische effecten teweeg te brengen, maar waarvan het gebruik beperkt is wanneer ze systemisch worden toegediend", voegt Cristina Simó, mede-eerste auteur van het onderzoek, toe.
Jaren werk en een spin-off
Het onderzoek consolideert de resultaten van ruim drie jaar samenwerking tussen verschillende instellingen. Een deel van de gegevens komt voort uit de proefschriften van Meritxell Serra en Ana Hortelao, beiden onderzoekers in IBEC's Smart nano-bio-devices-groep, geleid door Sánchez.
Het bevat ook het proefschrift van Cristina Simó, co-eerste auteur van de studie, die haar predoctoraal onderzoek uitvoerde in het Radiochemistry and Nuclear Imaging Lab onder leiding van Jordi Llop bij CIC biomaGUNE. De expertise van de groep van Esther Julián aan de UAB op het gebied van het diermodel van de ziekte is een extra bijdrage.
De technologie die ten grondslag ligt aan deze nanorobots, die Samuel Sánchez en zijn team al meer dan zeven jaar ontwikkelen, is onlangs gepatenteerd en dient als basis voor Nanobots Therapeutics, een spin-off van IBEC en ICREA, opgericht in januari 2023.
Het bedrijf, opgericht door Sánchez, fungeert als brug tussen onderzoek en klinische toepassing. “Het veiligstellen van robuuste financiering voor de spin-off is cruciaal om deze technologie verder te ontwikkelen en, als alles goed gaat, op de markt en in de samenleving te brengen. In juni, slechts vijf maanden na de oprichting van Nanobots Tx, hebben we met succes de eerste ronde van financiering, en we zijn enthousiast over de toekomst”, zegt Sanchez.
-
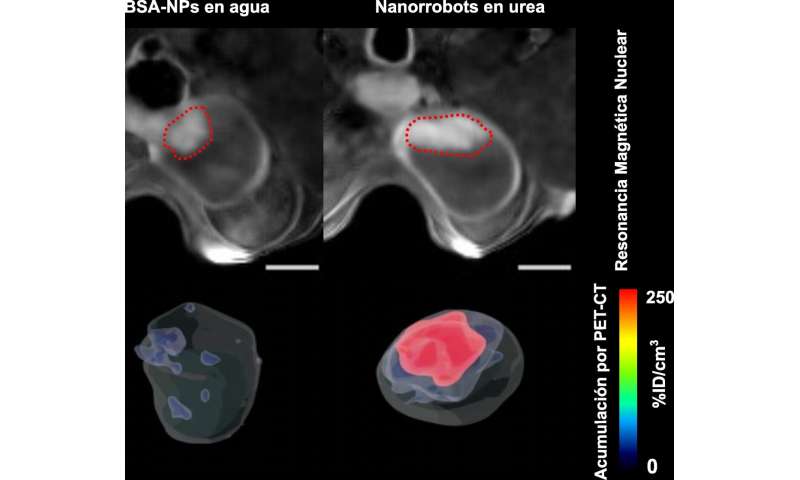
Lokalisatie van blaastumoren door middel van magnetische resonantiebeeldvorming en accumulatie van nanorobots in de tumor, gekwantificeerd door positronemissietomografie (PET). Credit:CIC biomaGUNE -
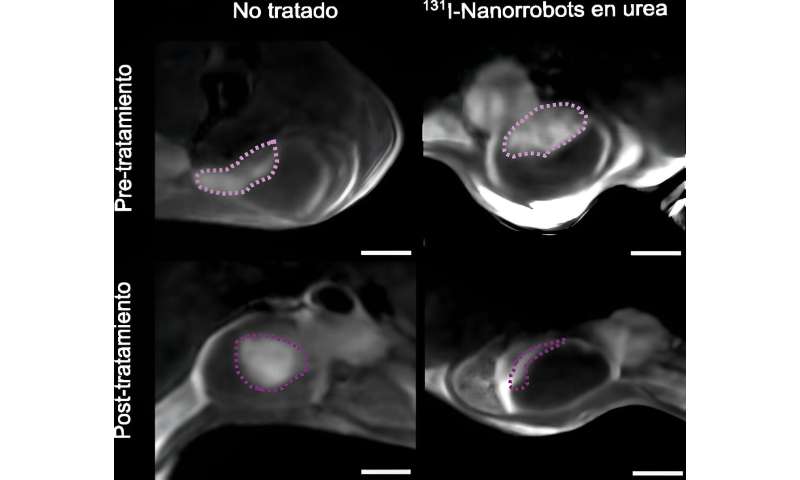
90% vermindering van de tumorgrootte na behandeling van kanker met nanorobots. Credit:CIC biomaGUNE
Technologische innovatie op het gebied van microscopie om nanorobots te lokaliseren
Het werken met nanorobots vormt een aanzienlijke wetenschappelijke uitdaging bij bio-imagingtechnieken voor het visualiseren van deze elementen in weefsels en in de tumor zelf. Gangbare niet-invasieve klinische technieken, zoals PET, missen de noodzakelijke resolutie om deze zeer kleine deeltjes op microscopisch niveau te lokaliseren.
Daarom heeft het Wetenschappelijk Microscopieplatform van IRB Barcelona een microscopietechniek gebruikt waarbij een laag laserlicht wordt gebruikt om monsters te belichten, waardoor 3D-beelden kunnen worden verkregen door lichtverstrooiing bij interactie met weefsels en deeltjes.
Toen ze merkten dat de tumor zelf een deel van het licht verstrooide, waardoor interferentie ontstond, ontwikkelden de wetenschappers een nieuwe techniek op basis van gepolariseerd licht die alle verstrooiing door het tumorweefsel en de tumorcellen tenietdoet. Deze innovatie maakt de visualisatie en locatie van nanorobots mogelijk zonder voorafgaande tagging met moleculaire technieken.
Meer informatie: Samuel Sánchez et al., Radionuclidentherapie met geaccumuleerde urease-aangedreven nanobots vermindert de grootte van de blaastumor in een orthotopisch muizenmodel, Nature Nanotechnology (2024). DOI:10.1038/s41565-023-01577-y
Journaalinformatie: Natuurnanotechnologie
Aangeboden door het Instituut voor Bio-engineering van Catalonië
 Een tweestapsbenadering gebruiken om alifatische amines om te zetten in onnatuurlijke aminozuren
Een tweestapsbenadering gebruiken om alifatische amines om te zetten in onnatuurlijke aminozuren Hoe het aantal atomen in een element te vinden
Hoe het aantal atomen in een element te vinden Nul tot held:over het hoofd gezien materiaal kan onze ecologische voetafdruk helpen verkleinen
Nul tot held:over het hoofd gezien materiaal kan onze ecologische voetafdruk helpen verkleinen Hoe de PKA te berekenen in titratie
Hoe de PKA te berekenen in titratie  Fotokatalysator maakt waterstofproductie 10 keer efficiënter
Fotokatalysator maakt waterstofproductie 10 keer efficiënter
 Groeien, maaien, mulch:de waarde van gazons vinden
Groeien, maaien, mulch:de waarde van gazons vinden Over wilde konijnen
Over wilde konijnen  NASA volgt orkaan Miriam in Central Pacific
NASA volgt orkaan Miriam in Central Pacific Tsunami's in het meer vormen een aanzienlijke bedreiging in het opwarmende klimaat
Tsunami's in het meer vormen een aanzienlijke bedreiging in het opwarmende klimaat  Saladeketen zegt dat een schonere landbouwmethode het toevoegen van biefstuk aan het menu zal compenseren. Wat is het?
Saladeketen zegt dat een schonere landbouwmethode het toevoegen van biefstuk aan het menu zal compenseren. Wat is het?
Hoofdlijnen
- Hoe recombinatie-frequenties te berekenen
- Voors en tegens van Recombinant DNA Technology
- Mottenvrouwtjes gebruiken geurnabijheid om partners aan te trekken
- Welke organen maken het vaatstelsel op?
- Genetische studie onderzoekt manieren om de productiviteit en malsheid van vlees te verhogen
- Nurture to Nature: hoe uw opvoeding uw hersenen kan beïnvloeden
- Mitochondria: definitie, structuur en functie (met diagram)
- Er is een genetische reden waarom Labrador Retrievers geobsedeerd zijn door voedsel
- Wat zijn de speciale dingen die gebeuren wanneer cellen worden gesplitst?
- NASA onderzoekt gebruik van baanbrekend materiaal voor nieuwe sensoren

- Dieet-nanodeeltjes hebben invloed op het darmmicrobioom
- Koolstofnanobuisjes het beste voor 3D-elektronica
- Onderzoeker ontwikkelt nieuwe generatie grafeen

- Twee-fotonmicroscopie:nieuw onderzoek kan de kosten van krachtige microscooptechniek drastisch verlagen
 Met behulp van coseismische calcietaders tot nu toe aardbevingen in de breuklijnen in New Mexico, een half miljoen jaar geleden
Met behulp van coseismische calcietaders tot nu toe aardbevingen in de breuklijnen in New Mexico, een half miljoen jaar geleden Partijdige berichtgeving heeft een grotere impact op kijkers zonder sterke mediavoorkeuren
Partijdige berichtgeving heeft een grotere impact op kijkers zonder sterke mediavoorkeuren Hoe melk een dierlijk lichaam goed doet?
Hoe melk een dierlijk lichaam goed doet? Op hematiet gebaseerde nanodraadstructuren om de conversie van zonne-energie naar brandstof bij foto-elektrochemische watersplitsing te verbeteren
Op hematiet gebaseerde nanodraadstructuren om de conversie van zonne-energie naar brandstof bij foto-elektrochemische watersplitsing te verbeteren Heeft Jupiter Venus in een op hol geslagen kas geduwd?
Heeft Jupiter Venus in een op hol geslagen kas geduwd? Waarom planten wereldwijd houtachtig werden
Waarom planten wereldwijd houtachtig werden Met veranderende demografie, meer raciale/etnische socialisatie nodig voor blanke jongeren
Met veranderende demografie, meer raciale/etnische socialisatie nodig voor blanke jongeren Klittenbandachtige voedselsensor detecteert bederf en besmetting
Klittenbandachtige voedselsensor detecteert bederf en besmetting
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

