
Wetenschap
Onderzoeksteam ontwikkelt op eiwitten gebaseerde microcapsule voor point-of-care-diagnostiek
Aptameren, de op nucleïnezuur gebaseerde biosensoren met het vermogen om specifieke eiwitten of kleine moleculen te binden, bieden een manier om doelmoleculen te identificeren zonder de complexiteit van analytische apparaten. Hoewel ze steeds vaker worden gebruikt in diagnostische toepassingen voor verschillende ziekten, is hun potentieel als effectieve sensoren voor kanker bijzonder opmerkelijk, omdat vroege detectie van kanker kan leiden tot een genezingspercentage van meer dan 90%.
Aptameren hebben echter te maken met kritische beperkingen omdat ze gevoelig zijn voor afbraak of aggregatie door nucleasen of geladen eiwitten die aanwezig zijn in biologische monsters zoals bloed of speeksel. Dit maakt het een uitdaging om ze rechtstreeks in klinische monsters te gebruiken zonder eerst die moleculen te verwijderen. Onlangs heeft een team van onderzoekers van de Pohang University of Science and Technology (POSTECH) dit probleem opgelost met behulp van een op eiwitten gebaseerde microcapsule.
Het onderzoeksteam onder leiding van professoren Seung Soo Oh en Sungwook Woo en Ph.D. kandidaat Jinmin Kim van de afdeling Materiaalwetenschappen en Techniek bij POSTECH ontwikkelde een aptameersensorsysteem dat de snelle detectie van doelmoleculen rechtstreeks uit biologische monsters mogelijk maakt, waardoor de noodzaak van voorbehandelingsprocessen wordt geëlimineerd. Dit onderzoek is gepubliceerd in Biosensors and Bioelectronics .
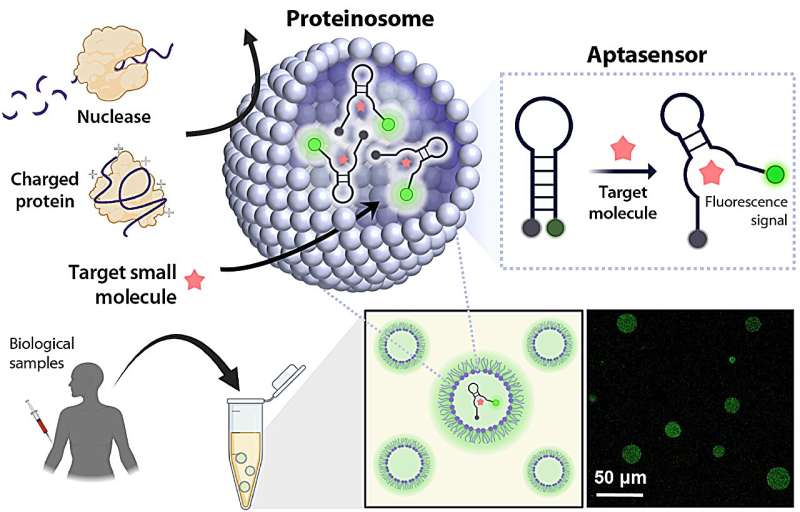
In dit onderzoek creëerde het team bolvormige microcapsules, proteïnosomen genaamd, op basis van zelfassemblage van eiwit-polymeer amfifielen. De microcapsule is ontworpen om een aptasensor te bevatten die is gebaseerd op een structuur-omschakelend aptameer dat reageert met doelmoleculen om onmiddellijk een fluorescerend signaal te produceren, en het oppervlak is samengesteld uit een grootteselectief semi-permeabel membraan dat selectief alleen kleine doelmoleculen doorlaat. terwijl het effectief de toegang van grotere schadelijke eiwitten blokkeert.
De resultaten toonden aan dat de optimale prestaties van de aptasensor voor doeldetectie volledig behouden bleven, zelfs in onbehandelde biovloeistoffen, waardoor effectieve en snelle detectie van doelmoleculen mogelijk werd, zoals estradiol, een belangrijk vrouwelijk hormoon geassocieerd met kanker in de voortplantingsorganen, dopamine, een neurotransmitter. dat wijst op de ziekte van Parkinson of Alzheimer, en cocaïne, een gereguleerde stof die vaak snelle detectie ter plaatse vereist.
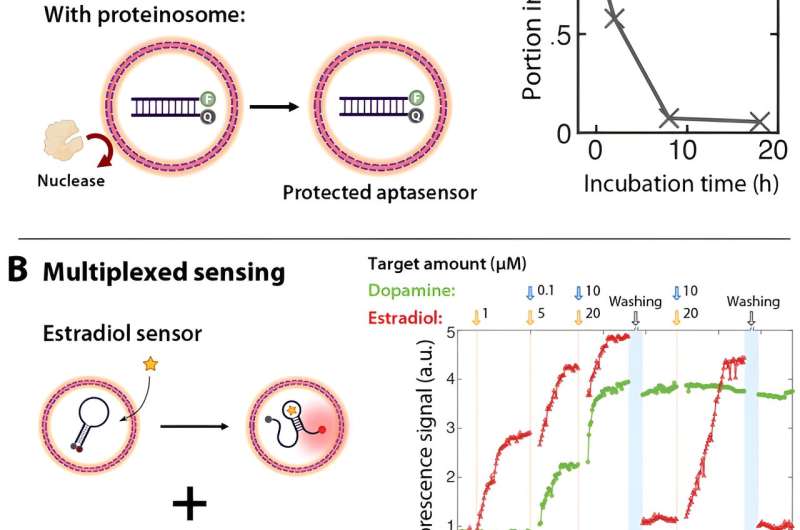
De door de onderzoekers ontwikkelde capsules vertoonden een robuuste bescherming tegen schadelijke eiwitten.
De aptasensoren in de microcapsules bleven bijvoorbeeld 18 uur lang onbeschadigd in sterk geconcentreerde nuclease-oplossingen, ongeveer 300.000 maal de normale serumspiegel. Door gebruik te maken van de eigenschap dat elke capsule als een onafhankelijk 'reactievat' functioneert, hebben de onderzoekers bovendien de onafhankelijke werking van meerdere aptasensoren in hetzelfde mengsel aangetoond, waardoor gelijktijdige realtime detectie van meerdere doelmoleculen mogelijk is en hun respectieve concentratieveranderingen kunnen worden gevolgd.
Professor Seung Soo Oh, die het onderzoek leidde, legde uit:"Door monsterscheiding en doeldetectie te integreren, hebben we een nieuwe point-of-care-biosensortechnologie met kleine moleculen ontwikkeld die direct toepasbaar is op biologische monsters zoals serum. Dit platform heeft het potentieel om zorgen voor een revolutie in de geneeskunde, waarbij vroege ziektedetectie en gepersonaliseerde behandeling worden gecombineerd."
Ph.D. kandidaat Jinmin Kim zei:"Het op proteïnosoom gebaseerde detectieplatform is een veelzijdig systeem omdat het kan worden uitgebreid naar sensoren voor verschillende doelmoleculen door simpelweg de aptasensor binnenin te veranderen."
Meer informatie: Jinmin Kim et al, Aptasensor-inkapseling van semi-permeabele proteïnosomen voor directe doeldetectie in onbehandelde biovloeistoffen, Biosensoren en bio-elektronica (2024). DOI:10.1016/j.bios.2024.116062
Aangeboden door Pohang Universiteit voor Wetenschap en Technologie
 Ontwikkelingen op het gebied van dubbelatomige katalysatoren maken hernieuwbare energiebronnen efficiënter
Ontwikkelingen op het gebied van dubbelatomige katalysatoren maken hernieuwbare energiebronnen efficiënter  Nieuw onderzoek naar de risico's van blootstelling aan lood door kogels die worden gebruikt bij de jacht op groot wild
Nieuw onderzoek naar de risico's van blootstelling aan lood door kogels die worden gebruikt bij de jacht op groot wild Onderzoekers koppelen weesreceptor aan opioïde-geïnduceerde jeuk
Onderzoekers koppelen weesreceptor aan opioïde-geïnduceerde jeuk Een niet-giftig alternatief voor gekleurde rook creëren
Een niet-giftig alternatief voor gekleurde rook creëren Een poreus porfyrine gebruiken om edele metalen terug te winnen uit elektronisch afval
Een poreus porfyrine gebruiken om edele metalen terug te winnen uit elektronisch afval
 NASA-satelliet analyseert krachtige supertyfoon Mangkhut
NASA-satelliet analyseert krachtige supertyfoon Mangkhut Bosbranden treffen Groenland na recordtemperaturen
Bosbranden treffen Groenland na recordtemperaturen De kust van Louisiana heeft nog steeds last van stormen, zich schrap zetten voor meer
De kust van Louisiana heeft nog steeds last van stormen, zich schrap zetten voor meer Uit historische beoordelingen blijkt dat megadroogtes op sommige plaatsen permanent kunnen worden als gevolg van klimaatverandering
Uit historische beoordelingen blijkt dat megadroogtes op sommige plaatsen permanent kunnen worden als gevolg van klimaatverandering Planten nemen meer koolstof op als ze eenmaal gewend zijn aan warmere temperaturen
Planten nemen meer koolstof op als ze eenmaal gewend zijn aan warmere temperaturen
Hoofdlijnen
- Hoe de hormonen van de hypofyse te onthouden
- Nieuw rapport vindt succes in adoptieprogramma voor wilde paarden, critici zijn het daar niet mee eens
- Zouden herten aanwijzingen kunnen bevatten over het verband tussen malariaresistentie en sikkelcel?
- Cicade-palooza! Miljarden insecten om Amerika te bedekken
- Oudste Homo Sapiens-fossielen die ooit zijn gevonden, suggereren een herschrijving van menselijke evolutie
- Menselijke activiteit maakt het voor wetenschappers moeilijker om oceanen uit het verleden te interpreteren
- Lichaamsmassa van bijen, ziekteverwekkers en lokale klimaatinvloeden hittetolerantie
- Onderzoekers ontdekten dat overmatige sociale interactie de collectieve respons verminderde
- Nieuwe onderzoeksaanpak:onderzoek naar het mondgevoel van voedsel met een microscoop
- Kleine sondes van geconjugeerd polyelektrolyt-nanodeeltjes geproduceerd door ultrasone trillingen blijken superieur aan commerciële producten
- Nanogestructureerde metalen coatings laten het licht door voor elektronische apparaten

- Wetenschappers ontcijferen de nanoschaalarchitectuur van een keversschil

- Nanodraden gekweekt op grafeen hebben een verrassende structuur
- Onderzoekers blijven de productie van grafeen verfijnen met HPC

 Microplastische verontreiniging gevonden in gemeenschappelijke bron van grondwater, onderzoekers rapporteren
Microplastische verontreiniging gevonden in gemeenschappelijke bron van grondwater, onderzoekers rapporteren Onderzoeksteam ontdekt nieuwe eigenschap van licht
Onderzoeksteam ontdekt nieuwe eigenschap van licht  Is deze beloegawalvis serieus een Russische spion?
Is deze beloegawalvis serieus een Russische spion?  Chemieprojecten met oxidatie
Chemieprojecten met oxidatie  Bio-ingenieurs zetten stap in de richting van een patch die een gebroken hart kan herstellen
Bio-ingenieurs zetten stap in de richting van een patch die een gebroken hart kan herstellen Hoe vrije radicalen uw lichaam beïnvloeden
Hoe vrije radicalen uw lichaam beïnvloeden  Twitter stijgt naarmate de wereldwijde gebruikersgroei weer opleeft
Twitter stijgt naarmate de wereldwijde gebruikersgroei weer opleeft Laag verlies, volledig vezelsysteem voor sterke en efficiënte koppeling tussen verre atomen
Laag verlies, volledig vezelsysteem voor sterke en efficiënte koppeling tussen verre atomen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

