
Wetenschap
Nanodeeltjes van rijstzemelen zijn veelbelovend als betaalbaar en gericht middel tegen kanker
Recente onderzoeken hebben aangetoond dat van planten afkomstige nanodeeltjes (pdNP's) met therapeutische effecten een effectief alternatief kunnen zijn voor traditionele kankerbehandelingen. Tot op heden zijn er echter geen pdNP's goedgekeurd als therapeutische middelen tegen kanker.
Rijstzemelen zijn een bijproduct dat ontstaat tijdens het raffinageproces van rijst en dat een beperkt nut en een lage commerciële waarde heeft. Het bevat echter verschillende verbindingen met kankerbestrijdende eigenschappen, zoals γ-oryzanol en γ-tocotrienol.
Om deze therapeutische eigenschappen van rijstzemelen te onderzoeken, heeft een team van onderzoekers onder leiding van professor Makiya Nishikawa van de Tokyo University of Science (TUS) in Japan nanodeeltjes uit rijstzemelen ontwikkeld en hun effectiviteit getest in muismodellen. Hun studie, gepubliceerd in het Journal of Nanobiotechnology op 16 maart 2024, was co-auteur van Dr. Daisuke Sasaki, mevrouw Hinako Suzuki, universitair hoofddocent Kosuke Kusamori en assistent-professor Shoko Itakura van TUS.
"De afgelopen jaren wordt een toenemend aantal nieuwe medicijnmodaliteiten ontwikkeld. Tegelijkertijd zijn de ontwikkelingskosten die verband houden met nieuwe therapieën dramatisch gestegen, wat heeft bijgedragen aan de last van de medische kosten. Om dit probleem aan te pakken, hebben we rijstzemelen gebruikt, een industrieel afval met kankerbestrijdende eigenschappen, om nanodeeltjes te ontwikkelen", legt prof. Nishikawa uit.
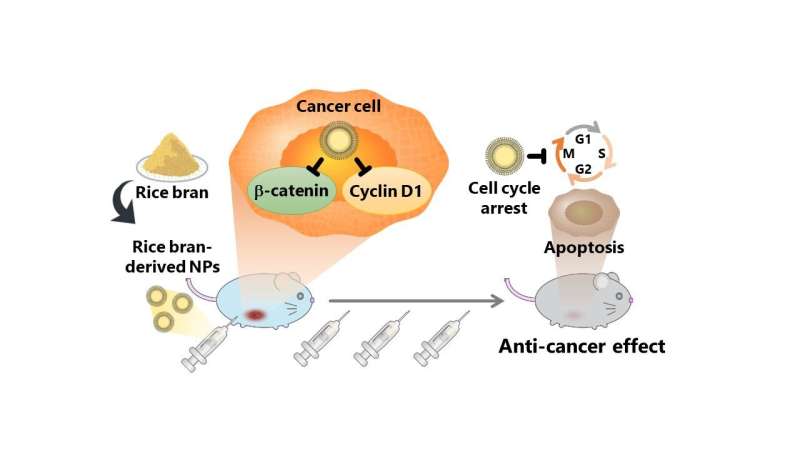
De studie evalueerde de kankerbestrijdende effecten van van rijstzemelen afgeleide nanodeeltjes (rbNP's), die werden verkregen door het verwerken en zuiveren van een suspensie van Koshihikari-rijstzemelen in water. Toen een kankercellijn genaamd colon26 werd behandeld met rbNP's, werd de celdeling gestopt en werd geprogrammeerde celdood geïnduceerd, wat wijst op sterke kankerbestrijdende effecten van de nanodeeltjes. De waargenomen antikankeractiviteit van rbNPs kan worden toegeschreven aan γ-tocotrienol en γ-oryzanol, die gemakkelijk worden opgenomen door kankercellen, wat resulteert in het stilvallen van de celcyclus en geprogrammeerde celdood.
Bovendien verminderden rbNP's de expressie van eiwitten, zoals β-catenine (een eiwit geassocieerd met de Wnt-signaleringsroute die betrokken is bij celproliferatie) en cycline D1, waarvan bekend is dat ze het terugkeren van kanker en metastasen bevorderen. Bovendien verminderden de rbNP's de expressie van β-catenine alleen in colon26-cellen zonder de niet-kankercellen te beïnvloeden.
"Een belangrijk punt van zorg in de context van pdNP's is hun lage farmacologische activiteit in vergelijking met farmaceutische geneesmiddelen. RbNP's vertoonden echter een hogere antikankeractiviteit dan DOXIL, een liposomale farmaceutische formulering van doxorubicine. Bovendien is doxorubicine cytotoxisch voor zowel kankercellen als niet-kankercellen. , terwijl rbNP's specifiek cytotoxisch zijn voor kankercellen, wat erop wijst dat rbNP's veiliger zijn dan doxorubicine", zegt prof. Nishikawa.
Om de kankerbestrijdende eigenschappen van rbNP's in het levende lichaam te bevestigen, injecteerden de onderzoekers rbNP's in muizen met agressief adenocarcinoom in hun peritoneale holte (omsloten door het middenrif, de buikspieren en het bekken en herbergen organen zoals darmen, lever en nieren). Ze observeerden een significante onderdrukking van de tumorgroei zonder nadelige effecten op de muizen. Bovendien remden de rbNP's de metastatische groei van melanoom B16-BL6-cellen van muizen significant in een muismodel met longmetastasen.
Rijstzemelen hebben verschillende eigenschappen die het tot een uitstekende bron van therapeutische pdNP's maken. Ten eerste is het economisch in vergelijking met veel andere bronnen van pdNP's. Bijna 40% van de rijstzemelen wordt in Japan weggegooid, wat een direct beschikbare bron van grondstoffen oplevert. Ten tweede is de bereidingsefficiëntie van rbNPs hoger dan die van eerder gerapporteerde pdNPs.
Naast dat ze praktisch en veilig zijn als therapeutisch middel tegen kanker, zijn de fysisch-chemische eigenschappen van rbNP's zeer stabiel. Een paar parameters, zoals het opzetten van scheidingstechnologieën op farmaceutisch niveau, het beoordelen van controleparameters van het productieproces en de evaluatie van de werkzaamheid en veiligheid in menselijke kankercellijnen en xenograft-diermodellen, moeten echter worden onderzocht voorafgaand aan klinische proeven bij mensen. /P>
Kortom, rijstzemelen, een afvalproduct uit de landbouw, zijn een bron van therapeutische pdNP's die betaalbaar, effectief en veilig zijn, en het potentieel hebben om de behandeling van kanker in de toekomst radicaal te veranderen.
“Door een productiemethode voor nanodeeltjes van rijstzemelen op te zetten met een stabiele kwaliteit en door hun veiligheid en effectiviteit te bevestigen, kunnen we geneesmiddelen voor de behandeling van kanker ontwikkelen die duurzaam, milieuvriendelijk en betaalbaar zijn. Bijgevolg kunnen we mogelijk meer kankerpatiënten helpen hun kanker te behouden goede lichamelijke en geestelijke gezondheid na de behandeling”, besluit prof. Nishikawa.