
Wetenschap
Nieuwe studie ontdekt klein doelwit op RNA om ontstekingen te kortsluiten
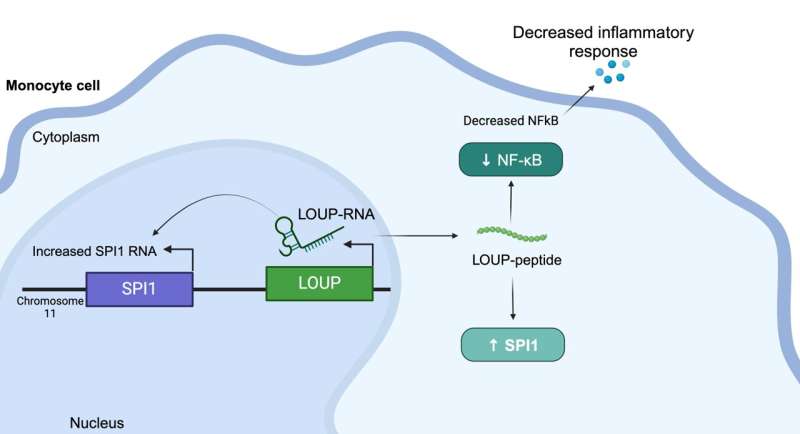
Onderzoekers van UC Santa Cruz hebben een peptide in menselijk RNA ontdekt dat ontstekingen reguleert en mogelijk een nieuw pad biedt voor de behandeling van ziekten zoals artritis en lupus. Het team gebruikte een screeningproces gebaseerd op de krachtige tool voor genbewerking CRISPR om licht te werpen op een van de grootste mysteries over ons RNA:het molecuul dat verantwoordelijk is voor het uitvoeren van genetische informatie in ons DNA.
Dit peptide is afkomstig van een lang niet-coderend RNA (lncRNA), genaamd LOUP. Volgens de onderzoekers codeert het menselijk genoom voor meer dan 20.000 lncRNA's, waardoor het de grootste groep genen is die uit het genoom worden geproduceerd. Maar ondanks deze overvloed weten wetenschappers weinig over waarom lncRNA’s bestaan of wat ze doen. Dit is de reden waarom lncRNA soms de ‘donkere materie van het genoom’ wordt genoemd.
De studie, gepubliceerd op 23 mei in de Proceedings of the National Academy of Sciences (PNAS), is een van de weinige in de bestaande literatuur die de mysteries van lncRNA wegneemt. Het presenteert ook een nieuwe strategie voor het uitvoeren van high-throughput screening om snel functionele lncRNA's in immuuncellen te identificeren. Dankzij de gepoolde schermbenadering kunnen onderzoekers zich in één experiment op duizenden genen richten, wat een veel efficiëntere manier is om niet-gekarakteriseerde delen van het genoom te bestuderen dan traditionele experimenten die zich op één gen tegelijk concentreren.
Het onderzoek werd geleid door immunoloog Susan Carpenter, een professor en Sinsheimer-voorzitter van de afdeling Moleculaire, Cel- en Ontwikkelingsbiologie van UC Santa Cruz. Ze bestudeert de moleculaire mechanismen die betrokken zijn bij de bescherming tegen infecties. Ze richt zich specifiek op de processen die tot ontstekingen leiden om de rol te bepalen die lncRNA's in deze routes spelen.
"Ontsteking is een centraal kenmerk van vrijwel elke ziekte", zei ze. "In deze studie concentreerde mijn laboratorium zich op het proberen te bepalen welke lncRNA-genen betrokken zijn bij het reguleren van ontstekingen."
Dit betekende het bestuderen van lncRNA's in een type witte bloedcel dat bekend staat als monocyt. Ze gebruikten een aanpassing van de CRISPR/Cas9-technologie, genaamd CRISPR-inhibitie (CRISPRi), om gentranscriptie te onderdrukken en uit te zoeken welke van de lncRNA's van een monocyt een rol spelen bij de differentiatie in een macrofaag – een ander type witte bloedcel dat cruciaal is voor een goed functionerende immuunrespons.
Daarnaast gebruikten de onderzoekers CRISPRi om macrofaag lncRNA te screenen op betrokkenheid bij ontstekingen. Onverwachts vonden ze een regio die multifunctioneel is en als RNA kan werken, maar ook een onontdekt peptide bevat dat ontstekingen reguleert.
Door te begrijpen dat dit specifieke peptide ontstekingen reguleert, hebben medicijnfabrikanten een doelwit om de moleculaire interactie achter die reactie te blokkeren om deze te onderdrukken, zei Carpenter. "In een ideale wereld zou je een klein molecuul ontwerpen om die specifieke interactie te verstoren, in plaats van je bijvoorbeeld te richten op een eiwit dat door het hele lichaam tot expressie zou kunnen komen," legde ze uit. "We zijn nog ver verwijderd van het met dat precisieniveau targeten van deze routes, maar dat is zeker het doel. Er is momenteel veel belangstelling voor RNA-therapieën."
Co-auteurs van de studie van UC Santa Cruz zijn onder meer Haley Halasz, Eric Malekos, Sergio Covarrubias, Samira Yitiz, Christy Montano, Lisa Sudek en Sol Katzman, samen met onderzoekers van UCSF en MIT.