
Wetenschap
Herbruikbare katalysator maakt oxidatie van C–H-bindingen met zuurstof eenvoudiger en efficiënter

Krediet:Tokyo Tech
In de chemische industrie is de selectieve splitsing en oxidatie van koolstof-waterstof (C-H) bindingen, genaamd "oxidatieve C-H-functionalisatie", een essentiële stap in de productie van veel oplosmiddelen, polymeren en oppervlakteactieve stoffen, evenals tussenverbindingen voor landbouwchemicaliën en farmaceutica. Idealiter zou men zuurstof willen gebruiken (O2 ) als enige oxidatiemiddel in dit proces om het gebruik van duurdere en milieubelastende stoffen, zoals waterstofperoxide (H2 O2 ), chloor (Cl2 ), of salpeterzuur (HNO3 ).
Echter, met behulp van O2 omdat het oxidatiemiddel enkele onopgeloste problemen met zich meebrengt. Hoewel er enige vooruitgang is geboekt op het gebied van winbare en herbruikbare katalysatoren, vereisen de meeste heterogene systemen hoge reactietemperaturen, hoge O2 hoge druk of het gebruik van giftige additieven. Dit verlamt op zijn beurt de reikwijdte van potentiële toepassingen, schaalbaarheid en efficiëntie van deze katalytische systemen.
Tegen deze achtergrond heeft een team van wetenschappers van Tokyo Tech, onder leiding van universitair hoofddocent Keigo Kamata, onlangs een veelbelovende katalysator gevonden voor oxidatieve CH-functionalisatie. Zoals uitgelegd in hun paper gepubliceerd in ACS Applied Materials &Interfaces , concludeerden ze op basis van eerdere kennis dat geïsoleerde mangaan (Mn) soorten gefixeerd in een kristallijne matrix een hoogwaardige heterogene katalysator zouden kunnen vormen, zelfs bij milde reactieomstandigheden.
Dienovereenkomstig onderzochten ze de katalysator murdochite-type Mg6 MnO8 , een steenzoutstructuur van magnesiumoxide (MgO) met een achtste van de Mg 2+ ionen vervangen door Mn 4+ ionen en nog een achtste vervangen door vacatures, wat resulteert in een kristal met Mn-ionen en vacatures die afwisselende lagen bezetten. Met behulp van een kosteneffectieve sol-gel-methode, geholpen door appelzuur, bereidde het team Mg6 MnO8 nanodeeltjes met een zeer groot oppervlak. Dr. Kamata legt uit:"Het specifieke oppervlak van onze Mg6 MnO8 katalysator was 104 m 2 /g, ongeveer zeven keer hoger dan die van Mg6 MnO8 gesynthetiseerd met behulp van eerder gerapporteerde methoden."
De onderzoekers toonden door middel van talrijke experimenten ook aan dat hun Mg6 MnO8 nanodeeltjes zouden de selectieve oxidatie van C–H van verschillende alkylareenverbindingen efficiënt kunnen katalyseren, zelfs onder milde reactieomstandigheden, namelijk 40°C en atmosferische druk. De opbrengst van de eindproducten was ook hoger dan die verkregen met bestaande op Mn gebaseerde katalysatoren. Om het helemaal af te maken, de Mg6 MnO8 nanodeeltjes kunnen gemakkelijk worden teruggewonnen via filtratie en vervolgens hergebruikt zonder enig duidelijk verlies van katalytische activiteit na meerdere cycli.
Ten slotte probeerde het team te begrijpen waarom hun voorgestelde katalysator zo goed presteerde door middel van een reeks kinetische en mechanistische onderzoeken. Ze concludeerden dat de isolatie van redox-sites (in dit geval Mn-soorten) in een kristallijne basismatrix (MgO) een bijzonder belangrijk kenmerk was om oxidatieve C–H-functionalisatie te bereiken met behulp van O2 bij milde omstandigheden.
Tevreden met de resultaten en hun bevindingen speculeert Dr. Kamata:"Onze aanpak vormt een veelbelovende strategie voor de ontwikkeling van zeer efficiënte heterogene oxidatiesystemen met brede substraatscopes." + Verder verkennen
Bariumruthenaat:een gemakkelijk te hanteren perovskietkatalysator met hoog rendement voor de oxidatie van sulfiden
 "The R134a vs. the R410a
"The R134a vs. the R410a Wetenschappers ontwikkelen een efficiënte manier om goedkope koellichamen te produceren
Wetenschappers ontwikkelen een efficiënte manier om goedkope koellichamen te produceren Beheersbare oppervlaktedefect engineering op overgangsmetaal trichalcogenide
Beheersbare oppervlaktedefect engineering op overgangsmetaal trichalcogenide Een potentieel goedkope, efficiënt en milieuvriendelijk systeem voor het zuiveren van aardgas
Een potentieel goedkope, efficiënt en milieuvriendelijk systeem voor het zuiveren van aardgas Hoe kolibries te voeden Graansiroop
Hoe kolibries te voeden Graansiroop
 Radioactiviteit van olie- en gasafvalwater blijft bestaan in stroomsedimenten in Pennsylvania
Radioactiviteit van olie- en gasafvalwater blijft bestaan in stroomsedimenten in Pennsylvania Onderzoek suggereert dat er overblijfselen zijn van de Beringstraat en andere menselijke migratiepaden onder water op knelpunten
Onderzoek suggereert dat er overblijfselen zijn van de Beringstraat en andere menselijke migratiepaden onder water op knelpunten Typen Smog
Typen Smog Levenscyclus van een duizendpoot
Levenscyclus van een duizendpoot  Al 110 jaar is klimaatverandering in het nieuws. Zijn we eindelijk klaar om te luisteren?
Al 110 jaar is klimaatverandering in het nieuws. Zijn we eindelijk klaar om te luisteren?
Hoofdlijnen
- Ontdekking van orgaanontwikkeling kan strijd tegen kanker stimuleren
- Zijn leefgebied is gedecimeerd, deze charismatische vogel uit Minnesota danst op de rand van de vergetelheid
- Vroegwaarschuwingssysteem voor veranderingen in het milieu:nieuwe dierenlabels met camera's en AI volledige eerste vlucht
- Biochemistry Blotting Techniques
- Onderzoek toont aan dat commerciële oogst van brekende schildpadden leidt tot bevolkingsafname
- Het vastleggen van de waardeketen leidt tot toekomstige bezorgdheid over de duurzaamheid van bossen
- Biologische leeftijd verklaart variatie in reacties op stress
- Hittetolerante broccoli voor de toekomst
- De structurele verschillen tussen zenuwen en bloedvaten
- Nieuwe NanoZymes gebruiken licht om bacteriën te doden
- Zacht geheugenapparaat opent de deur naar nieuwe biocompatibele elektronica (met video)

- Grafeen gemaakt met lasers voor draagbare gezondheidsapparaten

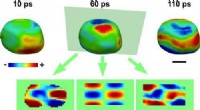
- Gouden nanokristaltrilling vastgelegd op film met miljard frames per seconde (met video)
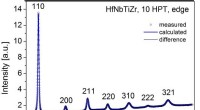
- Hoe kan röntgendiffractie worden gebruikt voor een betrouwbare studie van nanogestructureerde materialen?
 Nieuw model voor het meten van de beweging van de ijskap kan de voorspellingen van de zeespiegelstijging verbeteren
Nieuw model voor het meten van de beweging van de ijskap kan de voorspellingen van de zeespiegelstijging verbeteren Apparaat maakt opladen elektrisch voertuig tweerichtingsverkeer
Apparaat maakt opladen elektrisch voertuig tweerichtingsverkeer Hoe een auto op zonne-energie te bouwen
Hoe een auto op zonne-energie te bouwen  Astrofysici leggen een nieuwe klasse van voorbijgaande objecten vast
Astrofysici leggen een nieuwe klasse van voorbijgaande objecten vast Leren van mosselen:een tweekleppige zeedier inspireert onderzoekers om sterkere polymeren te maken
Leren van mosselen:een tweekleppige zeedier inspireert onderzoekers om sterkere polymeren te maken Kan een geluidsgolf je doden?
Kan een geluidsgolf je doden?  Nettowinst Ryanair vlakt af in eerste halfjaar
Nettowinst Ryanair vlakt af in eerste halfjaar Duitsers ventileren VW-woede in massaal dieselgate-pak
Duitsers ventileren VW-woede in massaal dieselgate-pak
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

