
Wetenschap
Injecteerbare stamcelassemblage voor kraakbeenregeneratie
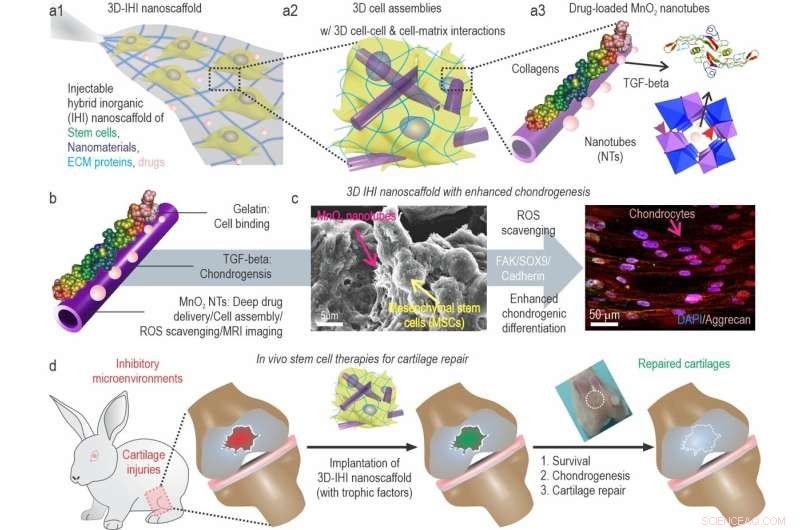
a) Een schematische illustratie van 3D TGFβ-BMSC-IHI nanoscaffold. b) De schematische illustratie van gelatine-gecoat en TGF-β3-geladen MnO2 NT's. c) Het FESEM-beeld gaf aan dat de meeste BMSC's contacten vormen met andere cellen en de 1D-fibrilachtige structuren, die vergelijkbaar waren met de structuren van natuurlijke weefsels. d) Door de oxidatieve micro-omgeving te hermodelleren, de levensvatbaarheid van de cellen te verbeteren en de chondrogenese van getransplanteerde cellen te verbeteren, zou kraakbeenregeneratie eindelijk kunnen worden bereikt. Krediet:Science China Press
Een studie onder leiding van Prof. Qiuyu Zhang (Northwestern Polytechnical University), Prof. Ki-Bum Lee (Rutgers University) en Prof. Liang Kong (School of Stomatology, The Fourth Military Medical University) heeft een injecteerbare hybride anorganische (IHI) vastgesteld. stamcelassemblage met nanoscaffold-sjabloon en toegepast op de regeneratie van kraakbeendefecten van kritieke grootte.
Kraakbeenletsels zijn vaak verwoestend en de meeste zijn niet te genezen vanwege de intrinsiek lage regeneratiecapaciteit van kraakbeenweefsels. De opkomst van 3D-stamcelcultuursystemen heeft geleid tot doorbraken in ontwikkelingsbiologie, ziektemodellering en regeneratieve geneeskunde. Stamcellen kunnen bijvoorbeeld, eenmaal met succes getransplanteerd, in eerste instantie trofische factoren afscheiden voor het verminderen van ontstekingen op plaatsen van kraakbeenletsels en vervolgens differentiëren tot kraakbeencellen (bijv. chondrocyten) voor functioneel herstel.
Desalniettemin moeten er nog kritieke barrières worden overwonnen voordat het therapeutisch potentieel van stamceltherapieën kan worden gerealiseerd. De beperkte controle over de chondrogene differentiatie van stamcellen in vivo heeft vaak geresulteerd in gecompromitteerde regeneratieve resultaten. Bovendien ondergaan stamcellen, vanwege de prevalentie van oxidatieve stress en ontsteking in de micro-omgeving van verwondingsplaatsen, vaak apoptose na injectie.
Om deze uitdagingen aan te gaan, demonstreerden de onderzoekers de ontwikkeling van een 3D IHI nanoscaffold-template stamcelassemblagesysteem voor geavanceerde 3D-stamcelcultuur en implantatie. 3D-IHI nanoscaffold assembleert snel stamcellen tot injecteerbare weefselconstructies door middel van op maat gemaakte 3D-cel-cel- en cel-matrix-interacties, levert diep en homogeen chondrogene eiwitten in de geassembleerde 3D-kweeksystemen en induceert controleerbaar chondrogenese door middel van nanotopografische effecten.
Eenmaal in vivo geïmplanteerd in een konijnenkraakbeenletselmodel, moduleert 3D-IHI nanoscaffold effectief de dynamische micro-omgeving na kraakbeenletsel door de integratie van de bovengenoemde regeneratieve signalen, en verwijdert tegelijkertijd reactieve zuurstofsoorten met behulp van een op mangaandioxide gebaseerde samenstelling. Op deze manier wordt zowel op korte als lange termijn een versneld herstel van kraakbeendefecten met snelle weefselreconstructie en functioneel herstel gerealiseerd. Gezien de uitstekende veelzijdigheid en het therapeutische resultaat van op 3D-IHI nanoscaffold gebaseerde kraakbeenregeneratie, kan het veelbelovende middelen bieden om een verscheidenheid aan weefselmanipulatietoepassingen vooruit te helpen.
Het onderzoek is gepubliceerd in National Science Review .
-
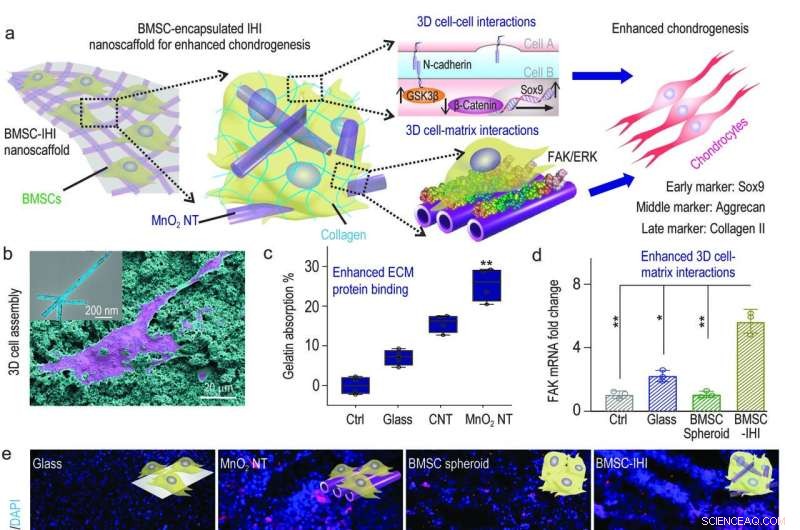
a) Een schematisch diagram dat de 3D-IHI nanoscaffold laat zien, zou de chondrogene differentiatie van BMSC kunnen verbeteren door een synergie tussen N-cadherine en FAK-gemedieerde routes. b) De sterke interacties tussen MnO2 NT's en functionele groepen die gewoonlijk in ECM-eiwitten voorkomen, ondersteunden effectief celhechting, zoals aangetoond via SEM-afbeelding. c) Bicinchoninezuurassay duidde op de verhoogde absorptie naar gelatine van MnO2 nanotube compared to control groups. d) The MnO2 nanotube-templated assembly method significantly enhanced cell-matrix interaction as demonstrated through the up-regulated expression patterns of the FAK gene. e) Representative immunostaining images showing the improved chondrogenesis of BMSC in the BMSC-IHI nanoscaffold group compared to the control groups. Scale bar:50 μm. f-h) The expression of chondrogenic genes, including SOX9 (f), Aggrecan (g), and Col-II (h) were characterized via qRT-PCR measurement. Credit:Science China Press
-
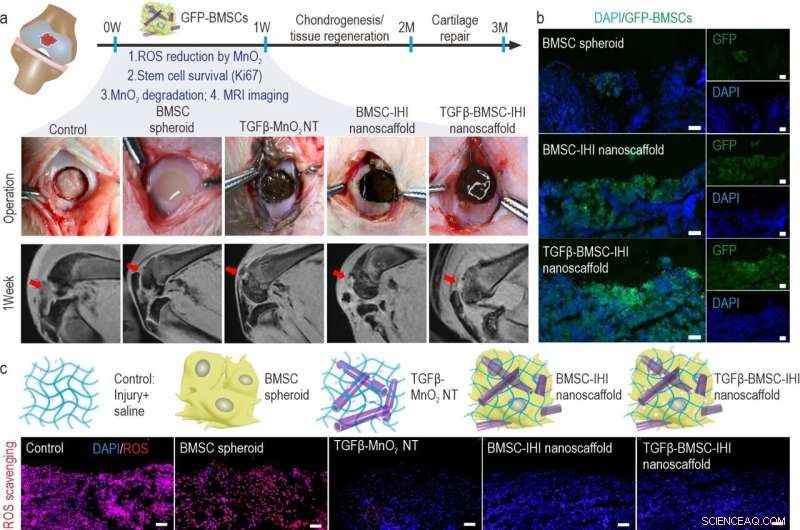
a) Schematic diagram illustrating the surgical process and timeline of cartilage repair. The degradation of MnO2 NTs and the regeneration process could be monitored via MRI. b) To identify our transplanted cells, BMSCs were genetically labeled with a green fluorescent protein (GFP). Scale bar:100 μm. c) The dramatically reduced red fluorescent signals of the ROS probe revealed that MnO2 NTs in the IHI nanoscaffold could effectively scavenge ROS in the defect area. Promoted cell proliferation was confirmed by the higher expression of proliferative marker Ki67 immunostaining. Scale bar:50 μm. d) The TGFβ-BMSC-IHI nanoscaffold could retain a significantly higher amount of cells after transplantation compared to other cell transplantation groups by quantifying the number of remaining GFP+ cells in (c). e) Histogram of the fluorescence intensity of ROS probe showed the effective consumption of ROS in the MnO2 NTs containing groups. f) Quantification of Ki67+ cells in the defects. The quantifications in (e) and (f) were generated based on the fluorescence intensities in (c). Credit:Science China Press
-
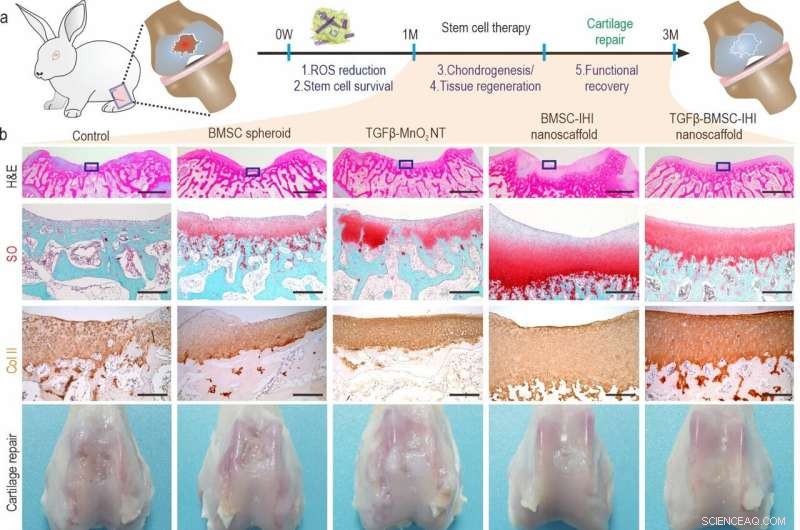
a) A schematic diagram illustrating the long-term (3 months) cartilage regeneration process. b) The in vivo cartilage regeneration was characterized through H&E, Safranin O staining, Col-II immunochemistry staining, as well as macroscopic views. Zoom out scale bar:2 mm, zoom in scale bar:200 μm. c-h) Quantifications of cartilage thickness (by H&E staining) (c), cellular components (by Safranin O staining) (d), ECM components (by Col II immunostaining) (e). Results of International Cartilage Repair Society (ICRS) macroscopic (f) and histologic scores (g) indicated significantly improved defect repair qualities in the TGFβ-BMSC-IHI nanoscaffold group. The reduced Osteoarthritis Research Society International (OARSI) scores revealed the TGFβ-BMSC-IHI nanoscaffold could prevent the deterioration of osteoarthritis (h). Credit:Science China Press
Discovery that TRPV4 gene regulates cartilage growth might yield future therapies for joint repair
 Wat is rodeoxideverf?
Wat is rodeoxideverf?  Wetenschapper vindt manier uit om kunstmatige fotosynthese op gang te brengen om lucht te zuiveren
Wetenschapper vindt manier uit om kunstmatige fotosynthese op gang te brengen om lucht te zuiveren Eenstapskatalysator zet nitraten om in water en lucht
Eenstapskatalysator zet nitraten om in water en lucht Hoogwaardige nitridehalfgeleider voor milieuvriendelijke fotovoltaïsche energie
Hoogwaardige nitridehalfgeleider voor milieuvriendelijke fotovoltaïsche energie Henneptestlab gelanceerd als antwoord op de behoefte van de industrie
Henneptestlab gelanceerd als antwoord op de behoefte van de industrie
 Biologische Vs. Chemische ongediertebestrijding
Biologische Vs. Chemische ongediertebestrijding  Tarieven van grote aardbevingen die niet worden beïnvloed door maanfasen, dag van het jaar
Tarieven van grote aardbevingen die niet worden beïnvloed door maanfasen, dag van het jaar Kaarten markeren steden in Michigan, groepen die het zwaarst zullen lijden onder de gevolgen van klimaatverandering
Kaarten markeren steden in Michigan, groepen die het zwaarst zullen lijden onder de gevolgen van klimaatverandering NASA-NOAA-satelliet vindt Barijat die Golf van Tonkin oversteekt
NASA-NOAA-satelliet vindt Barijat die Golf van Tonkin oversteekt Waterwegen van Chicago - die na meer dan 100 jaar nog steeds stromen
Waterwegen van Chicago - die na meer dan 100 jaar nog steeds stromen
Hoofdlijnen
- 10 planten verloren in de geschiedenis
- Een nieuwe kijk op toerisme en zijn bijdrage aan natuurbehoud in Nieuw-Zeeland
- Een keep-fit gadget voor uw hond deze kerst - wie heeft er echt baat bij?
- Onderzoekers vinden lage genetische diversiteit bij gedomesticeerde fretten
- Hoe raden werkt
- Genetische veranderingen helpen muggen om aanvallen van pesticiden te overleven
- Hoop voor honden met de meest voorkomende hart- en vaatziekten
- Onderzoekers lokaliseren genetische mutatie bij chronische nachtbrakers
- Waarom wordt natrium gebruikt in DNA-extractie?
- Onderzoekers creëren veelzijdige 3D-nanostructuren met behulp van DNA-stenen (met video)

- Nieuwe techniek maakt het makkelijker om halfgeleiders te etsen

- Waarom zijn gelegeerde metalen nanodeeltjes beter dan monometalen voor CNT-groei?
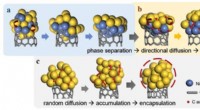
- Laserlicht op bruikbare golflengten van halfgeleider nanodraden

- Ultradunne lens kan een revolutie teweegbrengen in apparaten van de volgende generatie

 Het coronavirus het hoofd bieden met gedragseconomie
Het coronavirus het hoofd bieden met gedragseconomie Schoolprojecten: Elektrisch project
Schoolprojecten: Elektrisch project  Berkeley Labs CAMERA leidt internationale inspanningen voor autonome wetenschappelijke ontdekkingen
Berkeley Labs CAMERA leidt internationale inspanningen voor autonome wetenschappelijke ontdekkingen Oproep voor Australië om een nulvervuilingsdoel te stellen
Oproep voor Australië om een nulvervuilingsdoel te stellen Mensen vertrouwen te veel op virtuele assistenten
Mensen vertrouwen te veel op virtuele assistenten Rook van bosbranden verandert drastisch naarmate het ouder wordt, en dat is belangrijk voor de luchtkwaliteit benedenwinds
Rook van bosbranden verandert drastisch naarmate het ouder wordt, en dat is belangrijk voor de luchtkwaliteit benedenwinds Hoe toeristische bestemmingen weer kunnen opbouwen na het coronavirus
Hoe toeristische bestemmingen weer kunnen opbouwen na het coronavirus Stadia van een vulkaanuitbarsting
Stadia van een vulkaanuitbarsting
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

