
Wetenschap
Wetenschappers gebruiken lipide-nanodeeltjes om genbewerking precies op de lever te richten
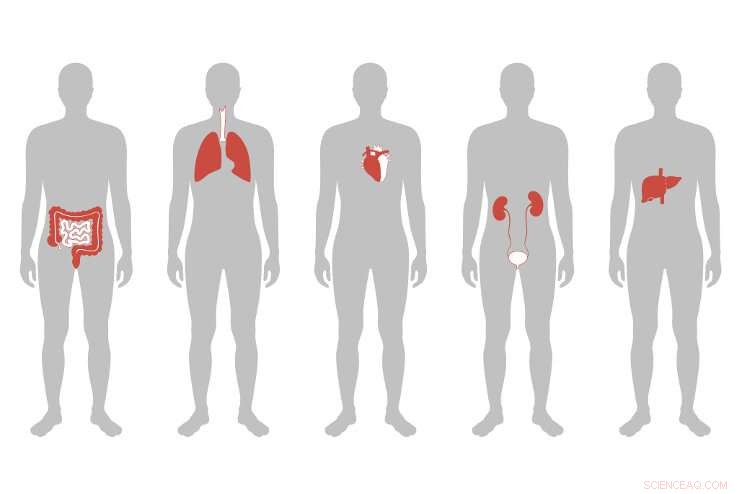
Onderzoekers ontwikkelden nanodeeltjes die een genbewerkingspakket specifiek naar de lever bij muizen dragen, met succes de niveaus van LDL "slechte" cholesterol in het bloed verlagen. Samen met eerdere studies die afgifte aan de hersenen of T-cellen aantonen, suggereren ze een toekomstige mogelijkheid van zeer gerichte therapieën voor het bewerken van genen. Krediet:Tufts University
De genoombewerkingstechnologie CRISPR is naar voren gekomen als een krachtig nieuw hulpmiddel dat de manier waarop we ziekten behandelen kan veranderen. De uitdaging bij het veranderen van de genetica van onze cellen, echter, is hoe het veilig te doen, effectief, en specifiek gericht op het gen, weefsel en orgaan dat behandeling nodig heeft. Wetenschappers van Tufts University en het Broad Institute of Harvard en MIT hebben unieke nanodeeltjes ontwikkeld die bestaan uit lipiden - vetmoleculen - die machines voor het bewerken van genen kunnen verpakken en specifiek aan de lever kunnen leveren. In een onderzoek dat vandaag is gepubliceerd in de Proceedings van de National Academy of Sciences , ze hebben aangetoond dat ze de lipidenanodeeltjes (LNP's) kunnen gebruiken om de CRISPR-machinerie efficiënt in de lever van muizen te brengen, wat resulteert in specifieke genoombewerking en een verlaging van het cholesterolgehalte in het bloed met maar liefst 57% - een verlaging die met slechts één injectie minstens enkele maanden kan aanhouden.
Het probleem van hoog cholesterol plaagt meer dan 29 miljoen Amerikanen, volgens de Centers for Disease Control and Prevention. De aandoening is complex en kan afkomstig zijn van meerdere genen, evenals van voedings- en levensstijlkeuzes, dus het is niet gemakkelijk te behandelen. De Tufts en Broad onderzoekers, echter, één gen hebben gemodificeerd dat een beschermend effect zou kunnen hebben tegen verhoogd cholesterol als het kan worden uitgeschakeld door genbewerking.
Het gen waar de onderzoekers zich op richtten codeert voor het angiopoietine-achtige 3 enzym (Angptl3). Dat enzym remt de activiteit van andere enzymen - lipasen - die helpen bij het afbreken van cholesterol. Als onderzoekers het Angptl3-gen kunnen uitschakelen, ze kunnen de lipasen hun werk laten doen en het cholesterolgehalte in het bloed verlagen. Het blijkt dat sommige gelukkige mensen een natuurlijke mutatie hebben in hun Angptl3-gen, wat leidt tot constant lage niveaus van triglyceriden en lipoproteïne met lage dichtheid (LDL), gewoonlijk "slechte" cholesterol genoemd, in hun bloedbaan zonder enige bekende klinische nadelen.
"Als we die aandoening kunnen repliceren door het angptl3-gen in anderen uit te schakelen, we hebben een goede kans op een veilige en langdurige oplossing voor een hoog cholesterolgehalte, " zei Qiaobing Xu, universitair hoofddocent biomedische technologie aan de Tufts' School of Engineering en corresponderende auteur van de studie. "We moeten er alleen voor zorgen dat we het genbewerkingspakket specifiek aan de lever leveren om geen ongewenste bijwerkingen te veroorzaken."
Het team van Xu was in staat om precies dat te doen in muismodellen. Na een enkele injectie van lipidenanodeeltjes verpakt met mRNA dat codeert voor CRISPR-Cas9 en een enkelvoudig RNA gericht op Angptl3, ze zagen een sterke verlaging van het LDL-cholesterol met maar liefst 57% en de triglyceridenspiegels met ongeveer 29%, die beide gedurende ten minste 100 dagen op die verlaagde niveaus bleven. De onderzoekers speculeren dat het effect veel langer kan aanhouden, misschien alleen beperkt door de langzame omzet van cellen in de lever, die zich over een periode van ongeveer een jaar kunnen voordoen. De verlaging van cholesterol en triglyceriden is dosisafhankelijk, zodat hun niveaus kunnen worden aangepast door minder of meer LNP's in de enkele opname te injecteren, aldus de onderzoekers.
Ter vergelijking, een bestaande, FDA-goedgekeurde versie van CRISPR mRNA-geladen LNP's kon LDL-cholesterol met maximaal 15,7% en triglyceriden met 16,3% verlagen toen het werd getest op muizen, volgens de onderzoekers.
De truc om een betere LNP te maken, was door de componenten aan te passen - de moleculen die samenkomen om bellen rond het mRNA te vormen. De LNP's bestaan uit lipiden met een lange keten die een geladen of polaire kop hebben die wordt aangetrokken door water, een koolstofkettingstaart die naar het midden van de bel wijst die de lading bevat, en een chemische linker daartussen. Ook aanwezig zijn polyethyleenglycol, en ja, zelfs wat cholesterol - dat een normale rol speelt in lipidemembranen om ze minder lekkend te maken - om hun inhoud beter vast te houden.
De onderzoekers ontdekten dat de aard en relatieve verhouding van deze componenten diepgaande effecten leken te hebben op de levering van mRNA in de lever, dus testten ze LNP's met veel combinaties van koppen, staarten, linkers en verhoudingen tussen alle componenten voor hun vermogen om levercellen te targeten. Omdat de in vitro potentie van een LNP-formulering zelden de in vivo prestatie weerspiegelt, ze evalueerden direct de leveringsspecificiteit en werkzaamheid bij muizen met een reportergen in hun cellen dat rood oplicht wanneer genoombewerking plaatsvindt. uiteindelijk, ze vonden een CRISPR mRNA-geladen LNP die alleen de lever verlichtte bij muizen, wat aantoont dat het specifiek en efficiënt hulpmiddelen voor het bewerken van genen in de lever kan brengen om hun werk te doen.
De LNP's werden voortgebouwd op eerder werk bij Tufts, waar Xu en zijn team LNP's ontwikkelden met een efficiëntie van maar liefst 90% bij het afleveren van mRNA in cellen. Uniek aan die nanodeeltjes was de aanwezigheid van disulfidebindingen tussen de lange lipideketens. Buiten de cellen, de LNP's vormen een stabiele bolvormige structuur die hun inhoud vergrendelt. Als ze zich in een cel bevinden, de omgeving binnenin verbreekt de disulfidebindingen om de nanodeeltjes uit elkaar te halen. De inhoud wordt dan snel en efficiënt in de cel afgegeven. Door verlies buiten de cel te voorkomen, de LNP's kunnen een veel hogere opbrengst hebben bij het leveren van hun inhoud.
"CRISPR is een van de krachtigste therapeutische hulpmiddelen voor de behandeling van ziekten met een genetische etiologie. We hebben onlangs het eerste klinische spoor bij mensen gezien voor CRISPR-therapie, mogelijk gemaakt door LNP-toediening die systemisch kan worden toegediend om genen in het menselijk lichaam te bewerken. Onze LNP hier ontwikkeld platform biedt een groot potentieel voor klinische vertaling, " zei Min Qiu, postdoctoraal onderzoeker in Xu's lab in Tufts. "We stellen ons voor dat met dit LNP-platform in de hand, we zouden nu van CRISPR een praktische en veilige benadering kunnen maken voor de behandeling van een breed spectrum van leverziekten of -aandoeningen, " zei Zachary Glass, afgestudeerde student in het Xu-lab. Qiu en Glass zijn co-eerste auteurs van de studie.
 Cryo-elektronenmicroscopie bereikt ongekende resolutie met behulp van nieuwe rekenmethoden
Cryo-elektronenmicroscopie bereikt ongekende resolutie met behulp van nieuwe rekenmethoden Hoe negatieve ionen te meten
Hoe negatieve ionen te meten Halogeenbinding-gemedieerde metaalvrije gecontroleerde kationische polymerisatie
Halogeenbinding-gemedieerde metaalvrije gecontroleerde kationische polymerisatie Wetenschappers ontwikkelen elastische metalen staven om scoliose te behandelen
Wetenschappers ontwikkelen elastische metalen staven om scoliose te behandelen Nieuwe composietkatalysator belooft een kosteneffectieve conversie van ethanol naar vliegtuigbrandstof
Nieuwe composietkatalysator belooft een kosteneffectieve conversie van ethanol naar vliegtuigbrandstof
 Het verhaal van Rum Jungle:een uraniummijn uit de Koude Oorlog die al tientallen jaren zuur in het milieu spuwt
Het verhaal van Rum Jungle:een uraniummijn uit de Koude Oorlog die al tientallen jaren zuur in het milieu spuwt Uit onderzoek blijkt dat er meerdere voedingsstoffen nodig zijn om fytoplankton te laten gedijen
Uit onderzoek blijkt dat er meerdere voedingsstoffen nodig zijn om fytoplankton te laten gedijen Hoeveel wormen eet een babyvogel?
Hoeveel wormen eet een babyvogel?  De aarde verliest zijn vuurkracht
De aarde verliest zijn vuurkracht Assimilatie van FY-3-gegevens bij het Met Office
Assimilatie van FY-3-gegevens bij het Met Office
Hoofdlijnen
- Pesticiden kunnen ervoor zorgen dat hommels hun buzz verliezen, studie vondsten
- Waar is mensenhaar van gemaakt?
- Dieetbeperking en levensduur bij mannelijke en hermafrodiete wormen
- Disruptieve bio-engineering - verandert de manier waarop cellen met elkaar omgaan
- Is het ethisch om stamcellen te gebruiken?
- Wat is opsomming in de microbiologie?
- Chimpansees bleken arm- en monduitdrukkingen te gebruiken om afstand over te brengen
- Waar vindt ademhaling plaats?
- Wat is de relatie tussen genetische manipulatie en DNA-technologie?
- Nieuw apparaat slaat elektriciteit op op siliciumchips

- Wetenschappers schalen terahertz-pieken in nanobuisjes
- Fluor geeft wit grafeen nieuwe krachten:onderzoekers veranderen gewone isolator in een magnetische halfgeleider
- Nanospace-gecontroleerd goudmateriaal gemaakt met behulp van moleculaire technologie
- Hoge lichtgevoeligheid 2-D-paar-gelaagde molybdeendiselenide fototransistors

 Stroomstoring:hoe een winterstorm Texas in een crisis dreef?
Stroomstoring:hoe een winterstorm Texas in een crisis dreef? Een geschiedenis van Afrikaans stof
Een geschiedenis van Afrikaans stof Jongeren gaan de straat op voor het klimaat:wie zijn ze?
Jongeren gaan de straat op voor het klimaat:wie zijn ze? Waarom zijn knaagdieren zulke populaire proefpersonen?
Waarom zijn knaagdieren zulke populaire proefpersonen?  Licht biedt controle voor 3D-printen met meerdere materialen
Licht biedt controle voor 3D-printen met meerdere materialen El Nino vervaagt, dus voorspellers verwachten een drukker orkaanseizoen
El Nino vervaagt, dus voorspellers verwachten een drukker orkaanseizoen AI-aangedreven avatar op technische show aangeprezen als kunstmatige mens
AI-aangedreven avatar op technische show aangeprezen als kunstmatige mens Presentatie van succesvolle STEM-prestaties van vrouwen, een sociaal vaccin tegen genderstereotypen
Presentatie van succesvolle STEM-prestaties van vrouwen, een sociaal vaccin tegen genderstereotypen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- Italian | Spanish | Portuguese | Swedish | Dutch | Danish | Norway | French | German |

-
Wetenschap © https://nl.scienceaq.com

