
Wetenschap
DNA-nanostructuren zijn geschikt voor toekomstige missies

De onderzoekers verzamelden drie verschillende DNA-nanostructuren, inclusief een C-vormige en twee tonachtige structuren, en toonden met transmissie-elektronenmicroscopie aan dat ze werden beschermd door hun gecombineerde coating- en verknopingsstrategie. Krediet:Wyss Institute aan de Harvard University
Het verslaan van kanker en een overvloed aan andere ziekten hangt niet alleen af van het verkrijgen van de juiste medicijnen, het gaat er ook om ze op de juiste plaatsen in het lichaam te krijgen, terwijl schade aan gezonde weefsels tot een minimum beperkt blijft. DNA-nanostructuren zoals zelf-assemblerende DNA-origami die zich in gedefinieerde vormen vouwen, zijn veelbelovende voertuigen voor de levering van medicijnen en diagnostiek, en verschillende vaccinatiestrategieën. Dit komt omdat ze flexibel kunnen worden gefunctionaliseerd met kleine moleculen en eiwitgeneesmiddelen, en immunogene antigenen, evenals functies die hun levering aan specifieke doelcellen en weefsels vergemakkelijken. In aanvulling, ze zijn biocompatibel en biologisch afbreekbaar.
Het grote potentieel van DNA-nanostructuren voor diverse biomedische toepassingen, echter, wordt nog steeds gehinderd door hun beperkte stabiliteit in de weefsels en het bloed van het lichaam. William Shih, doctoraat en zijn team hebben nu een eenvoudig, effectief, en schaalbare chemische crosslinking-benadering die DNA-nanostructuren de stabiliteit kan bieden die ze nodig hebben als leveringsvehikels voor medicijnen en diagnostiek. Hun studie is gepubliceerd in de Tijdschrift van de American Chemical Society ( JACS ).
"Om de buitengewone belofte van DNA-nanostructuren te helpen vervullen, we ontwikkelden een breed toepasbare chemische aanpak om hun weerstand tegen afbraak te vergroten, " zei William Shih, een lid van de kernfaculteit van het Wyss Institute die het project leidt in het Molecular Robotics Initiative van het Instituut. "Door DNA-nanostructuren in twee eenvoudige stappen aan te passen, kunnen we hun overleving drastisch verbeteren, wat een centraal knelpunt wegneemt bij de vertaling van die nanodevices naar oplossingen voor allerlei medische problemen."
DNA-origami wordt meestal samengesteld uit een lange DNA-streng die zich in een gedefinieerde 3D-vorm op de schaal van nanometers vouwt met behulp van meerdere korte stapelstrengen die verschillende delen van de structuur in de ruimte verbinden. De DNA-ruggengraat is sterk negatief geladen, wat betekent dat het moeilijk kan zijn om verschillende delen van de vouwstrengen bij elkaar te brengen omdat ze elkaar van nature afstoten, vergelijkbaar met de negatieve oppervlakken van twee magneten. Om deze afstotende krachten te overwinnen, onderzoekers voegen vaak een overmaat aan positief geladen ionen toe, zoals magnesiumionen (Mg 2 + ) op hun vouwreacties die de negatieve ladingen van DNA afdekken.
Vaak, echter, de toegevoegde Mg 2 + ionen worden niet voldoende gehandhaafd in origamistructuren van 3D-DNA. Vooral wanneer geïntroduceerd in het lichaam, waar normaal Mg 2 + concentraties zijn veel lager, Mg 2 + ionen lekken uit de nanostructuren en zorgen ervoor dat ze uiteenvallen. In aanvulling, DNA-nanostructuren worden constant aangevallen door DNA-nuclease-enzymen die van nature in het lichaam worden geproduceerd en vrije DNA-moleculen afbreken, hun stabiliteit drastisch verminderen, die gewoonlijk wordt gemeten als hun halfwaardetijd. Hieruit volgt logischerwijs dat door de structurele integriteit van DNA-nanostructuren te verstoren, deze interne en externe krachten beperken ook de afgifte van medicijnen of de beschikbaarheid van diagnostische reportermoleculen.
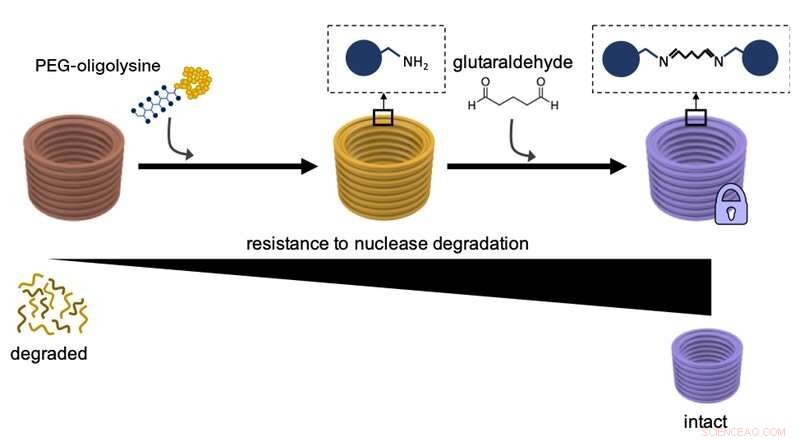
Dit diagram legt uit hoe DNA-nanostructuren eerst worden gecoat met PEG-oligolysines, en het vervolgens chemisch verknopen van verschillende PEG-oligolysines met glutaaraldehyde als verknopingsmiddel verhoogt hun weerstand tegen afbraak door DNA-nuclease-enzymen en verhoogt de algehele stabiliteit. Krediet:Wyss Institute aan de Harvard University
In een eerdere studie, Shih en zijn team hebben een manier gevonden om de behoefte aan overmatige Mg . te overwinnen 2 + concentraties om DNA-nanostructuren te stabiliseren. Door de oppervlakken van de grote DNA-strengen in wezen te coaten met een relatief klein onopvallend neutraliserend middel dat meerdere positieve ladingen draagt en bekend staat als PEG-oligolysine (of gePEGyleerd oligolysine), ze hadden een methode uitgevonden die gemakkelijk kon worden toegepast om DNA-nanostructuren in alle vormen en vormen op een schaalbare manier te stabiliseren. GePEGyleerd oligolysine bestaat uit korte ketens van het positief geladen aminozuur lysine - een van de bouwstenen van eiwitten - die stevig vastzitten aan polyethyleenglycol (PEG), een polymeer molecuul dat meerdere oligolysineketens kan binden. De onderzoekers denken dat PEG functioneert als een "moleculaire borstel" om aggregatie van de geneutraliseerde nanodeeltjes te voorkomen.
In tegenstelling tot individuele Mg 2 + ionen die, in theorie, elk kan slechts twee van de vele negatieve ladingen neutraliseren die door de DNA-ruggengraat worden blootgelegd met hun twee positieve ladingen, GePEGyleerd oligolysine kan meerdere negatieve DNA-ladingen tegelijk afdekken, en vormt zo een stabiel "elektrostatisch net" dat het oppervlak van DNA-nanostructuren bedekt. De stabiliteit van de gecoate nanostructuren bleef zelfs behouden in levende cellen en muizen, bewijzen dat het team op de goede weg was.
"Met deze eenvoudige strategie, we zouden de overleving van DNA-nanostructuren met ongeveer 400-voudig kunnen verlengen met halfwaardetijden tot 36 uur in fysiologische omgevingen die ook normale nucleaseniveaus bevatten, " zei eerste auteur Frances Anastassacos, doctoraat, die op het moment van de studie een afgestudeerde student was die met Shih werkte. "Echter, dit voldeed nog steeds niet aan wat nodig is in sommige daadwerkelijke therapeutische toepassingen. GePEGyleerd oligolysine had nog steeds de neiging om tot op zekere hoogte van het DNA af te vallen."
In de JACS studie, het team heeft nu dit resterende deel van het 'stabiliteitsprobleem' opgelost. "We hebben in wezen extra knopen in het elektrostatische net gelegd met behulp van een chemisch verknopingsreagens dat bekend staat als 'glutaraldehyde' dat verschillende gePEGyleerde oligolysines op het oppervlak van DNA-nanostructuren sterk bindt, " zei Anastassacos. "In de aanwezigheid van DNA-nucleaseniveaus die veel hoger zijn dan die in het menselijk lichaam, hun overleving verlengd tot meer dan 300 uur. De 400-voudige toename in stabiliteit die we met alleen gePEGyleerd oligolysine waarnamen, was nog eens 250-voudig verhoogd, wat een schot in de roos is voor klinische toepassingen."
Andere pogingen die erin slaagden om DNA-nanostructuren met chemische modificaties te stabiliseren, waren meestal gebaseerd op het herontwerp van bestaande structuren, zodat specifieke locaties binnen hun 3D-structuren toegankelijk zouden worden voor de ingezette chemie. In tegenstelling tot, "onze aanpak kan worden uitgevoerd op elke DNA-nanostructuur, en het gemak en de kosteneffectiviteit ervan zouden de vertaling van veel reeds bestaande en nieuw ontworpen therapeutische en diagnostische structuren aanzienlijk kunnen versterken, " zei Zhao Zhao, doctoraat, die een co-eerste auteur is van de studie en voormalig postdoctoraal onderzoeker in het team van Shih.
In hun studie hebben Shih en zijn team streefden naar het maximaliseren van de stabiliteit van DNA-nanostructuren. De onderzoekers, echter, denk dat door de verknopingsstap verder te variëren, de halfwaardetijd van de structuren kan worden afgestemd op specifieke toepassingen waarbij ladingmoleculen op verschillende tijdstippen en met verschillende tijdsintervallen beschikbaar moeten komen. Ze ontdekten al dat hun beschermingsmethode niet interfereerde met de binding van ladingmoleculen aan de gemodificeerde structuren en de opname van de structuren door gekweekte menselijke cellen. Nutsvoorzieningen, klinische vertaling kan beginnen.
 Enge opwarming bij palen die op rare tijden verschijnen, plaatsen
Enge opwarming bij palen die op rare tijden verschijnen, plaatsen Hel en ijswater:het smelten van gletsjers bedreigt de toekomst van Pakistan
Hel en ijswater:het smelten van gletsjers bedreigt de toekomst van Pakistan Australië slaagt er niet in om Great Barrier Reef te beschermen:activisten
Australië slaagt er niet in om Great Barrier Reef te beschermen:activisten Orkaanseizoen in combinatie met COVID-19-pandemie kan perfecte storm veroorzaken
Orkaanseizoen in combinatie met COVID-19-pandemie kan perfecte storm veroorzaken Afbeelding:Ries-krater, Duitsland
Afbeelding:Ries-krater, Duitsland
Hoofdlijnen
- Wanneer één referentiegenoom niet genoeg is
- Nieuwe bevindingen uit onderzoek naar kunstmatige selectie wijzen op een bedreiging voor mariene omgevingen
- Onderzoeksgroep ontdekt de oorsprong van octopussen onmiddellijke modulatie van lichaamskleuring
- Iran verhuist om laatste mascotte Aziatische cheeta's te redden
- Onderzoek toont aan dat plantengroeiregulatoren gunstig kunnen zijn voor de vestiging van uien, productie
- Wat is de formule voor cellulaire ademhaling?
- Wat zijn fysieke kenmerken die worden doorgegeven van ouders?
- Hands-on Science-activiteiten over bloed
- Stamcelplatform werpt nieuw licht op het begin van menselijke ontwikkeling
- Kunnen we meer goedaardige nanomaterialen vinden?
- Wetenschappers ontdekken hoe ze de excitatie van elektronica kunnen beheersen

- Verbandmateriaal helpt het bloeden te stoppen zonder aan de wond te hechten

- Onderzoekers zoeken naar manier om zonnecellen ultradun te maken, flexibel

- Licht schakelen met een zilveratoom

 Wat is het verschil tussen vijgen en pruimen?
Wat is het verschil tussen vijgen en pruimen?  Kan draadloze uitdagingskabel voor thuisinternetservice?
Kan draadloze uitdagingskabel voor thuisinternetservice? Strategisch doel Texas voor schuldenlast van studenten toont potentiële belofte en valkuilen
Strategisch doel Texas voor schuldenlast van studenten toont potentiële belofte en valkuilen Hoe Erosiesnelheid te berekenen
Hoe Erosiesnelheid te berekenen Klimaatmysteries stellen wetenschappers nog steeds voor raadsels, ondanks vooruitgang
Klimaatmysteries stellen wetenschappers nog steeds voor raadsels, ondanks vooruitgang Olie-etende bacteriën kunnen helpen morsen aan te pakken
Olie-etende bacteriën kunnen helpen morsen aan te pakken Kwantumeffecten helpen communicatiefouten te minimaliseren
Kwantumeffecten helpen communicatiefouten te minimaliseren Ammoniak op aanvraag? Alternatieve productiemethode voor een duurzame toekomst
Ammoniak op aanvraag? Alternatieve productiemethode voor een duurzame toekomst
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

