
Wetenschap
Voorgestelde kwantum nano-MRI zou afbeeldingen kunnen genereren met een resolutie op angstrom-niveau
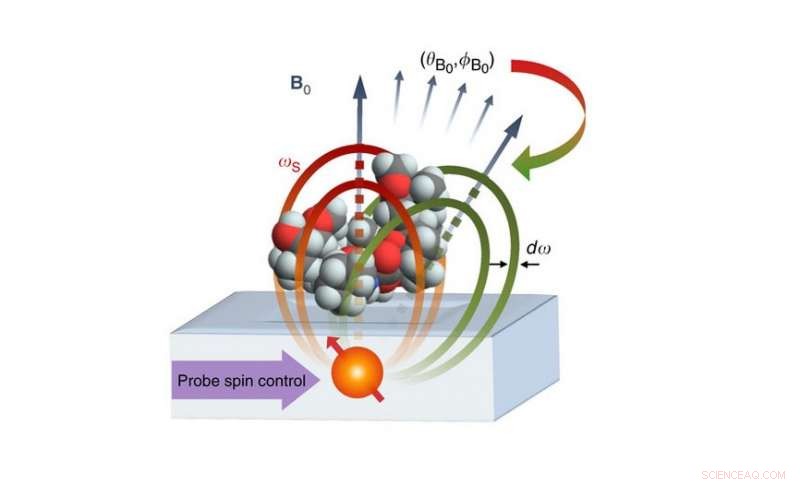
De voorgestelde nano-MRI-opstelling bestaat uit een atomaire qubit die 2-4 nm onder een oppervlak is gepositioneerd dat een molecuul bevat. De qubit fungeert als zowel de sensor als de bron van het magnetische veld voor het coderen van de kernspins van het molecuul. De gegevens over de nucleaire dichtheid worden vervolgens gebruikt om een 3D-beeld van de moleculaire structuur te genereren met een resolutie op angstrom-niveau. Krediet:Perunicic et al., Natuurcommunicatie
(Phys.org)—Vergelijkbaar met de manier waarop een conventionele MRI-machine (magnetic resonance imaging) grote magneten gebruikt om 3D-beelden te genereren, natuurkundigen hebben een voorstel ontwikkeld voor een kwantum nano-MRI-machine die de magnetische eigenschappen van een enkele atomaire qubit zou gebruiken om 3D-beelden te genereren met een resolutie van angstrom (0,1 nanometer). De nieuwe techniek zou kunnen leiden tot de ontwikkeling van één-molecuulmicroscopen voor het afbeelden van biomoleculen, met toepassingen in de ontdekking van geneesmiddelen en een beter begrip van ziekten.
De onderzoekers, onder leiding van Lloyd Hollenberg, hoogleraar natuurkunde aan de Universiteit van Melbourne, hebben een paper over de nieuwe techniek gepubliceerd in een recent nummer van Natuurcommunicatie .
"Continue wetenschappelijke vooruitgang in de afgelopen decennia hebben ons in staat gesteld om veel medische problemen op macroscopische schaal te begrijpen en daarom te genezen, bijvoorbeeld botbreuken of bloedstolsels, " vertelde hoofdauteur Viktor Perunicic van de Universiteit van Melbourne: Phys.org . "Echter, de ziekten waarmee de mensheid tegenwoordig wordt geconfronteerd, zijn microscopisch klein, omdat ze voortkomen uit storingen op moleculair niveau, bijvoorbeeld een eiwit met een misvormde vorm ergens in een cel. Kanker, suikerziekte, virale infecties en vele anderen hebben dit gemeen, maar op dit moment is er bijna geen middel om te zien wat er op dit niveau in ons lichaam gebeurt.
"In ons werk we willen dit probleem aanpakken door een blauwdruk te ontwikkelen voor technologie die direct 3D visueel inzicht kan geven in de atomaire structuur van individuele moleculen in hun cellulaire omgeving. We bereiken dit door gebruik te maken van kwantumcomputertechnologie in een concept dat magnetische resonantiebeeldvorming op atomaire schaal brengt."
Het voorgestelde beeldvormingssysteem bestaat uit een atomaire qubit die ongeveer 2 nanometer onder een oppervlak wordt geplaatst dat het af te beelden molecuul vasthoudt. De qubit fungeert als zowel de bron als de sensor van magnetische velden, met zijn kwantummagnetische eigenschappen (zijn spin) in wisselwerking met de magnetische eigenschappen van de atomen in het doelmolecuul. Door gegevens over deze interacties op verschillende oriëntaties te verzamelen, het systeem zou de posities van individuele atomen kunnen bepalen en een 3D-beeld van de structuur van het doelmolecuul kunnen construeren.
De wetenschappers simuleerden de nieuwe techniek met behulp van een rapamycinemolecuul (C 51 H 79 NEE 13 ), een immunosuppressivum dat vaak wordt gebruikt om afstoting van orgaantransplantaten te voorkomen. Bij conventionele beeldvormingstechnieken zoals röntgenkristallografie, het is moeilijk om de waterstofatomen te detecteren. Maar door de kernspindichtheid van waterstof te meten, de nano-MRI-methode kan 3D-beelden van de waterstofatomen genereren, evenals de koolstofatomen, met een gemiddelde beeldresolutie op angstrom-niveau.
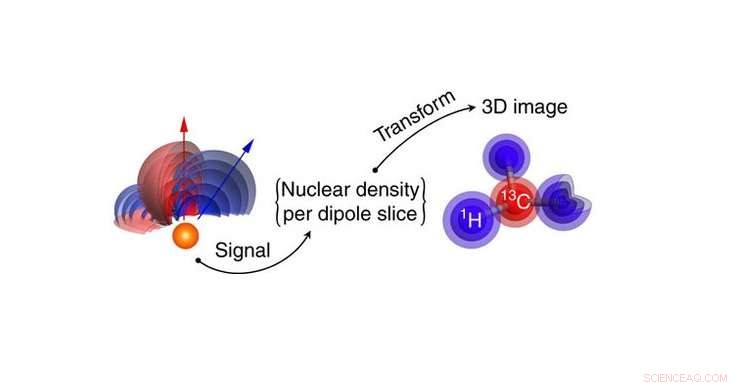
De kerndichtheid van het doelmolecuul wordt omgezet in een 3D-beeld van de kerndichtheid van waterstof- en koolstofatomen. Atoomposities worden direct uit de dichtheidsbeeldgegevens gehaald. Krediet:Perunicic et al., Natuurcommunicatie
"Het vermogen om de atomaire structuur van moleculen in hun oorspronkelijke cellulaire omgeving in beeld te brengen, is van vitaal belang voor zowel het begrijpen van de oorsprong van de ziekte als het vinden van de remedie, " zei Hollenberg. "Bijvoorbeeld, bij het zoeken en testen van nieuwe medicijnen zou men eerst een doelwit identificeren, vaak een membraaneiwit. Het in beeld brengen van de ware structuur van het eiwit in de cellulaire omgeving is essentieel om te begrijpen hoe medicijnmoleculen ermee zullen interageren. Op basis van deze informatie, een geneesmiddelmolecuul zou kunnen worden geselecteerd of ontworpen. belangrijk, hetzelfde beeldvormingsapparaat zou middelen verschaffen om te begrijpen en te testen hoe goed het medicijn werkt, door de interacties met het doelmolecuul op atomair niveau te observeren. Ons doel is om een veelzijdige technologie te ontwikkelen voor het observeren van de momenteel ontoegankelijke biochemische atomaire structuur van belangrijke moleculen in situ, op een manier die analoog is aan hoe MRI-machines in ziekenhuizen de anatomie van ons lichaam observeren."
Door de grote hoeveelheid gegevens die ermee gemoeid zijn, simulaties tonen aan dat de totale tijd om een afbeelding van het rapamycinemolecuul te genereren momenteel ongeveer 175 uur is. Echter, de onderzoekers verwachten dat toekomstige verbeteringen deze tijd sterk zullen verkorten, en de resolutie verder te verhogen. In de toekomst, ze zijn ook van plan om het systeemontwerp op te schalen voor het afbeelden van grotere biomoleculen.
"Tot nu toe heeft ons werk zich gericht op de fundamentele theoretische basis, begrijpen hoe het apparaat fysiek moet worden geconstrueerd met de momenteel beschikbare technologie, Perunicic zei. "We ontwikkelen de ingewikkelde kwantummechanische controle die het vermogen zou bieden om individuele moleculen in beeld te brengen, en voeren ook simulaties uit om de prestaties onder realistische omstandigheden te testen. Omdat de resultaten van deze onderzoeken bemoedigend waren, de natuurlijke richting voor de komende jaren is om experimentele proof-of-concept-demonstraties te ondernemen."
© 2016 Fys.org
 Ingenieurs maken de basisbouwsteen voor elektrospun nanovezels
Ingenieurs maken de basisbouwsteen voor elektrospun nanovezels Ontwerpbehandeling van geavanceerde metalen voor betere beeldhouwkunst
Ontwerpbehandeling van geavanceerde metalen voor betere beeldhouwkunst Onderzoekers ontwikkelen DNA-zonnebrandcrème die beter wordt naarmate je hem langer draagt
Onderzoekers ontwikkelen DNA-zonnebrandcrème die beter wordt naarmate je hem langer draagt Ontwikkeling van cellulaire membraan-FET (lipid-FET) voor gevoeligheid van biosensor
Ontwikkeling van cellulaire membraan-FET (lipid-FET) voor gevoeligheid van biosensor Metaalreducerende bacteriën bieden een groenere route voor de productie van koperkatalysatoren
Metaalreducerende bacteriën bieden een groenere route voor de productie van koperkatalysatoren
 Methaanlek zichtbaar vanuit de ruimte
Methaanlek zichtbaar vanuit de ruimte Wat voor soort vis is een Mahi Mahi?
Wat voor soort vis is een Mahi Mahi?  Nieuwe bevindingen werpen licht op de grote milieuverschuiving door het Midden-Eoceen in Zuid-China
Nieuwe bevindingen werpen licht op de grote milieuverschuiving door het Midden-Eoceen in Zuid-China Chili gaat toeristen en niet-inwoners op Paaseiland beperken
Chili gaat toeristen en niet-inwoners op Paaseiland beperken Video:Met klimaatverandering, zijn we als de walvis in The Hitchhikers Guide to the Galaxy?
Video:Met klimaatverandering, zijn we als de walvis in The Hitchhikers Guide to the Galaxy?
Hoofdlijnen
- Een Chromosome-diagram interpreteren
- Lijst van eencellige organismen
- Nieuwe studie werpt licht op hoe de vroegste vormen van leven op aarde zijn geëvolueerd
- Domme mensen zijn verrassend zelfverzekerd
- Afrika stroperij nu een oorlog, taskforce waarschuwt
- Groenlandse walvissen komen naar Cumberland Sound in Nunavut om te exfoliëren
- Wat zijn de functies van co-enzymen?
- Twee Caribische vogelvangbomen vernoemd naar twee vrouwen met over het hoofd gezien botanische werken
- De taal van cellulaire communicatie begrijpen
- Onderzoek toont aan dat grootte de structuur van holle nanodeeltjes beïnvloedt

- Ontwikkeling van geprinte elektronica met ultrahoge resolutie met behulp van dual-surface architecturen

- Ontdekking van de specifieke eigenschappen van op grafiet gebaseerde koolstofmaterialen

- De verwerking van big data energiezuiniger maken met magnetische circuits
- Nieuw op koolstof gebaseerd nanomateriaal:gemakkelijke diamantsynthese uit lagere diamandoïden
 Spin-kwantumnummer: definitie, hoe te berekenen en betekenis
Spin-kwantumnummer: definitie, hoe te berekenen en betekenis Op afstand bestuurde medicijnafgifte implantaatgrootte van druif kan helpen bij het beheer van chronische ziekten
Op afstand bestuurde medicijnafgifte implantaatgrootte van druif kan helpen bij het beheer van chronische ziekten Onderwaterseismometer kan horen hoe snel een gletsjer beweegt
Onderwaterseismometer kan horen hoe snel een gletsjer beweegt Samenzweringsovertuigingen kunnen de politieke betrokkenheid in de buitenwijken vergroten, toont nieuwe studie
Samenzweringsovertuigingen kunnen de politieke betrokkenheid in de buitenwijken vergroten, toont nieuwe studie Onderzoekers 3D printen minuscule veelkleurige microstructuren
Onderzoekers 3D printen minuscule veelkleurige microstructuren Sentinels bewaken convergerende ijsscheuren
Sentinels bewaken convergerende ijsscheuren Hoe maak je een Ocean Project uit een schoenendoos
Hoe maak je een Ocean Project uit een schoenendoos  Gebruikmaken van rijke satellietgegevens om de gewasopbrengst te schatten
Gebruikmaken van rijke satellietgegevens om de gewasopbrengst te schatten
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway | Italian |

-
Wetenschap © https://nl.scienceaq.com

