Wetenschap
IJzeren nanodeeltjes zorgen ervoor dat immuuncellen kanker aanvallen
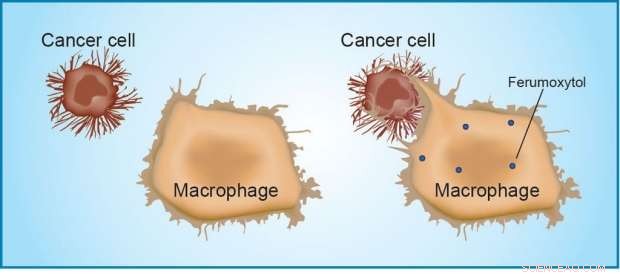
Een muisstudie wees uit dat ferumoxytol immuuncellen, genaamd tumor-geassocieerde macrofagen, ertoe aanzet om tumorcellen te vernietigen. Krediet:Amy Thomas
Stanford-onderzoekers ontdekten per ongeluk dat ijzeren nanodeeltjes die zijn uitgevonden voor de behandeling van bloedarmoede een ander doel hebben:het activeren van het vermogen van het immuunsysteem om tumorcellen te vernietigen.
IJzernanodeeltjes kunnen het immuunsysteem activeren om kankercellen aan te vallen, volgens een studie geleid door onderzoekers van de Stanford University School of Medicine.
De nanodeeltjes, die in de handel verkrijgbaar zijn als het injecteerbare ijzersupplement ferumoxytol, zijn goedgekeurd door de Food and Drug Administration om bloedarmoede door ijzertekort te behandelen.
Uit de muisstudie bleek dat ferumoxytol immuuncellen, de zogenaamde tumor-geassocieerde macrofagen, ertoe aanzet om kankercellen te vernietigen. wat suggereert dat de nanodeeltjes bestaande kankerbehandelingen zouden kunnen aanvullen. De vondst, beschreven in een paper online gepubliceerd op 26 september in Natuur Nanotechnologie , werd per ongeluk gemaakt tijdens het testen of de nanodeeltjes als Trojaanse paarden konden dienen door chemotherapie in tumoren bij muizen te sluipen.
"Het was echt verrassend voor ons dat de nanodeeltjes macrofagen activeerden, zodat ze kankercellen bij muizen begonnen aan te vallen, " zei Heike Daldrup-Link, MD, wie is de senior auteur van de studie en een universitair hoofddocent radiologie aan de School of Medicine. "We denken dat dit concept zou moeten gelden bij menselijke patiënten, te."
Het team van Daldrup-Link voerde een experiment uit met drie groepen muizen:een experimentele groep die nanodeeltjes kreeg geladen met chemo, een controlegroep die nanodeeltjes kreeg zonder chemo en een controlegroep die geen van beide kreeg. De onderzoekers deden de onverwachte observatie dat de groei van de tumoren bij controledieren die alleen nanodeeltjes kregen, werd onderdrukt in vergelijking met de andere controles.
Macrofagen weer op het goede spoor krijgen
De onderzoekers voerden een reeks vervolgtesten uit om te karakteriseren wat er gebeurde. Experimenteren met cellen in een schaaltje, ze toonden aan dat immuuncellen die tumor-geassocieerde macrofagen worden genoemd, nodig waren voor de antikankeractiviteit van de nanodeeltjes; in celculturen zonder macrofagen, de ijzeren nanodeeltjes hadden geen effect tegen kankercellen.
Voordat dit onderzoek werd gedaan, het was al bekend dat bij gezonde mensen, tumor-geassocieerde macrofagen detecteren en eten individuele tumorcellen. Echter, grote tumoren kunnen de tumor-geassocieerde macrofagen kapen, waardoor ze stoppen met aanvallen en in plaats daarvan beginnen met het afscheiden van factoren die de groei van de kanker bevorderen.
De studie toonde aan dat de ijzeren nanodeeltjes de macrofagen terugzetten naar hun kankeraanvallende staat, zoals blijkt uit het volgen van de producten van het metabolisme van de macrofagen en het onderzoeken van hun patronen van genexpressie.
Verder, in een muismodel van borstkanker, de onderzoekers toonden aan dat het ferumoxytol de tumorgroei remde wanneer het in doses werd gegeven, aangepast voor lichaamsgewicht, vergelijkbaar met die goedgekeurd door de FDA voor de behandeling van bloedarmoede. Eerdere studies hadden aangetoond dat de nanodeeltjes worden gemetaboliseerd over een periode van ongeveer zes weken, en de nieuwe studie toonde aan dat het antikankereffect van een enkele dosis nanodeeltjes gedurende ongeveer drie weken afnam.
De wetenschappers testten ook of de nanodeeltjes de verspreiding van kanker konden stoppen. In een muismodel van kleincellige longkanker, de nanodeeltjes verminderden de tumorvorming in de lever, een veel voorkomende plaats van metastase bij zowel muizen als mensen. In een apart model van levermetastase, voorbehandeling met nanodeeltjes voordat tumorcellen werden geïntroduceerd, verminderde het volume van levertumoren aanzienlijk.
Potentiële klinische toepassingen
De resultaten van de studie suggereren verschillende mogelijke toepassingen om te testen in menselijke proeven, aldus Daldrup-Link. Bijvoorbeeld, na een operatie om een mogelijk uitgezaaide tumor te verwijderen, patiënten hebben vaak chemotherapie nodig, maar moeten wachten tot ze herstellen van de operatie om de ernstige bijwerkingen van conventionele chemo te verdragen. De ijzeren nanodeeltjes missen de toxische bijwerkingen van chemotherapie, wat suggereert dat ze aan patiënten kunnen worden gegeven tijdens de chirurgische herstelperiode.
"We denken dat dit de tijd kan overbruggen dat de patiënt behoorlijk ziek is na de operatie, en helpen voorkomen dat de kanker zich verspreidt totdat ze chemotherapie kunnen krijgen, zei Daldrup-Link.
De nanodeeltjes kunnen ook kankerpatiënten helpen van wie de tumoren niet volledig kunnen worden verwijderd. "Als er na de operatie nog wat tumorcellen over zijn, de situatie die kankerchirurgen positieve marges noemen, we denken dat het zou kunnen werken om daar ijzeren nanodeeltjes te injecteren, en de kleinere tumorzaden kunnen mogelijk worden opgevangen door ons immuunsysteem, " zei Daldrup-Link.
Het feit dat de nanodeeltjes al door de FDA zijn goedgekeurd, versnelt het vermogen om deze toepassingen bij mensen te testen, voegde ze eraan toe.
De nieuwe bevindingen zullen kankeronderzoekers ook helpen nauwkeurigere evaluaties uit te voeren van combinaties van nanodeeltjes en geneesmiddelen, aldus Daldrup-Link. "In veel onderzoeken onderzoekers beschouwen nanodeeltjes gewoon als vehikels voor medicijnen, " zei ze. "Maar ze kunnen verborgen intrinsieke effecten hebben die we niet zullen waarderen tenzij we naar de nanodeeltjes zelf kijken."
 Kunnen luminescente zonneconcentratoren zonne-energie betaalbaarder maken?
Kunnen luminescente zonneconcentratoren zonne-energie betaalbaarder maken?  Computervideosimulatie kan overstromingen beperken
Computervideosimulatie kan overstromingen beperken Canadese oliestijging zet Trudeau klimaatactie in twijfel
Canadese oliestijging zet Trudeau klimaatactie in twijfel Onderzoekers creëren definitieve methode om door bosbranden besmette wijndruiven te detecteren
Onderzoekers creëren definitieve methode om door bosbranden besmette wijndruiven te detecteren Volgens de weersvoorspelling zou het 90 graden zijn. Dus waarom zegt je thermometer dat het 100 is?
Volgens de weersvoorspelling zou het 90 graden zijn. Dus waarom zegt je thermometer dat het 100 is?
Hoofdlijnen
- Animal Cell Shoe Box Project
- Onderzoek verduidelijkt de functie van de nucleaire hormoonreceptor in planten
- Is er een psychologische reden waarom mensen gemeen zijn op internet?
- Wetenschappers nemen de temperatuur van knokkelkoorts risico
- P53 (TP53) Tumor Protein: Function, Mutation
- Manitobas goudvleugelzangers:'s werelds laatste pure populatie die wordt geraakt door lokale en verre instandhoudingsproblemen
- Fokresistente kippen voor verbeterde voedselveiligheid
- Vroegtijdige waarschuwing gezondheids- en welzijnssysteem kan boeren miljoenen ponden besparen
- Vier klassen van macromoleculen belangrijk voor levende dingen
 Britse ruimtevaartfunctionarissen zoeken handige naam voor Marsrover
Britse ruimtevaartfunctionarissen zoeken handige naam voor Marsrover Welke metalen reageren met water om waterstof te produceren?
Welke metalen reageren met water om waterstof te produceren?  Terwijl aanvalsdrones zich vermenigvuldigen, Israëlische bedrijven ontwikkelen verdedigingswerken
Terwijl aanvalsdrones zich vermenigvuldigen, Israëlische bedrijven ontwikkelen verdedigingswerken Het afsluiten van sociale media vermindert het geweld niet, maar voedt het eerder
Het afsluiten van sociale media vermindert het geweld niet, maar voedt het eerder Hugo, ik en iedereen:Doe mee aan de oorlog tegen plasticvervuiling
Hugo, ik en iedereen:Doe mee aan de oorlog tegen plasticvervuiling Soorten lijken bedrieglijk veerkrachtig tegen klimaatverandering
Soorten lijken bedrieglijk veerkrachtig tegen klimaatverandering Hoe Yards in Feet
Hoe Yards in Feet Amerikaanse regelgevers zullen Boeing dwingen 737 MAX-jets opnieuw te bedraden:rapport
Amerikaanse regelgevers zullen Boeing dwingen 737 MAX-jets opnieuw te bedraden:rapport
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com