
Wetenschap
Microscopische medicijndepots verhogen de werkzaamheid tegen tumoren in diermodel

Onderzoekers op het gebied van biomedische technologie hebben een techniek ontwikkeld voor het creëren van microscopische "depots" voor het opsluiten van medicijnen in kankertumoren. In een diermodel, deze medicijndepots waren 10 keer effectiever in het verkleinen van tumoren dan het gebruik van dezelfde medicijnen zonder de depots. Krediet:Quanyin Hu
Onderzoekers op het gebied van biomedische technologie hebben een techniek ontwikkeld voor het creëren van microscopische "depots" voor het opsluiten van medicijnen in kankertumoren. In een diermodel, deze medicijndepots waren 10 keer effectiever in het verkleinen van tumoren dan het gebruik van dezelfde medicijnen zonder de depots.
Sommige geneesmiddelen tegen kanker zijn het meest effectief buiten kankercellen. Bijvoorbeeld, het antikankergeneesmiddel TRAIL valt het celmembraan van een kankercel aan, terwijl een ander medicijn, cilengitide, remt de groei van bloedvaten rond een tumor, het uithongeren van voedingsstoffen.
Om de effectiviteit van deze medicijnen te verbeteren, wetenschappers willen zowel voorkomen dat ze worden opgenomen in de kankercellen als voorkomen dat ze door de bloedsomloop van de tumorplaats worden weggespoeld.
"We hebben nu een manier gevonden om beide te doen, door microschaaldepots van deze medicijnen in een tumor te creëren, " zegt Zhen Gu, corresponderende auteur van een paper over het werk en een assistent-professor in de gezamenlijke afdeling biomedische technologie aan de North Carolina State University en de University of North Carolina in Chapel Hill.
De onderzoekers beginnen met het maken van een medicijncocktail van TRAIL en cilengitide, wikkel de cocktail vervolgens in een "nanodrager" met een diameter van 100 nanometer (nm). De nanodrager wordt vervolgens bezaaid met humaan serumalbumine (HSA), een overvloedig eiwit in menselijk bloed.
De nanodrager van 100 nm is ook bezaaid met kleinere nanocapsules - slechts 10 nm in diameter - die zijn gemaakt van een hyaluronzuurgel en een enzym bevatten dat transglutaminase (TG) wordt genoemd. De nanodragers worden vervolgens in de bloedbaan geïnjecteerd.
Sommige kankertumoren produceren grote hoeveelheden van het enzym hyaluronidase, die hyaluronzuur afbreekt. Dus, wanneer de nanodragers een kankertumor binnendringen, de hyaluronidase lost de kleine hyaluronzuurgel-nanocapsules op hun oppervlak op. Hierdoor komen de TG-enzymen vrij, die helpen bij het verbinden van de HSA-eiwitten die het oppervlak van andere nanodragers bedekken, het creëren van een verknoopt medicijndepot in de tumor.
De grootte van het verknoopte depot verhindert grotendeels dat het wordt opgenomen door individuele kankercellen of dat het snel wordt weggevaagd in de bloedbaan. In aanvulling, de TG kan ook helpen nanodragers te binden aan andere eiwitten in de tumor, helpen om het depot op zijn plaats te houden.
De omgeving in de tumor is ook zuurder dan de omgeving, en deze zuurgraad breekt langzaam de nanodragers af.
“Dit zorgt voor een geleidelijke, aanhoudende afgifte van de TRAIL en cilengitide in de tumoromgeving, het maximaliseren van de effectiviteit van de medicijnen, "zegt Gu.
De onderzoekers evalueerden deze techniek met behulp van borstkankertumoren bij muizen.
"We ontdekten dat het gebruik van verknoopte depots om TRAIL en cilengitide af te leveren, tumoren tien keer meer kromp dan het gebruik van dezelfde dosis van die medicijnen met behulp van conventionele technieken, " zegt Quanyin Hu, hoofdauteur van het papier en een Ph.D. student aan de gezamenlijke afdeling biomedische technologie van NC State en UNC-Chapel Hill.
"Dit is een proof-of-concept-studie en er moet extra werk worden gedaan om de techniek te ontwikkelen, " zegt Gu. "Maar het is veelbelovend, en we denken dat deze strategie ook kan worden gebruikt voor immunotherapie van kanker. We zouden meer werk in een diermodel moeten doen voordat we klinische proeven kunnen uitvoeren."
Gu merkt ook op dat het te vroeg is om de kosten van de techniek te schatten.
"We bevinden ons in de beginfase van de ontwikkeling van deze techniek, en we proberen het proces eenvoudiger en effectiever te maken - wat de productiekosten zou verlagen, " zegt Gu. "Dat maakt het moeilijk om in te schatten wat de mogelijke kosten zijn.
"En hoewel we geen significante gezondheidsrisico's voorzien, afgezien van die van welke medicijnen dan ook die worden afgeleverd, een van de redenen waarom we dierproeven en klinische proeven doen, is om onvoorziene risico's te identificeren."
De krant, "Tumor-micro-omgeving-gemedieerde constructie en deconstructie van extracellulaire medicijnafgiftedepots, " werd op 19 januari gepubliceerd in het tijdschrift NanoLetters . Het papier is co-auteur van Wujin Sun, Yue Lu, Jager Bomba, en Yanqi Ye op de gezamenlijke afdeling biomedische engineering van NC State en UNC-Chapel Hill; Tianyue Jiang van Nanjing Tech University; en Ari Isaacson van UNC-Chapel Hill. Het werk werd ondersteund door NC TraCS, NIH's Clinical and Translational Science Awards op UNC-CH, toekenningsnummer 1UL1TR001111.
 Hoe hittegolven en droogte samen de perfecte vuurstorm produceren
Hoe hittegolven en droogte samen de perfecte vuurstorm produceren Meer eiwitten en goed voor de planeet:9 redenen waarom we microalgen zouden moeten eten
Meer eiwitten en goed voor de planeet:9 redenen waarom we microalgen zouden moeten eten De natuur doet ertoe - en het stuurt ons een SOS die we niet langer kunnen negeren
De natuur doet ertoe - en het stuurt ons een SOS die we niet langer kunnen negeren Grote door de wind aangedreven oceaanstromingen verschuiven naar de polen
Grote door de wind aangedreven oceaanstromingen verschuiven naar de polen De methaanemissies van noordelijke meren zijn overdag hoger
De methaanemissies van noordelijke meren zijn overdag hoger
Hoofdlijnen
- Anatomy & Physiology Project Ideeën
- Waarom hebben plantencellen zowel celwanden als celmembranen?
- Monitoring van microben om marsonauten gezond te houden
- Nucleïnezuren: structuur, functie, typen en voorbeelden
- Over de zes koninkrijken
- Processen die ATP gebruiken als energiebron
- De verpakking van DNA in chromosomen
- Squash-variëteit waarvan ooit werd gedacht dat ze uitgestorven was, gedijt goed op biologische boerderij
- Hoe onderhoudt een cel homeostase?
- Plasmonische nanoantennes veelbelovend in optische innovaties
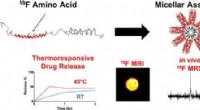
- Onderzoekers ontwikkelen een eiwitmicel die kan worden gevisualiseerd door MRI terwijl het hemotherapeutica levert
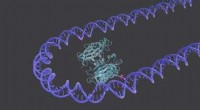
- DNA-bouwpakket voor nanomotoren

- DNA-nanoschakelaars onthullen hoe levensmoleculen met elkaar in verbinding staan
- Bionische deeltjes assembleren zichzelf om licht op te vangen
 Jaarlijks wordt 1,3 miljard ton voedsel verspild. Kunnen we het stoppen?
Jaarlijks wordt 1,3 miljard ton voedsel verspild. Kunnen we het stoppen? Resistentie berekenen voor LED
Resistentie berekenen voor LED Aardgaslekken zijn belangrijke bron van broeikasgasemissies in Los Angeles
Aardgaslekken zijn belangrijke bron van broeikasgasemissies in Los Angeles Hoe het punt van discontinuïteit te vinden in Algebra II
Hoe het punt van discontinuïteit te vinden in Algebra II  NASA richt zich op kustecosystemen met nieuwe ruimtesensor
NASA richt zich op kustecosystemen met nieuwe ruimtesensor De ongelooflijke reis van de eerste Afrikaanse schildpad die in Europa aankwam
De ongelooflijke reis van de eerste Afrikaanse schildpad die in Europa aankwam Hoe de symmetrie lijn te vinden in een kwadratische vergelijking
Hoe de symmetrie lijn te vinden in een kwadratische vergelijking  NASA-NOAA-satelliet volgt de ontwikkeling van Isaias, beweging, doorweekt potentieel
NASA-NOAA-satelliet volgt de ontwikkeling van Isaias, beweging, doorweekt potentieel
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Swedish | German | Dutch | Danish | Norway | Portuguese |

-
Wetenschap © https://nl.scienceaq.com

