
Wetenschap
Nanobuisbos in een microfluïdisch kanaal kan helpen bij het opsporen van zeldzame eiwitten en virussen

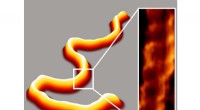
Een cilindrische structuur met patronen die bestaat uit koolstofnanobuisjes.
Ingenieurs van MIT hebben een nieuwe techniek bedacht om moeilijk te detecteren moleculen te vangen, met behulp van bossen van koolstofnanobuisjes.
Het team heeft een eenvoudig microfluïdisch kanaal aangepast met een reeks verticaal uitgelijnde koolstofnanobuisjes - opgerolde roosters van koolstofatomen die lijken op kleine buisjes kippengaas. De onderzoekers hadden eerder een methode bedacht om koolstofnanobuisjes op hun uiteinden te laten staan, als bomen in een bos. Met deze methode, ze creëerden een driedimensionale reeks van permeabele koolstofnanobuisjes in een microfluïdisch apparaat, waardoor vloeistof kan stromen.
Nutsvoorzieningen, in een studie die deze week in de Tijdschrift voor micro-engineering en nanotechnologie , de onderzoekers hebben de nanobuis-array de mogelijkheid gegeven om bepaalde deeltjes op te vangen. Om dit te doen, het team bedekte de array, laag voor laag, met polymeren van wisselende elektrische lading.
"Je kunt elke nanobuis in het bos zien als concentrisch bedekt met verschillende lagen polymeer, " zegt Brian Wardle, hoogleraar luchtvaart en ruimtevaart aan het MIT. "Als je het in doorsnede tekende, het zou zijn als ringen aan een boom."
Afhankelijk van het aantal aangebrachte lagen, de onderzoekers kunnen dikkere of dunnere nanobuisjes maken en daarmee de porositeit van het bos aanpassen om grotere of kleinere deeltjes van belang te vangen.
De polymeercoating van de nanobuisjes kan ook chemisch worden gemanipuleerd om specifieke biodeeltjes die door het bos stromen te binden. Om dit idee te testen, de onderzoekers pasten een gevestigde techniek toe om het oppervlak van de nanobuisjes te behandelen met antilichamen die binden aan prostaatspecifiek antigeen (PSA), een gemeenschappelijk experimenteel doel. De met polymeer beklede arrays vingen 40 procent meer antigenen op, vergeleken met arrays zonder de polymeercoating.
Wardle zegt dat de combinatie van koolstofnanobuisjes en meerlaagse coatings kan helpen bij het fijn afstemmen van microfluïdische apparaten om extreem kleine en zeldzame deeltjes te vangen, zoals bepaalde virussen en eiwitten.
"Er zijn kleinere biodeeltjes die zeer rijke hoeveelheden informatie bevatten waartoe we momenteel geen toegang hebben in point-of-care [medische testen] apparaten zoals microfluïdische chips, " zegt Ward, wie is een co-auteur van het papier. "Arrays van koolstofnanobuisjes zouden eigenlijk een platform kunnen zijn dat zich op die grootte van biodeeltjes zou kunnen richten."

Een ingezoomde weergave van koolstofnanobuisjes, individuele buizen laten zien.
De hoofdauteur van het artikel is Allison Yost, een voormalig afgestudeerde student die momenteel ingenieur is bij Accion Systems. Anderen op het papier zijn onder meer afgestudeerde student Setareh Shahsavari; postdoc Roberta Polak; School of Engineering Hoogleraar onderwijsinnovatie Gareth McKinley; hoogleraar materiaalkunde en techniek Michael Rubner, en Raymond A. en Helen E. St. Laurent hoogleraar chemische technologie Robert Cohen.
Een poreus bos
Koolstofnanobuisjes zijn onderwerp geweest van intensief wetenschappelijk onderzoek, omdat ze uitzonderlijke elektrische, mechanisch, en optische eigenschappen. Hoewel hun gebruik in microfluïdica niet goed is onderzocht, Wardle zegt dat koolstofnanobuisjes een ideaal platform zijn omdat hun eigenschappen kunnen worden gemanipuleerd om bepaalde moleculen van nanometergrootte aan te trekken. Aanvullend, koolstofnanobuisjes zijn voor 99 procent poreus, wat betekent dat een nanobuis ongeveer 1 procent koolstof en 99 procent lucht is.
"Wat heb je nodig, "zegt Wardle. "Je moet hoeveelheden vloeistof door dit materiaal laten stromen om alle miljoenen deeltjes die je niet wilt vinden kwijt te raken en degene te pakken die je wel wilt vinden."
Bovendien, Wardle zegt, een driedimensionaal bos van koolstofnanobuisjes zou veel meer oppervlakte bieden waarop doelmoleculen kunnen interageren, vergeleken met de tweedimensionale oppervlakken in conventionele microfluïdica.
"De opname-efficiëntie zou schalen met het oppervlak, ’ merkt Wardle op.
Een veelzijdige reeks
Het team integreerde een driedimensionale reeks koolstofnanobuizen in een microfluïdisch apparaat door chemische dampafzetting en fotolithografie te gebruiken om koolstofnanobuizen op siliciumwafels te laten groeien en te modelleren. Vervolgens groepeerden ze de nanobuisjes in een cilindervormig bos, van ongeveer 50 micrometer lang en 1 millimeter breed, en centreerde de array binnen een breedte van 3 millimeter, 7 millimeter lang microfluïdisch kanaal.
De onderzoekers bedekten de nanobuisjes in opeenvolgende lagen van afwisselend geladen polymeeroplossingen om onderscheidende, bindende lagen rond elke nanobuis. Om dit te doen, ze lieten elke oplossing door het kanaal stromen en ontdekten dat ze in staat waren om een meer uniforme coating te creëren met een opening tussen de bovenkant van het nanobuisbos en het dak van het kanaal. Door zo'n kloof konden oplossingen overlopen, dan het bos in, coating each individual nanotube. In the absence of a gap, solutions simply flowed around the forest, coating only the outer nanotubes.
After coating the nanotube array in layers of polymer solution, the researchers demonstrated that the array could be primed to detect a given molecule, by treating it with antibodies that typically bind to prostate specific antigen (PSA). They pumped in a solution containing small amounts of PSA and found that the array captured the antigen effectively, throughout the forest, rather than just on the outer surface of a typical microfluidic element.
Wardle says that the nanotube array is extremely versatile, as the carbon nanotubes may be manipulated mechanically, electrically, and optically, while the polymer coatings may be chemically altered to capture a wide range of particles. He says an immediate target may be biomarkers called exosomes, which are less than 100 nanometers wide and can be important signals of a disease's progression.
"Science is really picking up on how much information these particles contain, and they're sort of everywhere, but really hard to find, even with large-scale equipment, " Wardle says. "This type of device actually has all the characteristics and functionality that would allow you to go after bioparticles like exosomes and things that really truly are nanometer scale."
Dit verhaal is opnieuw gepubliceerd met dank aan MIT News (web.mit.edu/newsoffice/), een populaire site met nieuws over MIT-onderzoek, innovatie en onderwijs.
 Afvalplastic omgezet in filtratiemembranen
Afvalplastic omgezet in filtratiemembranen Melkeiwit kan de gezondheid van bosbessen helpen verbeteren
Melkeiwit kan de gezondheid van bosbessen helpen verbeteren Nieuwe biosensor ontworpen om gifstoffen en meer te detecteren
Nieuwe biosensor ontworpen om gifstoffen en meer te detecteren Wetenschappers ontsluiten het potentieel van ultradunne 2D-materialen
Wetenschappers ontsluiten het potentieel van ultradunne 2D-materialen Wetenschappers ontwikkelen nieuw systeem om opkomende door teken overgedragen ziekten te bestuderen
Wetenschappers ontwikkelen nieuw systeem om opkomende door teken overgedragen ziekten te bestuderen
 Wat is de wind in een toendra?
Wat is de wind in een toendra?  Veranderingen in de baan van de aarde maakten de opkomst van complex leven mogelijk
Veranderingen in de baan van de aarde maakten de opkomst van complex leven mogelijk Een van de beroemdste stranden van Australië verdwijnt, en stormen zijn niet de schuldige
Een van de beroemdste stranden van Australië verdwijnt, en stormen zijn niet de schuldige Wijzigingen in de bemesting van de winterteelt kunnen het stikstofverlies verminderen, winst verhogen
Wijzigingen in de bemesting van de winterteelt kunnen het stikstofverlies verminderen, winst verhogen Externe bemesting in chordaten
Externe bemesting in chordaten
Hoofdlijnen
- Wat zijn de verschillen van eenvoudig en gestratificeerd weefsel?
- Onderzoekers gebruiken het ritme van DNA-replicatie om kankercellen te doden
- Belofte van nieuwe antibiotica ligt in het aanhaken van kleine giftige tetherballs aan bacteriën
- De oudste kleur van de aarde was roze
- Osmosis Feiten voor kinderen
- Nucleïnezuurfuncties
- Dennen kappen:eerder vroeger dan later doen is beter voor fynbos
- Wat betekent homozygoot?
- De centrale hoek vinden
- JILA-monsterverwerking van 5 minuten verbetert de beeldvorming en analyse van DNA
- De verwerking van big data energiezuiniger maken met magnetische circuits
- Zilveren nanodeeltjes op grafeenoxidedrager
- Volledig functionele nano-sneeuwman heeft toepassingen voor groenere energie
- Verdraaide objecten op nanoschaal veranderen om toepassingen in toekomstige technologieën op maat te maken

 Klimaatverandering helpt de temperaturen van de hittegolven in Californië op te drijven
Klimaatverandering helpt de temperaturen van de hittegolven in Californië op te drijven Detectorhonden bieden hoop om numbats te redden
Detectorhonden bieden hoop om numbats te redden Nieuwe studie presenteert volledig bedrukte bipolaire Li-S-batterijen in vaste toestand
Nieuwe studie presenteert volledig bedrukte bipolaire Li-S-batterijen in vaste toestand Colorados 834 miljoen dode bomen dreigen branden te verergeren (update)
Colorados 834 miljoen dode bomen dreigen branden te verergeren (update) Onderzoekers voeren eenvoudige berekeningen uit door lichtpatronen door een doorschijnende kubus te laten schijnen
Onderzoekers voeren eenvoudige berekeningen uit door lichtpatronen door een doorschijnende kubus te laten schijnen CaPtAs:een nieuwe niet-centrosymmetrische supergeleider
CaPtAs:een nieuwe niet-centrosymmetrische supergeleider Doorbraak voor lab-on-a-chip materiaal
Doorbraak voor lab-on-a-chip materiaal Draagbare apparaten kunnen ziekte diagnosticeren zodra deze zich voordoet
Draagbare apparaten kunnen ziekte diagnosticeren zodra deze zich voordoet
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway | French |

-
Wetenschap © https://nl.scienceaq.com

