
Wetenschap
Met suiker omhulde nanowormen niet als ontbijt in het menselijke immuunsysteem
IJzernanodeeltjes die vóór magnetische resonantiebeeldvorming worden geïnjecteerd, kunnen weefsels beter zichtbaar maken en dezelfde nanodeeltjes kunnen artsen in staat stellen tumoren nauwkeurig te richten met nieuwe medicijnen. Echter, een van de uitdagingen voor het praktische gebruik van nanodeeltjes in het menselijk lichaam is wat wetenschappers een gebrek aan "hemocompatibiliteit" noemen - nanodeeltjes hebben de neiging om aangevallen en geklaard te worden door het immuunsysteem, hun nut teniet doen en mogelijk ook bijwerkingen veroorzaken, waaronder shock en bloeddrukdaling. Een onderzoek van het University of Colorado Cancer Center dat onlangs in het tijdschrift is gepubliceerd ACS Nano beschrijft een belangrijk mechanisme dat het immuunsysteem gebruikt om zich op ijzeren nanodeeltjes te richten en brengt onderzoekers een stap dichter bij het helpen van nanodeeltjes om deze activering te omzeilen.
"In principe, we probeerden te begrijpen hoe het immuunsysteem nanodeeltjes herkent, " zegt Dmitri Simberg, doctoraat, onderzoeker bij het CU Cancer Center en assistent-professor aan de Skaggs School of Pharmacy and Pharmaceutical Sciences, senior auteur van de krant.
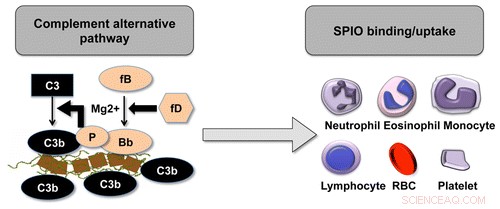
Simberg en collega's begonnen met het injecteren van een versie van met suikerpolymeer dextran gecoate ijzernanodeeltjes die bekend staan als superparamagnetische nanowormen in muizen. Zoals verwacht, het immuunsysteem van de muis viel de nanodeeltjes aan, zoals blijkt uit "opname" door veel immuuncellen, waaronder lymfocyten, neutrofielen en monocyten.
"Echter, we zagen niet dezelfde opname door immuuncellen bij muizen met een zeer specifieke deficiëntie, ' zegt Simberg.
Eén categorie geteste muizen was zo ontworpen dat ze niet in staat waren om eiwitten te produceren die essentieel zijn voor het "complementsysteem" - een van de mechanismen van het immuunsysteem voor het herkennen van pathogenen in bloed. Zoals een post-it op de rug van een vijand slaan, het lichaam gebruikt deze ongeveer 30 eiwitten om ziekteverwekkers en vreemde materialen te markeren voor vernietiging door het immuunsysteem.
"Muizen zonder complementeiwitten vielen nanodeeltjes niet aan en maakten ze niet schoon, " zegt Simberg. In deze complement-deficiënte muizen, superparamagnetische dextran-ijzeroxide-nanowormen ontsnapten aan het immuunsysteem en konden naar wens functioneren, magnetisch labelen van cellen op een manier die MRI-beeldvorming zou ondersteunen.
"Naast muizen, menselijke leukocyten met gehandicapte complementsystemen namen geen ijzernanodeeltjes op, ", zegt Simberg. Menselijke bloedcellen die zowel door gezonde deelnemers als door kankerpatiënten werden gedoneerd, namen nanodeeltjes efficiënt in; toen het bloed werd behandeld met een medicijn dat het complementsysteem remt, de immuuncellen vielen de nanodeeltjes niet aan.
Helaas, de oplossing voor de praktische problemen van het gebruik van nanodeeltjes is niet het blokkeren van het vermogen van het menselijk immuunsysteem om het complementsysteem te rekruteren, wat een essentieel hulpmiddel is in de strijd van het lichaam tegen infectie en ziekte. ("Dat zou slecht zijn, " zegt Simberg.) In plaats daarvan, Simberg en collega's zetten de onderzoekslijn voort op zoek naar manieren om nanodeeltjes te engineeren om dit systeem te omzeilen.
Er zijn drie routes die het complementsysteem activeren:lectine, klassiek en alternatief. De lectineroute herkent specifieke configuraties van suikermoleculen die veel voorkomen op het oppervlak van schadelijke micro-organismen, waaronder salmonella en listeria. De "dextraan" in superparamagnetische dextran-ijzeroxide-nanowormen is een suiker die wordt herkend door de lectine-route, waardoor het complementsysteem wordt geactiveerd en het immuunsysteem deze deeltjes aanvalt. Echter, Simberg en collega's toonden aan dat door het induceren van crosslinks tussen suikermoleculen die deze nanodeeltjes bekleden, de structuur was voldoende veranderd om onzichtbaar te worden voor deze lectineroute.
"Toen we een chemische stof gebruikten om verknopingen op nanodeeltjesoppervlakken te maken, we zagen dat ze bijna onzichtbaar waren voor het immuunsysteem van muizen, ", zegt Simberg. Deze verknoping verminderde de opname van nanodeeltjes door het immuunsysteem met meer dan 70 procent.
Maar (tot verbazing van de onderzoekers), de techniek hielp nanodeeltjes niet om het menselijke immuunsysteem te ontwijken.
"Het bleek dat terwijl muizen meestal de lectineroute gebruiken om het complementsysteem te activeren om nanowormen aan te vallen, bij mensen is de meest actieve route die nanowormen aanvalt de alternatieve route. Deze alternatieve route wordt niet misleid door crosslinking en dus blijft het menselijke complementsysteem gecrosslinkte nanodeeltjes herkennen en aanvallen. ' zegt Simberg.
Echter, het beeld is nog complexer dan dat:ondanks complementactivering, Door de oppervlaktesuikers van nanodeeltjes te verknopen, konden de nanodeeltjes nog steeds gedeeltelijk aan menselijke immuuncellen ontsnappen. Als het geen aanvulling is op systeemontduiking, wat is het met deze crosslinks die nanodeeltjes hielpen ontsnappen?
"We hebben een paper in behandeling over precies dit, "zegt Simberg. "We hopen over een paar maanden voor publicatie in te dienen."
 Onderzoekers rapporteren een temperatuurgevoelige gel die vocht absorbeert en afgeeft
Onderzoekers rapporteren een temperatuurgevoelige gel die vocht absorbeert en afgeeft Wetenschappers ontwikkelen een manier om afvalplastic te gebruiken om autobrandstof te maken
Wetenschappers ontwikkelen een manier om afvalplastic te gebruiken om autobrandstof te maken Hoe is een watermolecule als een magneet?
Hoe is een watermolecule als een magneet?  Waarvoor wordt urethaan gebruikt?
Waarvoor wordt urethaan gebruikt?  Biphilic oppervlakken verminderen ontdooitijden in warmtewisselaars
Biphilic oppervlakken verminderen ontdooitijden in warmtewisselaars
 Nieuw pad om klimaatverandering te beperken en vooruitgang op het gebied van duurzame-ontwikkelingsdoelstellingen van de VN te stimuleren
Nieuw pad om klimaatverandering te beperken en vooruitgang op het gebied van duurzame-ontwikkelingsdoelstellingen van de VN te stimuleren De langzame maar gestage vooruitgang in de richting van ecologische duurzaamheid
De langzame maar gestage vooruitgang in de richting van ecologische duurzaamheid NASA-NOAA-satelliet ziet tropische depressie 22 sterker worden in de Golf van Mexico
NASA-NOAA-satelliet ziet tropische depressie 22 sterker worden in de Golf van Mexico Tyfoon verzwakt maar kan Japan nog steeds bedreigen
Tyfoon verzwakt maar kan Japan nog steeds bedreigen Een wiebel, geluk en voorbereidingen verminderden de verwoesting van Laura
Een wiebel, geluk en voorbereidingen verminderden de verwoesting van Laura
Hoofdlijnen
- Ideeën voor Cookie Science Fair Projects
- Voorkeuren voor het eten van insecten voorspellen na ontbossing
- Klimaatverandering:kunnen kolibries de hitte aan?
- Het redden van Indonesische paradijsvogels dorp voor dorp
- Vier klassen van macromoleculen belangrijk voor levende dingen
- Wat doet Choline voor het lichaam?
- Onderzoek wijst achteruitgang van arctische kustvogels aan
- Earth Microbiome Project:het microbioom van... alles in kaart brengen
- Stelten vliegen honderden kilometers om eieren te leggen die meer dan 50% van hun lichaamsgewicht uitmaken
- IBM-wetenschappers demonstreren in-memory computing met 1 miljoen apparaten voor toepassingen in AI
- Flexibel, draagbare supercondensatoren op basis van poreuze nanokoolstof nanocomposieten
- Methode van onderzoekers houdt belofte in voor hersenonderzoek, betere tests voor virussen

- Nanospace-gecontroleerd goudmateriaal gemaakt met behulp van moleculaire technologie
- Nanodeeltjes kunnen van de longen naar het bloed reizen, mogelijk verklaren van risico's voor het hart
 Onderzoekers werpen licht op modulatie van thermische bleking van koraalriffen door interne golven
Onderzoekers werpen licht op modulatie van thermische bleking van koraalriffen door interne golven Hoe de totale valafstand voor valbeveiliging
Hoe de totale valafstand voor valbeveiliging Dammen in de bovenste Mekong-rivier wijzigen de biologische beschikbaarheid van voedingsstoffen stroomafwaarts
Dammen in de bovenste Mekong-rivier wijzigen de biologische beschikbaarheid van voedingsstoffen stroomafwaarts Wat is een manometer?
Wat is een manometer?  Zes belangrijkste celfuncties
Zes belangrijkste celfuncties Professor verdedigt rol in dataschandaal Cambridge Analytica
Professor verdedigt rol in dataschandaal Cambridge Analytica Microvervuiling die China en Zuid-Azië teistert:studie
Microvervuiling die China en Zuid-Azië teistert:studie Elektriciteit gebruiken om magnetisme te veranderen
Elektriciteit gebruiken om magnetisme te veranderen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

