
Wetenschap
Nanosilicium splitst snel water zonder licht, warmte, of elektriciteit
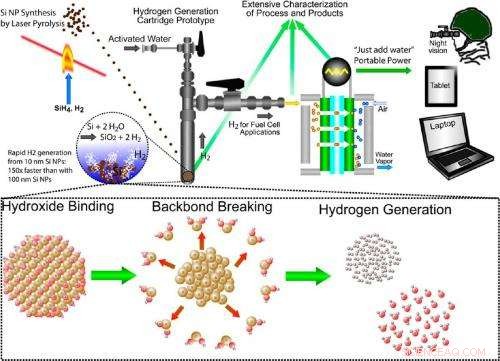
Illustratie van de multidisciplinaire aanpak voor de productie van waterstof door siliciumoxidatie. De aanpak omvat het synthetiseren van silicium nanodeeltjes, de silicium-waterreactie die waterstof op aanvraag genereert, en het gebruik van de waterstof in een brandstofcel voor draagbare energie. Krediet:Folarin Erogbogbo, et al. ©2013 American Chemical Society
(Phys.org)—Hoewel wetenschappers weten dat wanneer silicium zich vermengt met water, waterstof wordt geproduceerd door oxidatie, niemand had verwacht hoe snel silicium nanodeeltjes deze taak zouden kunnen uitvoeren. Zoals een nieuwe studie heeft onthuld, 10-nm silicium nanodeeltjes kunnen 150 keer sneller waterstof genereren dan 100-nm silicium nanodeeltjes, en 1, 000 keer sneller dan bulksilicium. De ontdekking zou de weg kunnen effenen voor snelle waterstofgeneratietechnologieën "gewoon water toevoegen" voor draagbare apparaten zonder dat er licht nodig is, warmte, of elektriciteit.
De onderzoekers, Folarin Erogbogbo aan de Universiteit van Buffalo en coauteurs, hebben hun paper gepubliceerd over het gebruik van nanosilicium om waterstof te genereren in een recent nummer van Nano-letters .
Als waterstof ooit zal worden gebruikt om energie te leveren voor brede commerciële toepassingen, een van de vereisten is het vinden van een snelle, goedkope manier om waterstof te produceren. Een van de meest voorkomende waterstofproductietechnieken is het splitsen van water in waterstof en zuurstof. Er zijn verschillende manieren om water te splitsen, zoals met een elektrische stroom (elektrolyse), warmte, zonlicht, of een stof die chemisch reageert met water. Dergelijke stoffen zijn onder meer aluminium, zink, en silicium.
Zoals de wetenschappers hebben uitgelegd, silicium-water oxidatiereacties zijn tot dusver traag en niet concurrerend met andere watersplitsingstechnieken. Echter, silicium heeft enkele theoretische voordelen, zoals overvloedig zijn, gemakkelijk te vervoeren zijn, en met een hoge energiedichtheid. Verder, bij oxidatie met water, silicium kan theoretisch twee mol waterstof per mol silicium afgeven, of 14% van zijn eigen massa in waterstof.
Om deze redenen, de wetenschappers besloten om silicium nader te bekijken, specifiek silicium nanodeeltjes, die nog niet eerder zijn onderzocht op waterstofproductie. Omdat silicium nanodeeltjes een groter oppervlak hebben dan grotere deeltjes of bulk silicium, men zou verwachten dat de nanodeeltjes sneller waterstof kunnen genereren dan de grotere stukken silicium.
Maar de verbeteringen die de wetenschappers ontdekten met silicium nanodeeltjes overtroffen hun verwachtingen ver. De reactie van 10-nm siliciumdeeltjes met water produceerde in totaal 2,58 mol waterstof per mol silicium (zelfs de theoretische verwachtingen overtroffend), het duurt 5 seconden om 1 mmol waterstof te produceren. In vergelijking, de reactie met 100 nm siliciumdeeltjes leverde in totaal 1,25 mol waterstof per mol silicium op, het duurt 811 seconden om elke mmol waterstof te produceren. Voor bulksilicium, totale productie was slechts 1,03 mol waterstof per mol silicium, het duurt 12,5 uur om elke mmol waterstof te produceren. Voor een tariefvergelijking, het 10-nm silicium genereerde waterstof 150 keer sneller dan 100-nm silicium en 1, 000 keer sneller dan bulksilicium.
"Ik geloof dat het grootste belang van dit werk de demonstratie is dat silicium snel genoeg met water kan reageren om praktisch bruikbaar te zijn voor on-demand waterstofopwekking, " co-auteur Mark Swihart, Hoogleraar chemische en biologische technologie aan de Universiteit van Buffalo, vertelde Phys.org . "Dit resultaat was zowel onverwacht als van potentieel praktisch belang. Hoewel ik niet geloof dat oxidatie van siliciumnanodeeltjes op korte termijn een haalbare methode zal worden voor grootschalige waterstofopwekking, dit proces zou best interessant kunnen zijn voor kleinschalige draagbare toepassingen waar water beschikbaar is."

Een vergelijking van waterstofgeneratiesnelheden voor verschillende vormen van silicium. Maximale tarieven staan in de linkerkolom met afbeeldingen van de monsters erop. De gemiddelde tarieven staan in de rechterkolom. De rode lijn geeft de maximale gerapporteerde snelheid aan voor waterstof gegenereerd uit aluminium. Krediet:Folarin Erogbogbo, et al. ©2013 American Chemical Society
Naast het sneller produceren van waterstof dan grotere stukken silicium, het 10-nm silicium produceert ook aanzienlijk sneller waterstof dan aluminium- en zink-nanodeeltjes. Zoals Swihart uitlegde, de verklaring voor deze ongelijkheid verschilt voor de twee materialen.
"Vergeleken met aluminium, silicium reageert sneller omdat aluminium een dichter en robuuster oxide vormt (Al 2 O 3 ) op het oppervlak, die de reactie beperkt, " zei hij. "In aanwezigheid van een base zoals KOH [kaliumhydroxide], silicium produceert meestal oplosbaar kiezelzuur (Si(OH) 4 ). In vergelijking met zink, silicium is gewoon reactiever, vooral bij kamertemperatuur."
Hoewel het grotere oppervlak van het 10-nm silicium in vergelijking met grotere siliciumstukken bijdraagt aan de snelle waterstofproductiesnelheid, oppervlakte alleen kan de enorme snelheidsstijging die de wetenschappers hebben waargenomen niet verklaren. Het oppervlak van 10-nm silicium is 204 m 2 /G, ongeveer 6 keer groter dan het oppervlak van 100 nm silicium, dat is 32 m 2 /G.
Om te begrijpen wat de veel grotere toename van de waterstofproductiesnelheid veroorzaakt, de onderzoekers voerden experimenten uit tijdens het siliciumetsproces. Ze vonden dat, voor de 10-nm deeltjes, etsen omvat het verwijderen van een gelijk aantal roostervlakken in elke richting (isotroop etsen). In tegenstelling tot, voor 100 nm deeltjes en microdeeltjes, ongelijke aantallen roostervlakken worden in elke richting verwijderd (anisotroop etsen).
De onderzoekers schrijven dit etsverschil toe aan de verschillende geometrieën van kristallen van verschillende grootte. Als gevolg van dit verschil, de grotere deeltjes nemen niet-sferische vormen aan die minder reactieve oppervlakken blootstellen in vergelijking met de kleinere deeltjes, die bijna bolvormig blijven, het blootstellen van alle kristalfacetten voor reactie. Grotere deeltjes ontwikkelen ook dikkere lagen van geoxideerde siliciumbijproducten waardoor water moet diffunderen. Beide factoren beperken de reactiesnelheid op grotere deeltjes.
Om te bevestigen dat de 10 nm silicium-waterreactie waterstof genereert zonder bijproducten die de toepassingen zouden kunnen verstoren, de onderzoekers gebruikten de door silicium gegenereerde waterstof om een brandstofcel te laten werken. De brandstofcel presteerde erg goed, meer stroom en spanning produceren dan de theoretische hoeveelheid zuivere waterstof, wat te wijten is aan het feit dat de 10-nm deeltjes meer waterstof genereerden dan de theoretische 14 gew.%.
De onderzoekers hopen dat dit verrassende vermogen van silicium nanodeeltjes om snel water te splitsen en waterstof te genereren zou kunnen leiden tot de ontwikkeling van een waterstof-on-demand technologie waarmee brandstofcellen kunnen worden gebruikt in draagbare apparaten. Deze technologie vereist een grootschalige, energiezuinige methode voor de productie van silicium nanodeeltjes, maar zou enkele voordelen kunnen hebben in vergelijking met andere waterstofgeneratietechnieken.
"Het belangrijkste voordeel van siliciumoxidatie voor waterstofopwekking is de eenvoud, " zei Swihart. "Met deze benadering, waterstof wordt snel geproduceerd, op kamertemperatuur, en zonder de noodzaak van een externe energiebron. De energie die nodig is voor waterstofopwekking wordt effectief opgeslagen in het silicium. Alle energie-input die nodig is voor de productie van het silicium kan op een centrale locatie worden geleverd, en het silicium kan vervolgens worden gebruikt in draagbare toepassingen.
"Het belangrijkste nadeel van siliciumoxidatie is de relatieve inefficiëntie ervan. De energie-input die nodig is om de siliciumnanodeeltjes te maken, is veel groter dan de energie die beschikbaar is uit de waterstof die uiteindelijk wordt geproduceerd. Voor grootschalige toepassingen, dit zou een probleem zijn. Voor draagbare toepassingen, Het is niet. Bijvoorbeeld, de kosten van elektriciteit geleverd door een gewone huishoudbatterij kunnen gemakkelijk 10 tot 100 keer hoger zijn dan de kosten van elektriciteit van een nutsbedrijf, maar batterijen spelen nog steeds een belangrijke rol in ons leven."
In de toekomst, de onderzoekers zijn van plan om de waterstofproductiecapaciteit van siliciumoxidatie verder te vergroten door te experimenteren met verschillende mengsels.
"Een richting die we momenteel nastreven is het gebruik van mengsels van silicium nanodeeltjes met metaalhydriden, die ook reageren met water om waterstof te produceren, Swihart zei. "Verbindingen zoals lithiumhydride en natriumhydride reageren met water om de base (LiOH of NaOH) te produceren die nodig is om de siliciumoxidatie te katalyseren. Echter, ze kunnen te snel reageren met water (explosief) en zijn niet stabiel in de lucht. Door ze te mengen met siliciumnanodeeltjes of ze te coaten met siliciumnanodeeltjes kan zowel hun reactiviteit worden getemperd als de waterstofgeneratiecapaciteit van het systeem worden vergroot door de toegevoegde base te vervangen (bijv. KOH in het gepubliceerde artikel) met een materiaal dat ook waterstof genereert."
Copyright 2013 Phys.org
Alle rechten voorbehouden. Dit materiaal mag niet worden gepubliceerd, uitzending, geheel of gedeeltelijk herschreven of herverdeeld zonder de uitdrukkelijke schriftelijke toestemming van Phys.org.
 Meer elektronische materialen geopend met nieuw metaal-organisch raamwerk
Meer elektronische materialen geopend met nieuw metaal-organisch raamwerk Onderzoek bevordert de duurzaamheid van de productie van chirurgische latexhandschoenen
Onderzoek bevordert de duurzaamheid van de productie van chirurgische latexhandschoenen Vergroening van de farmaceutische industrie
Vergroening van de farmaceutische industrie Snel reagerend, kleurveranderende moleculaire sonde detecteert wanneer een materiaal op het punt staat te falen
Snel reagerend, kleurveranderende moleculaire sonde detecteert wanneer een materiaal op het punt staat te falen Gemakkelijke ontleding van metaal-NHC-complexen onder katalytische omstandigheden en de sleutelrol van NHC-gestabiliseerde nanodeeltjes
Gemakkelijke ontleding van metaal-NHC-complexen onder katalytische omstandigheden en de sleutelrol van NHC-gestabiliseerde nanodeeltjes
 Wereldwijde stedelijke groei gekenmerkt door voorsteden, geen wolkenkrabbers
Wereldwijde stedelijke groei gekenmerkt door voorsteden, geen wolkenkrabbers Een deel van de Groenlandse ijskap bevindt zich mogelijk dicht bij een kantelpunt
Een deel van de Groenlandse ijskap bevindt zich mogelijk dicht bij een kantelpunt Brandstichters Portugal voeden natuurbrandvernietiging
Brandstichters Portugal voeden natuurbrandvernietiging Broeikasgassen veroorzaken meer veranderingen dan we aankunnen
Broeikasgassen veroorzaken meer veranderingen dan we aankunnen Historische bosbranden in het Amazonewoud bedreigen het klimaat en verhogen het risico op nieuwe ziekten
Historische bosbranden in het Amazonewoud bedreigen het klimaat en verhogen het risico op nieuwe ziekten
Hoofdlijnen
- Een 3D-poster maken van de celcyclus
- Een menselijk hart maken van pop-flessen
- Panspermia:zorgden buitenaardse zaden ervoor dat het leven op aarde explodeerde?
- Hoe gelukkig te zijn in een relatie
- Hoe worden nieuwe cellen geproduceerd?
- Hoe werkt ureum denaturisch?
- Hoe een 3D-model van het ademhalingssysteem te maken
- Federale overheid:geen lijst van bedreigde soorten voor walrus
- Bloedbad vreest race om zeldzame Australische papegaai te redden
- Onderzoekers schakelen magnetisme van individuele moleculen om

- Omgevingslicht verandert breking in 2D-materiaal

- Een spin-wave detectiveverhaal:onderzoekers verifiëren verrassend gedrag in een 2D-magneet
- Kwantumgolven in het hart van organische zonnecellen

- Nieuw nanodeeltje levert, volgt kankermedicijnen

 Gallons converteren naar metrische tonnen
Gallons converteren naar metrische tonnen Het verschil tussen onderzoeksvragen en hypothese
Het verschil tussen onderzoeksvragen en hypothese  Nanometers converteren naar Joules
Nanometers converteren naar Joules Globale temperatuurverandering toe te schrijven aan externe factoren, bevestigt nieuwe studie
Globale temperatuurverandering toe te schrijven aan externe factoren, bevestigt nieuwe studie Door goedkope en veilige zwart-witte materialen te combineren, ontstaan kleurrijke pigmenten
Door goedkope en veilige zwart-witte materialen te combineren, ontstaan kleurrijke pigmenten Zichtbaar licht-geïnduceerde bifunctionele rhodium katalyse ontwikkeld voor decarbonylatieve koppeling van imiden met alkynen
Zichtbaar licht-geïnduceerde bifunctionele rhodium katalyse ontwikkeld voor decarbonylatieve koppeling van imiden met alkynen GM verdiensten hoogste verwachtingen; voorspelling verlaagd na staking
GM verdiensten hoogste verwachtingen; voorspelling verlaagd na staking Hoe Factor-polynomen in factor vier te begrippen
Hoe Factor-polynomen in factor vier te begrippen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Spanish | Portuguese | Swedish | Dutch | Danish | Norway | Italian | German |

-
Wetenschap © https://nl.scienceaq.com

