
Wetenschap
Koolstofnanobuisjes verlagen zenuwbeschadigend chloride in cellen
Een nanomateriaal ontwikkeld door onderzoekers van Duke kan helpen bij het reguleren van chlorideniveaus in zenuwcellen die bijdragen aan chronische pijn, epilepsie, en traumatisch hersenletsel.
De bevindingen, online gepubliceerd op 10 december 2012, in het journaal Klein , werden aangetoond in individuele zenuwcellen en in de hersenen van muizen en ratten, en kunnen toekomstige toepassingen hebben in intracraniële of spinale apparaten om neurale verwondingen te helpen behandelen.
Koolstof nanobuisjes zijn een nanomateriaal met unieke eigenschappen, inclusief mechanische sterkte en elektrische geleidbaarheid. Deze kenmerken, samen met hun kleine formaat, ze aantrekkelijk maken voor zowel onderzoekers in technologie als geneeskunde.
In een wereld van krimpende computers en smartphones, koolstofnanobuisjes zijn aangeboord als een oplossing voor het verbeteren van microchips. Ze overtreffen siliciummicrochips in grootte en prestaties, tegemoet komen aan de vraag naar kleinere, snellere apparaten. Voor mensen met zenuwletsel en bepaalde neurologische aandoeningen, apparaten die zijn bedekt met of volledig zijn gemaakt van koolstofnanobuisjes, zouden een nieuwe weg kunnen bieden voor het verbeteren van behandelingsopties.
"Koolstofnanobuisjes zijn veelbelovend voor een scala aan toepassingen, en we beginnen pas hun enorme potentieel te zien, " zei hoofdauteur Wolfgang Liedtke, MD, doctoraat, universitair hoofddocent geneeskunde en neurobiologie aan Duke. "Hun uitzonderlijke mechanische en elektrische eigenschappen maken ze ideaal voor het ontwikkelen van apparaten die in verbinding staan met zenuwweefsel. de precieze mechanismen achter koolstofnanobuisjes en hun effect op neuronen blijven ongrijpbaar."
Niet alle koolstofnanobuisjes zijn hetzelfde. Jie Liu, doctoraat, George Barth Geller, hoogleraar scheikunde aan de Duke University en hoofdauteur van de studie, ontwikkelde specifieke koolstofnanobuisjes die buitengewoon zuiver zijn. Genoemd weinigwandige koolstofnanobuisjes, ze hebben superieure eigenschappen ten opzichte van hun in de handel verkrijgbare tegenhangers.
Duke-onderzoekers gingen aanvankelijk na of koolstofnanobuisjes toxische of nadelige effecten hadden op levend weefsel. Neuronen bestuderen die zijn gekweekt uit knaagdieren, die een "hersenschors in een schaal voorstelt, Ze ontdekten het tegenovergestelde. Het blootstellen van de cellen aan koolstofnanobuisjes bleek een voedend effect te hebben op de neuronen, waardoor ze groter en sterker worden.
"Eerdere studies hebben gekeken naar het gedrag van koolstofnanobuisjes op neuronen. de onzuiverheid in de nanobuisjes had een significante invloed op de resultaten. Nadat we in ons laboratorium zuivere, enkelwandige koolstofnanobuisjes hadden ontwikkeld, we ontdekten dat nanobuisjes de groei van de neuronale cellen aanzienlijk versnelden, " zei Liu.
Neurale circuits kunnen worden beschadigd door verhoogd chloride in neuronen. Bij een aantal ziekten gaat het om schade aan de neurale circuits, waaronder chronische pijn, epilepsie, en traumatisch hersenletsel.
Lage niveaus van chloride in neuronen worden onderhouden door een chloridetransporteiwit genaamd KCC2, die functioneert door chloride-ionen uit de cel te karnen. In volwassen neuronen, er is geen back-up voor deze functie.
De onvolgroeide neuronen die in het laboratorium van Liedtke werden gekweekt, hadden hoge niveaus van chloride, maar naarmate de cellen rijpen, hun chloridegehalte daalde naarmate KCC2 toenam. Toen de neuronen werden blootgesteld aan koolstofnanobuisjes, de cellen rijpten veel sneller, en het chloridegehalte daalde sneller. Onderzoekers ontdekten dat jongere cellen die werden blootgesteld aan koolstofnanobuisjes meer KCC2-eiwit produceerden.
"Koolstof nanobuisjes verbeterden de regulatie van chloride in neuronen tot normale niveaus. Deze veranderingen zijn van enorm belang voor de cel, ' zei Liedtke.
De toename van KCC2-eiwit was ook verbonden met een toename van calcium in de neuronen. De verhoogde calciumspiegels activeerden een eiwit dat in de hersenen wordt aangetroffen, CaMKII genaamd, dat een neuron signaleert om meer KCC2 aan te maken.
Vergelijkbare resultaten werden waargenomen in muizenhersenen, omdat de koolstofnanobuisjes een toename van de activiteit van het KCC2-gen veroorzaakten, wat suggereert dat de weinigwandige koolstofnanobuisjes de genregulatie van KCC2 beïnvloeden.
Deze bevindingen kunnen leiden tot de ontwikkeling van een nieuwe generatie neurale engineering-apparaten die koolstofnanobuisjes gebruiken. Bestaande apparaten die de functie van zenuwcellen moduleren, maken gebruik van elektrische systemen die al tientallen jaren oud zijn.
"We hopen dat koolstofnanobuisjes net zo goed zullen werken in gewonde zenuwen als in onze studie van zich ontwikkelende neuronen, "Vervolgde Liedtke. "Het gebruik van koolstofnanobuisjes staat nog in de kinderschoenen, en we zijn verheugd om deel uit te maken van een zich ontwikkelend veld met zoveel potentieel."
 Hogere koolstofdioxidegehaltes kunnen ons denken in de war brengen
Hogere koolstofdioxidegehaltes kunnen ons denken in de war brengen Ontbossing in Braziliaanse Amazone stijgt naar hoogste punt in 12 jaar
Ontbossing in Braziliaanse Amazone stijgt naar hoogste punt in 12 jaar Logging en het effect ervan op het ecosysteem
Logging en het effect ervan op het ecosysteem  Boomringen van gletsjers kunnen aanwijzingen bevatten voor de toekomst van planeten
Boomringen van gletsjers kunnen aanwijzingen bevatten voor de toekomst van planeten De meest voorkomende oceaanplanten
De meest voorkomende oceaanplanten
Hoofdlijnen
- Organisme: definitie, types, kenmerken en voorbeelden
- Wat eerst kwam,
- Verschil tussen korrel- en agranulaire leukocyten
- Septate versus niet-Septate Hyphae
- De celstructuur van een ui
- Vogels onthullen het belang van goede buren voor gezondheid en veroudering
- Uitvindingen in 1947
- Wat gebeurt er tijdens de G1-fase?
- Effecten van de microscoop op Science
- Chemici kunnen slim glas slimmer maken door het op nanoschaal te manipuleren

- 15 keer sterker dan staal:wetenschappers ontwikkelen zich het sterkst, lichtste glazen nanovezels ter wereld

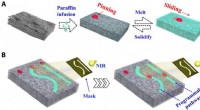
- Met paraffine doordrenkte poreuze grafeenfilm (PIPGF) met programmeerbare bevochtigbaarheid
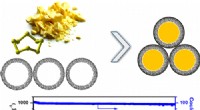
- Op weg naar het maken van lithium-zwavelbatterijen een commerciële realiteit voor een grotere energiestoot
- Stralend licht op tweedimensionale magneten

 Nieuwe experimenten en simulaties onthullen moleculaire interacties in extreme fasen van waterijs
Nieuwe experimenten en simulaties onthullen moleculaire interacties in extreme fasen van waterijs Heavy metal donder:Eiwit kan worden ingeschakeld om elektriciteit als een metaal te geleiden
Heavy metal donder:Eiwit kan worden ingeschakeld om elektriciteit als een metaal te geleiden Studie kan strategieën verbeteren om de afvoer van nutriënten naar de Mississippi te verminderen
Studie kan strategieën verbeteren om de afvoer van nutriënten naar de Mississippi te verminderen Hoe maak je een katrol voor kinderen
Hoe maak je een katrol voor kinderen  SpaceX lanceert forse raket met 24 satellieten, experimenten
SpaceX lanceert forse raket met 24 satellieten, experimenten Betonblok op je borst:astronauten vertellen over mislukte ruimtelancering
Betonblok op je borst:astronauten vertellen over mislukte ruimtelancering Coronavirus:wat we nu doen, kan het klimaattraject van de aarde veranderen
Coronavirus:wat we nu doen, kan het klimaattraject van de aarde veranderen Bijna een op de drie mensen wereldwijd zal in 2030 nog steeds voornamelijk vervuilende kookbrandstoffen gebruiken
Bijna een op de drie mensen wereldwijd zal in 2030 nog steeds voornamelijk vervuilende kookbrandstoffen gebruiken
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | German | Dutch | Danish | Swedish | Norway |

-
Wetenschap © https://nl.scienceaq.com

