
Wetenschap
Virus-nabootsende nanodeeltjes kunnen langdurige immuniteit stimuleren
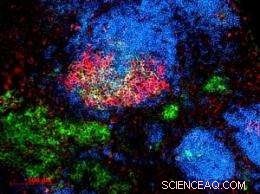
Blauw toont rustende B-cellen. Rood toont geactiveerde B-cellen die worden "getraind" om hoogwaardige antilichamen te produceren. Groen toont gespecialiseerde antilichaam-producerende cellen. (Klik op afbeelding voor versie met hoge resolutie. Credit:Emory University)
Emory postdoctoraal fellow Sudhir Pai Kasturi, doctoraat, creëerde minuscule deeltjes bezaaid met moleculen die Toll-achtige receptoren inschakelen. Hij werkte samen met collega Niren Murthy, doctoraat, universitair hoofddocent bij de Wallace H. Coulter Department of Biomedical Engineering aan Georgia Tech en Emory University.
Vaccinwetenschappers zeggen dat hun "heilige graal" is om een levenslange immuniteit te stimuleren. Levende virale vaccins zoals de pokken- of gele koortsvaccins bieden immuunbescherming die tientallen jaren aanhoudt, maar ondanks hun succes, wetenschappers zijn in het ongewisse gebleven over hoe ze zo'n langdurige immuniteit induceren.
Wetenschappers van het Emory Vaccine Center hebben minuscule nanodeeltjes ontworpen die qua grootte en immunologische samenstelling op virussen lijken en die levenslange immuniteit bij muizen opwekken. Ze ontwierpen de deeltjes om de immuunstimulerende effecten na te bootsen van een van de meest succesvolle vaccins die ooit zijn ontwikkeld:het vaccin tegen gele koorts. de deeltjes, gemaakt van biologisch afbreekbare polymeren, hebben componenten die twee verschillende delen van het aangeboren immuunsysteem activeren en kunnen door elkaar worden gebruikt met materiaal van veel verschillende bacteriën of virussen.
De resultaten worden beschreven in het nummer van deze week van Natuur .
"Deze resultaten pakken een al lang bestaande puzzel in de vaccinologie aan:hoe zorgen succesvolle vaccins voor langdurige immuniteit?", zegt senior auteur Bali Pulentran, doctoraat, Charles Howard Candler, hoogleraar pathologie en laboratoriumgeneeskunde aan de Emory University School of Medicine en onderzoeker aan het Yerkes National Primate Research Center.
"Deze deeltjes kunnen een onmiddellijke manier zijn om schaarse voorraden op te rekken wanneer de toegang tot viraal materiaal beperkt is, zoals pandemische griep of tijdens een opkomende infectie. In aanvulling, er zijn veel ziekten, zoals hiv, malaria, tuberculose en dengue, die nog steeds geen effectieve vaccins hebben, waar we verwachten dat dit type immuniteitsversterker een rol zou kunnen spelen.”
Eén injectie met het levende virale gelekoortsvaccin, ontwikkeld in de jaren dertig door Nobelprijswinnaar Max Theiler, decennialang kan beschermen tegen ziekteverwekkende vormen van het virus. Pulendran en zijn collega's hebben onderzocht hoe mensen reageren op het vaccin tegen gele koorts, in de hoop het te imiteren.
Een aantal jaar geleden, zij stelden vast dat het gelekoortsvaccin meerdere Toll-like receptoren (TLR's) in het aangeboren immuunsysteem stimuleerde. TLR's zijn aanwezig in zowel insecten als zoogdieren, vogels en vissen. Het zijn moleculen die tot expressie worden gebracht door cellen die stukjes virussen kunnen waarnemen, bacteriën en parasieten en kunnen het immuunsysteem activeren. De groep van Pulendran toonde aan dat het immuunsysteem het gelekoortsvaccin via meerdere TLR's waarnam, en dat dit nodig was voor de door het vaccin opgewekte immuniteit.
"TLR's zijn als het zesde zintuig in ons lichaam, omdat ze een voortreffelijk vermogen hebben om virussen en bacteriën waar te nemen, en deze informatie over te brengen om de immuunrespons te stimuleren, ', zegt Pulendran. "We ontdekten dat om de beste immuunrespons te krijgen, je moet meer dan één soort Toll‑like receptor raken. Ons doel was om een synthetisch deeltje te maken dat deze taak volbrengt.”
Emory postdoctoraal fellow Sudhir Pai Kasturi, doctoraat, creëerde minuscule deeltjes bezaaid met moleculen die Toll-achtige receptoren inschakelen. Hij werkte samen met collega Niren Murthy, doctoraat, universitair hoofddocent bij de Wallace H. Coulter Department of Biomedical Engineering aan Georgia Tech en Emory University.
"We zijn erg enthousiast over het bouwen op dit platform om verbeterde vaccins te ontwerpen voor bestaande en opkomende infectieziekten", zegt Kasturi, de primaire auteur die in het laboratorium van Pulentran in het Emory Vaccine Center werkt. Een van de componenten van de deeltjes is MPL (monofosforyllipide A), een onderdeel van bacteriële celwanden, en de andere is imiquimod, een chemische stof die de effecten van viraal RNA nabootst. De deeltjes zijn gemaakt van PLGA-poly(melkzuur)-co-(glycolzuur)-een synthetisch polymeer dat wordt gebruikt voor biologisch afbreekbare transplantaten en hechtingen.
Alle drie de componenten zijn afzonderlijk door de FDA goedgekeurd voor menselijk gebruik. Sinds enkele decennia is het enige door de FDA goedgekeurde vaccinadditief was aluin, totdat in 2009 een baarmoederhalskankervaccin met MPL werd goedgekeurd. Vanwege verschillen in het immuunsysteem tussen muizen en apen, de wetenschappers vervingen imiquimod door de verwante chemische resiquimod voor experimenten met apen.
In muizen, de deeltjes kunnen de productie van antilichamen tegen eiwitten van het griepvirus of miltvuurbacteriën verschillende ordes van grootte effectiever stimuleren dan aluin, vonden de auteurs. In aanvulling, de immuuncellen blijven ten minste 18 maanden in de lymfeklieren aanwezig, bijna de levensduur van een muis. Bij experimenten met apen, nanodeeltjes met viraal eiwit zouden robuuste reacties kunnen induceren die groter zijn dan vijf keer de respons die wordt veroorzaakt door een dosis van hetzelfde virale eiwit dat op zichzelf wordt gegeven, zonder de nanodeeltjes.
 Zelfherstellende katalysatoren maken het gemakkelijker om zonne-energie op te slaan met water
Zelfherstellende katalysatoren maken het gemakkelijker om zonne-energie op te slaan met water Onderzoekssamenwerking kan spuitgieten een nieuwe vorm geven
Onderzoekssamenwerking kan spuitgieten een nieuwe vorm geven Waterafstotend materiaal werpt af als een slang bij beschadiging
Waterafstotend materiaal werpt af als een slang bij beschadiging Waarom hebben planten water nodig in fotosynthese?
Waarom hebben planten water nodig in fotosynthese?  Onderzoekers vinden nieuwe manieren om verspild methaan te benutten
Onderzoekers vinden nieuwe manieren om verspild methaan te benutten
Hoofdlijnen
- De wetenschap ontdekt waarom sommigen van ASMR-video's houden en anderen ze haten
- Welke mechanismen zorgen voor de nauwkeurigheid van DNA-replicatie?
- Een eiwitduo zorgt ervoor dat de chromosomen in de voortplantingscellen hun significante andere vinden
- Het vinden van een dodelijke parasieten kwetsbaarheden
- Misplaatste monarchen:clusters van vlinders in het noorden
- Wat zijn enkele kenmerken van DNA?
- Genetische barcodes worden gebruikt om cruciale populaties in een ecosysteem van koraalriffen te kwantificeren
- Onderzoek suggereert dat gevaarlijke gewassenschimmel giftige chemicaliën produceert om insecten af te weren
- Wat levert elektronen voor de lichtreacties?
- Optische nanoantenne met hoge bitrate ontwikkeld voor gebruik met optische golfgeleider

- Bacteriële nanoporiën openen de toekomst van gegevensopslag

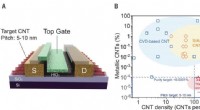
- Proces om goed uitgelijnde CNT-arrays te produceren op een siliciumwafel van 10 centimeter
- Innovatieve sensor detecteert specifiek en nauwkeurig moleculen

- Zullen door bellen aangedreven microraketten door de menselijke maag zoeven?
 Apples nieuwsabonnementsservice een allegaartje voor uitgevers
Apples nieuwsabonnementsservice een allegaartje voor uitgevers Phonon nano-engineering:trillingen van nano-eilanden voeren warmte effectiever af
Phonon nano-engineering:trillingen van nano-eilanden voeren warmte effectiever af Wie heeft de term virtual reality populair gemaakt?
Wie heeft de term virtual reality populair gemaakt?  Hoe het percentage transmissie te berekenen
Hoe het percentage transmissie te berekenen De temperatuur van de oceaan meten door de snelheid te meten van de geluidsgolven die er doorheen gaan
De temperatuur van de oceaan meten door de snelheid te meten van de geluidsgolven die er doorheen gaan Artefacten blootgelegd door orkaan Maria leiden tot archeologische ontdekking
Artefacten blootgelegd door orkaan Maria leiden tot archeologische ontdekking We weten eindelijk waarom het oude Romeinse beton langer meegaat dan het onze
We weten eindelijk waarom het oude Romeinse beton langer meegaat dan het onze  Slechte cijfers gekoppeld aan lestijden die niet overeenkomen met onze biologische klokken
Slechte cijfers gekoppeld aan lestijden die niet overeenkomen met onze biologische klokken
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- Italian | Spanish | Swedish | German | Dutch | Danish | Norway | French | Portuguese |

-
Wetenschap © https://nl.scienceaq.com

