
Wetenschap
'S Werelds kleinste batterij:opladen doet elektroden van nanoformaat opzwellen, langwerpig en spiraalvormig
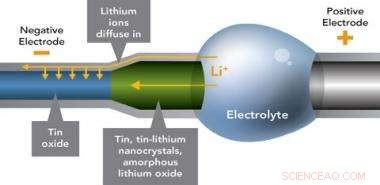
Deze batterij van nanoformaat laat zien hoe positieve lithiumionen de negatieve elektrode (blauw) overspoelen, het veranderen van de grootte, vorm en aard van het materiaal (het groene deel van de elektrode). Sommige oplaadbare materialen zijn mogelijk beter bestand tegen herhaalde vormveranderingen dan andere.
(PhysOrg.com) -- Nieuwe afbeeldingen met hoge resolutie van elektrodedraden gemaakt van materialen die worden gebruikt in oplaadbare lithium-ionbatterijen laten zien dat ze verwringen als ze worden opgeladen met elektriciteit. De dunne, draden van nanoformaat kronkelen en worden dik als lithiumionen naar binnen stromen tijdens het opladen, volgens een artikel in de uitgave van het tijdschrift van deze week Wetenschap . Het werk suggereert hoe oplaadbare batterijen het uiteindelijk begeven en biedt mogelijk inzichten voor het bouwen van betere batterijen.
Batterijontwikkelaars weten dat het steeds opnieuw opladen en gebruiken van lithiumbatterijen de elektrodematerialen beschadigt, maar deze afbeeldingen op nanometerschaal bieden een realistisch beeld van hoe. Dunne draden van tinoxide, die dienen als de negatieve elektrode, een derde dik worden en twee keer zo lang uitrekken door het binnenstromen van lithiumionen. de lithiumionen veranderen het tinoxide van een netjes gerangschikt kristal in een amorf glasachtig materiaal.
"Nanodraden van tinoxide waren beter bestand tegen de vervormingen die gepaard gaan met elektrische stroom dan bulktinoxide, dat is een bros keramiek, " zei Chongmin Wang, een materiaalwetenschapper bij het Pacific Northwest National Laboratory van het Department of Energy. "Het doet me denken aan het maken van een touw van staal - je windt dunnere draden samen in plaats van één dik touw te maken."
In een van de video's hieronder weergegeven, de nanodraad lijkt op een rietje, terwijl de lithiumionen lijken op een drank die er doorheen wordt gezogen. Herhaalde vormveranderingen kunnen de elektrodematerialen beschadigen door kleine defecten te introduceren die zich in de loop van de tijd ophopen.
Op jacht naar elektronen
In eerder werk bij DOE's Environmental Molecular Sciences Laboratory op de PNNL-campus, Wang, PNNL-chemicus Wu Xu en andere collega's slaagden erin een momentopname te maken van een grotere nanodraad van ongeveer een micrometer - of een honderdste van de breedte van een mensenhaar - die gedeeltelijk was opgeladen. Maar de experimentele opstelling liet het opladen niet in actie zien.
Om de dynamiek van een geladen elektrode te bekijken, Wang en Xu werkten samen met Jianyu Huang bij DOE's Center for Integrated Nanotechnologies bij Sandia National Laboratories in New Mexico en anderen. Het team gebruikte een speciaal uitgeruste transmissie-elektronenmicroscoop om een miniatuurbatterij op te zetten. Met dit instrument konden ze kleinere draden met een diameter van ongeveer 200 nanometer (ongeveer een vijfde van de breedte van de vorige nanodraden) in beeld brengen tijdens het opladen.
Oplaadbare lithium-ionbatterijen werken omdat lithiumionen van elektronen houden. Positief geladen lithiumionen hangen normaal gesproken in de positieve elektrode, waar een metaaloxide zijn elektronen deelt met lithium. Maar het opladen van een batterij pompt vrije elektronen in de negatieve elektrode, die aan de overkant van een meer van elektrolyten zit waardoor lithiumionen kunnen zwemmen, maar elektronen niet. Het lithium verlangt meer naar de elektronen aan de negatieve kant van het meer dan de elektronen die het deelt met het metaaloxide aan de positieve kant. Dus lithiumionen stromen van de positieve naar de negatieve elektrode, daar paren met vrije elektronen.
Maar elektronen zijn wispelturig. Door een batterij in een apparaat te gebruiken, kunnen de elektronen uit de negatieve elektrode glippen, de lithiumionen achterlatend. Dus zonder vrije elektronen metgezellen, de lithiumionen keren terug naar de positieve elektrode en de omhelzing van het metaaloxide.
De miniatuurbatterij van Wang omvatte een positieve elektrode van lithiumkobaltoxide en een negatieve elektrode gemaakt van dunne nanodraden van tinoxide. Tussen de twee elektroden, een elektrolyt zorgde voor een kanaal voor lithiumionen en een barrière voor elektronen. De elektrolyt is speciaal ontworpen om de omstandigheden in de microscoop te weerstaan.
Toen het team de miniatuurbatterij met een constante spanning oplaadde, lithiumionen worden door de tinoxidedraad opgezogen, getrokken door de elektronen aan de negatieve elektrode. De draad vetgemest en verlengd met ongeveer 250 procent in totaal volume, en kronkelde als een slang.
In aanvulling, de microscopie toonde aan dat de draad begon in een kristallijne vorm. Maar de lithiumionen veranderden het tinoxide in een materiaal zoals glas, waarin atomen meer willekeurig zijn gerangschikt dan in een kristal. De onderzoekers concludeerden dat de hoeveelheid vervorming die optreedt tijdens het opladen en gebruik na een tijdje het batterijmateriaal kan verslijten. Toch, het tinoxide leek het beter te doen als nanodraad dan in zijn grotere, bulkvorm.
"We denken dat dit werk het nieuwe denken over energieopslag in het algemeen zal stimuleren, " zei Wang. "Dit is nog maar het begin, en we hopen dat het ons door het voortdurende werk zal laten zien hoe we een betere batterij kunnen ontwerpen."
Toekomstig werk omvat onder meer het in beeld brengen van wat er gebeurt als zo'n miniatuurbatterij herhaaldelijk wordt opgeladen en ontladen. Wanneer een batterij wordt gebruikt, de lithiumionen moeten teruglopen door de tinoxidedraad en over de elektrolyt naar de positieve elektrode. Hoeveel structurele schade het terugtrekkende lithium in zijn kielzog achterlaat, zal onderzoekers helpen begrijpen waarom oplaadbare batterijen niet meer werken nadat ze zo vaak zijn opgeladen.
De onderzoekers willen ook een volledig functionerende oplaadbare batterij van nanoformaat ontwikkelen.
 Team gedecodeerd moleculair mechanisme dat zwermmotiliteit van bacteriële populaties remt
Team gedecodeerd moleculair mechanisme dat zwermmotiliteit van bacteriële populaties remt Onderzoekers ontwikkelen test van 15 minuten om immuunrespons te beoordelen
Onderzoekers ontwikkelen test van 15 minuten om immuunrespons te beoordelen Revolutionaire nieuwe materialen voor roerige koolstoftijden:superfilters die de wereld zich kan veroorloven
Revolutionaire nieuwe materialen voor roerige koolstoftijden:superfilters die de wereld zich kan veroorloven Het productieproces van rubber
Het productieproces van rubber Potentiële testartefacten bij antimalariascreening
Potentiële testartefacten bij antimalariascreening
 Chemische reacties die betrokken zijn bij de groei van planten
Chemische reacties die betrokken zijn bij de groei van planten Lijst met Woestijnen in India
Lijst met Woestijnen in India  Verklaring van een klimaatnoodsituatie en volgende stappen voor actie
Verklaring van een klimaatnoodsituatie en volgende stappen voor actie Koetoiletten in Nederland willen e-moo-sessies verminderen
Koetoiletten in Nederland willen e-moo-sessies verminderen Waarom voedingskeuzes een impact hebben op de wereldwijde fauna en menselijke populaties
Waarom voedingskeuzes een impact hebben op de wereldwijde fauna en menselijke populaties
Hoofdlijnen
- Zeegras is wereldwijd een belangrijk visgebied
- Hoe een zevende-graadsmodel van een dierencel te bouwen
- How Do Living Things Grow?
- Wat zijn natuurlijke polymeren?
Enkele van de meest voorkomende voorbeelden van polymeren zijn kunststoffen en eiwitten. Hoewel plastics het resultaat zijn van het industriële proces, zijn eiwitten rijk aan aard en worden ze daarom meestal als een
- Your Brain On: Exam Stress
- Twee hersengebieden werken samen om vinken te helpen weten wanneer en hoe ze hun liedjes moeten afstemmen op specifieke situaties
- Habitatverlies is de grootste bedreiging voor Australische soorten
- 10 manieren waarop uw geheugen volledig onnauwkeurig is
- Hoe Facebook kraakt over nepnieuws (en waarom nepnieuws werkt)
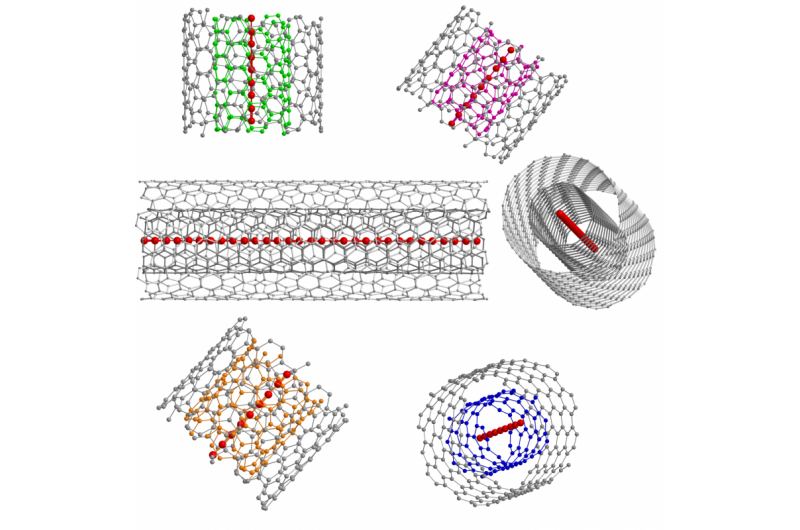
- Onderzoekers presenteren een direct eerste bewijs van stabiele, ultralange 1D-koolstofkettingen
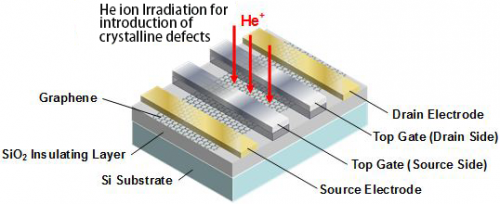
- Ontwikkeling van grafeentransistor met nieuw werkingsprincipe
- Onderzoek bootst hersencellen na om het geheugenvermogen te vergroten

- Onderzoekers gebruiken aluminium nanostructuren voor fotorealistisch printen van plasmonische kleurenpaletten

- Wetenschappers gebruiken DNA om een transistor te assembleren uit grafeen

 NASA vindt zware regen in orkaan Erick
NASA vindt zware regen in orkaan Erick Gentesten in de dokterspraktijk
Gentesten in de dokterspraktijk Hoge verwachtingen nu de nieuwe nachttrein van Oostenrijk vertrekt naar Brussel
Hoge verwachtingen nu de nieuwe nachttrein van Oostenrijk vertrekt naar Brussel Het middelpunt tussen twee nummers berekenen
Het middelpunt tussen twee nummers berekenen Zelfrijdende deeltjes kunnen condenseren door te draaien en naar drukke gebieden te bewegen
Zelfrijdende deeltjes kunnen condenseren door te draaien en naar drukke gebieden te bewegen Quasar met hoge roodverschuiving ontdekt door Pan-STARRS
Quasar met hoge roodverschuiving ontdekt door Pan-STARRS Kwantumsensor doorbraak met behulp van natuurlijk voorkomende trillingen in kunstmatige atomen
Kwantumsensor doorbraak met behulp van natuurlijk voorkomende trillingen in kunstmatige atomen Geneeskunde in de oudheid - van oude tempels tot Romeinse logistiek
Geneeskunde in de oudheid - van oude tempels tot Romeinse logistiek
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Swedish | German | Dutch | Norway | Portuguese | Danish |

-
Wetenschap © https://nl.scienceaq.com

