
Wetenschap
Bescheiden eiwit, nanodeeltjes tag-team om kankercellen te doden
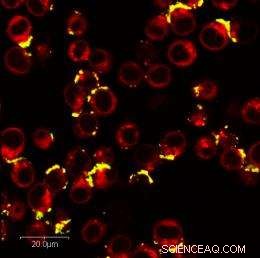
Transferrine-dragende nanodeeltjes die Ramos-kankercellen hebben getarget en doordrongen. Gele gebieden vertegenwoordigen de intracellulaire compartimenten van de cellen waar de nanodeeltjes zich bevinden. Rode gebieden vertegenwoordigen intracellulaire compartimenten zonder nanodeeltjes. Afbeelding:Shaomin Tian, UNC Chapel Hill.
(PhysOrg.com) -- Een normaal goedaardig eiwit dat in het menselijk lichaam wordt aangetroffen, lijkt in staat te zijn - in combinatie met nanodeeltjes - bepaalde kankercellen aan te vallen en te doden, zonder die deeltjes ook met chemotherapiemedicijnen te hoeven laden.
De bevinding zou kunnen leiden tot een nieuwe strategie voor gerichte kankertherapieën, volgens de wetenschappers van de Universiteit van North Carolina in Chapel Hill die de ontdekking deden.
Echter, ze waarschuwden ook dat het resultaat zorgen oproept over onverwachte "off-target" -effecten bij het ontwerpen van nano-aflevermiddelen.
transferrine, het vierde meest voorkomende eiwit in menselijk bloed, wordt al bijna twee decennia gebruikt als een middel om kankercellen af te leveren op tumoren. De receptor van het eiwit wordt tot overexpressie gebracht op het oppervlak van veel snelgroeiende kankercellen, dus behandelingen in combinatie met transferrineliganden kunnen ze opzoeken en eraan binden. Nanodeeltjes doordrenkt met transferrine worden lange tijd als veilig en niet-toxisch beschouwd.
Nutsvoorzieningen, UNC-onderzoekers hebben aangetoond dat, verrassend genoeg, het hechten van transferrine aan een oppervlak van nanodeeltjes kan B-cellymfoomcellen effectief en selectief targeten en doden, gevonden in een agressieve vorm van non-Hodgkin-lymfoom. Men dacht dat nanodeeltjes ook giftige chemotherapiemiddelen zouden moeten bevatten om zo'n effect te hebben.
De ontdekking werd gedaan door een team van onderzoekers onder leiding van Joseph DeSimone, doctoraat, Chancellor's Eminent Professor of Chemistry in UNC's College of Arts and Sciences en William R. Kenan Jr. Distinguished Professor of Chemical Engineering aan de North Carolina State University, samen met Jin Wang, doctoraat, en Shaomin Tian, doctoraat, in het laboratorium van DeSimone. Hun bevindingen verschijnen in het online nummer van deze week van de Tijdschrift van de American Chemical Society .
De wetenschappers zeggen dat het resultaat een interessante ontwikkeling is op het gebied van nanogeneeskunde, waarvan onderzoekers hopen dat ze uiteindelijk algemeen aanvaarde alternatieven - of vervangingen - voor chemo- en bestralingsbehandeling zullen bieden. Die therapieën, hoewel beschouwd als de meest effectieve methoden die momenteel beschikbaar zijn om kanker aan te pakken, ook vaak schade aan gezonde weefsels en organen als bijwerking.
Met behulp van de PRINT-technologie (Particle Replication in Non-wetting Templates) - een techniek die is uitgevonden in het laboratorium van DeSimone en waarmee wetenschappers nanodeeltjes met een goed gedefinieerde grootte en vorm kunnen produceren - produceerden de UNC-onderzoekers biocompatibele nanodeeltjes gebonden met humaan transferrine, en toonden aan dat de deeltjes veilig en nauwkeurig een breed spectrum van kankers kunnen herkennen. Evenals B-cellymfoomcellen, de deeltjes waren ook effectief gericht op niet-kleincellige longen, eierstok, lever- en prostaatkankercellen.
Over het algemeen, de nanodeeltjes waren niet-toxisch voor dergelijke cellen en zouden daarom moeten kunnen worden geladen met standaard chemotherapiemiddelen en worden gebruikt om die kankers aan te scherpen.
Echter, voor Ramos-cellen, een agressieve vorm van B-cellymfoom, de transferrine-gebonden PRINT-nanodeeltjes herkenden ze niet alleen, maar veroorzaakten ook celdood. In de tussentijd, vrij transferrine - dat werd geïncubeerd met Ramos-cellen maar niet gebonden aan nanodeeltjes - doodde geen Ramos-cellen, zelfs bij hoge concentraties.
Onderzoekers voeren verder onderzoek uit om te bepalen hoe en waarom de transferrine-dragende nanodeeltjes toxisch bleken voor de Ramos-cellen, maar niet voor de andere tumortypes.
"Hoewel dit potentieel opwindend is voor de ontwikkeling van geheel nieuwe strategieën voor de behandeling van bepaalde soorten lymfomen met mogelijk minder bijwerkingen, deze studie roept ook bezorgdheid op over onverwachte off-target effecten wanneer men gerichte chemotherapiemiddelen ontwerpt voor andere soorten kankers, ', aldus DeSimone. DeSimone is ook lid van UNC's Lineberger Comprehensive Cancer Center en de co-hoofdonderzoeker van het Carolina Center for Cancer Nanotechnology Excellence. Hij werd onlangs ook aangesteld als adjunct-lid bij het Memorial Sloan-Kettering Cancer Center in New York.
 Richten op maagkanker:nieuwe benadering van selectieve chemotherapie
Richten op maagkanker:nieuwe benadering van selectieve chemotherapie De toekomst ziet er rooskleurig uit voor oneindig recyclebaar plastic
De toekomst ziet er rooskleurig uit voor oneindig recyclebaar plastic De oorsprong van smaakafwijkingen in uien
De oorsprong van smaakafwijkingen in uien Wetenschappers gebruiken trechtervisie om goedkope en efficiënte zonne-energie te pionieren
Wetenschappers gebruiken trechtervisie om goedkope en efficiënte zonne-energie te pionieren Cyanobacteriën kunnen een revolutie teweegbrengen in de plasticindustrie
Cyanobacteriën kunnen een revolutie teweegbrengen in de plasticindustrie
 Onderzoek toont aan dat kosteneffectieve polymeerkit het verlies van irrigatiewater wereldwijd aanzienlijk kan verminderen
Onderzoek toont aan dat kosteneffectieve polymeerkit het verlies van irrigatiewater wereldwijd aanzienlijk kan verminderen Hoe onderscheid te maken tussen een mannelijke en vrouwelijke mus
Hoe onderscheid te maken tussen een mannelijke en vrouwelijke mus Vier feiten over de Stratosphere
Vier feiten over de Stratosphere Wat betekenen de cijfers in recyclingsymbolen op plastic artikelen?
Wat betekenen de cijfers in recyclingsymbolen op plastic artikelen?  Leeftijden van het Navajo-zandsteen
Leeftijden van het Navajo-zandsteen
Hoofdlijnen
- Microbiologie vs. Biochemie
- Hoe kan een mutatie in DNA invloed hebben op eiwitsynthese?
- Wat zijn de verschillen tussen PCR en klonen?
- Cavendish redden:team kweekt 's werelds eerste ziekteresistente bananen in Panama
- Gebruik van microscopen in de wetenschap
- Verschillen tussen een neuron en een neuroglia
- Sommige apen die vatbaar zijn voor isolatie
- Diepe wortels in planten aangedreven door bodemhydrologie
- DNA is digitaal geworden - wat kan er mis gaan?
- Gepulseerde lasers in vloeistoffen versnellen de jacht op effectieve katalysatoren

- Microscopische grafeenvlokken geïsoleerd in 2010 - nu zoekt wereldwijd onderzoek naar praktische toepassingen

- Wetenschappers ontwikkelen methode voor het observeren van nanokristalvorming met atomaire resolutie

- Gelatine-nanodeeltjes kunnen medicijnen in de hersenen afleveren

- Nanodeeltjestherapie richt zich op lymfekliermetastasen
 Thailand neemt grote slagtanden van olifanten in beslag ter waarde van meer dan $ 450, 000
Thailand neemt grote slagtanden van olifanten in beslag ter waarde van meer dan $ 450, 000 Waar is uranium voor gebruikt?
Waar is uranium voor gebruikt?  IPCC-rapport schetst catastrofaal beeld van smeltend ijs en stijgende zeespiegel - en de realiteit kan nog erger zijn
IPCC-rapport schetst catastrofaal beeld van smeltend ijs en stijgende zeespiegel - en de realiteit kan nog erger zijn Covalent gemodificeerd tweedimensionaal arseen
Covalent gemodificeerd tweedimensionaal arseen Instructies voor een Egg Drop Science Fair Project
Instructies voor een Egg Drop Science Fair Project Zelfassemblerende nanodeeltjesarrays kunnen schakelen tussen een spiegel en een raam
Zelfassemblerende nanodeeltjesarrays kunnen schakelen tussen een spiegel en een raam Een niet-verslavende opioïde pijnstiller zonder bijwerkingen
Een niet-verslavende opioïde pijnstiller zonder bijwerkingen Natuurkundigen kwantificeren temperatuurveranderingen in metalen nanodraden
Natuurkundigen kwantificeren temperatuurveranderingen in metalen nanodraden
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

