
Wetenschap
Dual-Purpose Nanodeeltjes Spot resterende tumoren, Verbetert kankerchirurgie
(PhysOrg.com) -- De zekerste remedie voor kanker is om elk laatste stukje van een tumor te verwijderen door middel van een operatie. Helaas, voor de meeste kankers is dat ook de moeilijkste aanpak vanwege twee problemen:het is tegenwoordig bijna onmogelijk om elke laatste tumor in het lichaam te herkennen en het is vaak moeilijk om te bepalen waar een tumor stopt en gezond weefsel begint. Een oplossing voor beide problemen kan voorhanden zijn in de vorm van een nanodeeltje voor twee doeleinden dat tumorcellen binnendringt en ze verlicht met behulp van fluorescentiebeeldvorming of magnetische resonantiebeeldvorming (MRI).
Een team van onderzoekers onder leiding van Roger Tsien, doctoraat, een lid van het door het National Cancer Institute gefinancierde centrum voor nanotechnologie voor behandeling, Begrip, en monitoring van kanker aan de Universiteit van Californië, San Diego, ontwikkelde een nanodeeltje voor twee doeleinden dat alleen cellen binnendringt die zijn bedekt met twee eiwitten die tumorcellen gebruiken om gezond weefsel binnen te dringen. Zodra de nanodeeltjes zich ophopen in tumorcellen, ze worden gemakkelijk zichtbaar met behulp van MRI of een standaard fluorescentiemicroscoop. De onderzoekers melden dat ze tumoren met een diameter tot 200 micron kunnen opsporen, en dat ze vervolgens zelfs microscopisch kleine sporen van kwaadaardig weefsel kunnen verwijderen door het fluorescentiesignaal te volgen dat de nanodeeltjes uitzenden. Dr. Tsien en zijn collega's rapporteren hun werk in back-to-back papers die verschijnen in de Proceedings van de National Academy of Sciences .
De onderzoekers bouwden hun sonde met behulp van een bolvormig polymeer nanodeeltje dat bekend staat als een dendrimeer. Dendrimeren hebben talrijke chemische verbindingen op hun oppervlak, waardoor het team van Dr. Tsien drie verschillende entiteiten aan elk nanodeeltje kon hechten:een activeerbaar celpenetrerend peptide (ACPP); drie moleculen van de fel fluorescerende kleurstof die bekend staat als Cy5; en 15-30 moleculen gadoliniumchelaat, een krachtig MRI-contrastmiddel, aan elk nanodeeltje.
ACPP's zijn kort, positief geladen peptiden gekoppeld door een splitsbaar molecuul aan een tweede negatief geladen peptide. Positief geladen peptiden staan bekend om hun vermogen om cellen binnen te dringen, maar in de geïnactiveerde toestand blokkeert het gekoppelde negatief geladen peptide de celpenetratie. Het splitsen van de linker verwijdert het negatief geladen peptide, waardoor het resterende positief geladen peptide - en eventuele aangehechte lading - de cellen kan binnendringen. In dit geval, de linker wordt alleen gesplitst door een van de twee eiwitten - matrix metalloproteïne-2 of matrix metalloproteïne-9 - die in grote aantallen aanwezig zijn op het oppervlak van tumorcellen. Als gevolg van deze specificiteit, nanodeeltjes die aan dit ACPP zijn gehecht, komen alleen tumorcellen binnen. Nanodeeltjes gehecht aan een soortgelijk peptide, maar een die niet kan worden gespleten, kwamen niet in de tumorcellen en werden snel uit het lichaam verwijderd.
Wanneer geïnjecteerd in dieren met menselijke tumoren, de nanodeeltjes verzamelden zich gedurende 48 uur in tumoren en waren gemakkelijk zichtbaar met behulp van MRI van het hele lichaam. Toen de onderzoekers dit experiment uitvoerden, ze zagen heldere randen rond zelfs kleine tumoren. Bij nader onderzoek met behulp van fluorescentiemicroscopie, de onderzoekers waren in staat om de gekartelde randen van tumoren duidelijk af te bakenen.
Met behulp van de heldere fluorescerende randen als richtlijn, de onderzoekers waren toen in staat om een meer complete tumorverwijdering te bereiken dan mogelijk was zonder begeleiding van nanodeeltjes. Tumordragende muizen die de nanodeeltjes voorafgaand aan de operatie ontvingen, hadden een betere lange termijn tumorvrije overleving en algehele overleving dan dieren waarvan de tumoren werden verwijderd met behulp van traditionele fellichtverlichting. De onderzoekers werden gedocumenteerd met behulp van follow-up-MRI dat ze alle tumoren tijdens de operatie hadden verwijderd.
Dit werk wordt gedetailleerd beschreven in twee papers. De eerste is getiteld, "Activeerbare celpenetrerende peptiden gekoppeld aan nanodeeltjes als dubbele sondes voor in vivo fluorescentie en MR-beeldvorming van proteasen, " en de tweede met de titel, "Chirurgie met moleculaire fluorescentiebeeldvorming met behulp van activeerbare celpenetrerende peptiden vermindert de resterende kanker en verbetert de overleving."
 Deep learning en holografie creëren een betere point-of-care-sensor
Deep learning en holografie creëren een betere point-of-care-sensor Gemultiplexte biosensoren in het voordeel van de gezondheidszorg
Gemultiplexte biosensoren in het voordeel van de gezondheidszorg Elektronenkristallografie bleek net zo goed te werken als röntgenkristallografie alleen op kleinere kristallen
Elektronenkristallografie bleek net zo goed te werken als röntgenkristallografie alleen op kleinere kristallen Een thermometer maken voor kinderen
Een thermometer maken voor kinderen Effect van menselijke activiteiten op het milieu
Effect van menselijke activiteiten op het milieu
 Satellieten gebruiken om schattingen van gewasopbrengsten te verbeteren
Satellieten gebruiken om schattingen van gewasopbrengsten te verbeteren Rambowortel kan helpen bij klimaatactie, vredesopbouw, en milieukwesties
Rambowortel kan helpen bij klimaatactie, vredesopbouw, en milieukwesties Arctisch onderzoek om licht te werpen op organismen die essentieel zijn voor de voedselketen
Arctisch onderzoek om licht te werpen op organismen die essentieel zijn voor de voedselketen Hoe mangroven mensen beschermen tegen steeds frequentere en krachtigere tropische stormen
Hoe mangroven mensen beschermen tegen steeds frequentere en krachtigere tropische stormen De grootste dataset voor het zoutgehalte van het zeeoppervlak tot nu toe helpt onderzoekers om zoute wateren in kaart te brengen
De grootste dataset voor het zoutgehalte van het zeeoppervlak tot nu toe helpt onderzoekers om zoute wateren in kaart te brengen
Hoofdlijnen
- Waarom is bioinformatica belangrijk in genetisch onderzoek?
- Hoe succesvol te zijn in Microbiology
- Studie werpt nieuw licht op de overleving van krilllarven
- Killer-tandpijn veroorzaakt waarschijnlijk ellende voor orka's in gevangenschap
- Wetenschappers onderzoeken mysteries achter diversiteit van DNA-samenstelling tussen soorten
- Woedend debat:houdt het ruimen van wolven stroperij tegen?
- Net als doorgewinterde vakantieliefhebbers, majoid krabben versieren hun schelpen
- Wat is het doel van ademhaling?
- Hoe is de concentratie van een oplossing van invloed op osmose?
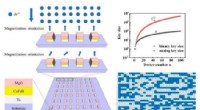
- Zeer veilige fysiek niet-kloneerbare cryptografische primitieven op basis van grensvlakmagnetische anisotropie
- Implantaat om hersenchemicaliën beter op te sporen na neurotrauma

- Nieuw composietmateriaal stimuleert het streven naar geavanceerde elektrische voertuigen

- Bacterieel nanometrisch amorf Fe-gebaseerd oxide als anodemateriaal voor lithium-ionbatterijen

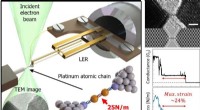
- Aan een zijden draadje hangen:beeldvorming en sondeerketens van enkele atomen
 Klimaat om de theeproductie in Kenia te verwoesten
Klimaat om de theeproductie in Kenia te verwoesten Kunnen astronauten sterren zien vanuit het ruimtestation?
Kunnen astronauten sterren zien vanuit het ruimtestation? Je hebt alle 6 stukjes van de puzzel nodig om stedelijke veerkracht op te bouwen, maar al te vaak is het de politiek die een gat laat?
Je hebt alle 6 stukjes van de puzzel nodig om stedelijke veerkracht op te bouwen, maar al te vaak is het de politiek die een gat laat? De behoefte aan elementaire wiskunde en wetenschappelijke vaardigheden in studenten
De behoefte aan elementaire wiskunde en wetenschappelijke vaardigheden in studenten
Voor studenten die een graad in de humaniora volgen, lijken wiskunde- en bètaklassen misschien vervelend afleidend, en elementaire wiskundige en wetenschappelijke v
 Google gaat de strijd aan om de markt voor cloudgaming
Google gaat de strijd aan om de markt voor cloudgaming Titaniumkatalyse maakt stereoselectieve synthese van C-glycosiden en glycopeptiden mogelijk
Titaniumkatalyse maakt stereoselectieve synthese van C-glycosiden en glycopeptiden mogelijk Meer wetenschap in de kunst van het maken van nanokristallen
Meer wetenschap in de kunst van het maken van nanokristallen NASA analyseert zware regenval in Kammuris
NASA analyseert zware regenval in Kammuris
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Portuguese | Swedish | German | Dutch | Danish | Norway | Spanish |

-
Wetenschap © https://nl.scienceaq.com

