
Wetenschap
Hoe wordt H2CO3 in de natuur gevormd?
Hier is het proces:
1. CO2 lost op in water: CO2 uit de atmosfeer lost op in regenwater en andere waterlichamen.
2. Vorming van carbonzuur: De opgeloste CO2 reageert met water om koolzuur te vormen (H2CO3). Deze reactie is omkeerbaar en wordt beschreven door het volgende evenwicht:
CO2 (aq) + H2O (l) ⇌ H2CO3 (aq)
Sleutelpunten:
* Het evenwicht ligt zwaar in de richting van CO2 en water, wat betekent dat de meeste opgeloste CO2 blijft als CO2 -moleculen.
* De vorming van koolzuur is om verschillende redenen een cruciaal proces:
* verzuring van de oceaan: Naarmate meer CO2 oplost in de oceaan, neemt de pH af (wordt zuurder), wat invloed heeft op het leven op zee.
* verwering van rotsen: Koolzuurzuur draagt bij aan het verweren van rotsen, het vrijgeven van mineralen en het beïnvloeden van de vorming van grotten en andere geologische formaties.
* Vorming van bicarbonaationen: Koolzuurzuur kan een proton (H+) doneren om bicarbonaationen (HCO3-) te vormen die een cruciale rol spelen bij het bufferen van de pH van waterlichamen.
Samenvattend: Koolzuurzuur bestaat niet in de natuur in een pure vorm, maar wordt gevormd in water door de reactie van opgeloste CO2 en water. Deze reactie is cruciaal voor verschillende natuurlijke processen en heeft aanzienlijke gevolgen voor het milieu.
 Hoe zijn oceanen volgens de wetenschappelijke hypothese ontstaan?
Hoe zijn oceanen volgens de wetenschappelijke hypothese ontstaan?  Waterstofauto's voor de massa een stap dichter bij de realiteit, dankzij UCLA-uitvinding
Waterstofauto's voor de massa een stap dichter bij de realiteit, dankzij UCLA-uitvinding Is het waar dat tin meer waard is dan koper?
Is het waar dat tin meer waard is dan koper?  Nabij-infrarood fotoactiveerbare oxygenatiekatalysatoren van amyloïde peptide
Nabij-infrarood fotoactiveerbare oxygenatiekatalysatoren van amyloïde peptide Waarom zou je kristalstructuur bestuderen?
Waarom zou je kristalstructuur bestuderen?
 Hoe een kwelder in Massachusetts verandert wat we weten over de kust van New England
Hoe een kwelder in Massachusetts verandert wat we weten over de kust van New England Waar past een sneeuwuil in een voedselweb?
Waar past een sneeuwuil in een voedselweb?  Wetenschappers boren al 50 jaar in de oceaanbodem - dit is wat ze tot nu toe hebben gevonden
Wetenschappers boren al 50 jaar in de oceaanbodem - dit is wat ze tot nu toe hebben gevonden Slimme steden en de kwaliteit van leven in Gauteng . na de apartheid
Slimme steden en de kwaliteit van leven in Gauteng . na de apartheid Aandacht voor gezondheid bij het overstappen op schonere elektriciteit
Aandacht voor gezondheid bij het overstappen op schonere elektriciteit
Hoofdlijnen
- Wat is het zelfstandig naamwoord van de wetenschap?
- Hoe gebruiken wetenschappers tegenwoordig de evolutietheorie van Charles Darwin?
- Is teamwetenschap productief? Studie meet het collaboratieve karakter van translationele geneeskunde
- Wat scheidt de intracellulaire en extracellulaire vloeistofcompartimenten?
- De buitenste laag van een dierlijke cel?
- Wat is de naam van wetenschapper die dinosaurussen bestudeert?
- Wat is de term van somatische diploïde kern?
- Doorbraak laat zien hoe DNA wordt 'bewerkt' om genetische ziekten te corrigeren
- Bevat een skeletspiervezel veel kernen?
- Kabul verslikt zich in vuile lucht terwijl de temperatuur daalt

- Expeditie wil ontdekken hoe smeltend ijs de aanvoer van voedingsstoffen in de zee beïnvloedt

- Wind van verandering zorgt voor alarmerend tempo van de opwarming van de oceaan

- Verbijsterd door olieramp, sommigen in Huntington Beach zeggen dat het tijd is om offshore-boringen te beëindigen

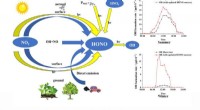
- Atmosferische salpeterigzuurchemie onthult een aanzienlijk onderschatte oxidatiecapaciteit in Noord-China
 Waarom het een goed idee is om met je dronken oom over politiek te praten
Waarom het een goed idee is om met je dronken oom over politiek te praten  Wat zijn de drie belangrijkste soorten soorten die in een gemeenschap optreden?
Wat zijn de drie belangrijkste soorten soorten die in een gemeenschap optreden?  Hoeveel voor die Nobelprijs in de etalage?
Hoeveel voor die Nobelprijs in de etalage?  Wat is de methode om het mengsel te scheiden?
Wat is de methode om het mengsel te scheiden?  Hersenachtige computers van legers komen dichter bij het kraken van codes
Hersenachtige computers van legers komen dichter bij het kraken van codes Inningswetten voor internetverkoop worden geleidelijk van kracht
Inningswetten voor internetverkoop worden geleidelijk van kracht Een psychotherapeut legt uit waarom sommige volwassenen slecht reageren op jonge klimaatstakers
Een psychotherapeut legt uit waarom sommige volwassenen slecht reageren op jonge klimaatstakers Stimulans voor het aanpassen van woningen kan ook de energierekening en ongelijkheid verminderen
Stimulans voor het aanpassen van woningen kan ook de energierekening en ongelijkheid verminderen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

