
Wetenschap
Voor de reactie A op producten worden opeenvolgende halfwaardetijden waargenomen van 10 minuten en 40 van 0,10 M aan het begin van Wat is de geïntegreerde snelheidswet, welke constante?
$$ln[A]_t =-kt + ln[A]_0$$
waar:
* $[A]_t$ is de concentratie van reactant A op tijdstip t
* $k$ is de snelheidsconstante
* $[A]_0$ is de initiële concentratie van reactant A
Er wordt gegeven dat de opeenvolgende halfwaardetijden van de reactie 10 minuten en 40 minuten zijn. De halfwaardetijd van een eerste orde reactie wordt gegeven door:
$$t_{1/2} =\frac{ln2}{k}$$
waar:
* $t_{1/2}$ is de halfwaardetijd van de reactie
* $k$ is de snelheidsconstante
We kunnen de gegeven halfwaardetijden gebruiken om de snelheidsconstante te berekenen:
$$k =\frac{ln2}{t_{1/2}}$$
$$k =\frac{ln2}{40 \ min} =1,15 \times 10^{-2} min^{-1}$$
Er wordt ook gegeven dat de initiële concentratie van reactant A 0,10 M was. We kunnen deze informatie gebruiken om de concentratie van A op elk moment t te berekenen:
$$ln[A]_t =-kt + ln[A]_0$$
$$ln[A]_t =-1,15 \maal 10^{-2} min^{-1} \maal t + ln(0,10 M)$$
$$[A]_t =e^{-1,15 \tijden 10^{-2} min^{-1} \tijden t + ln(0,10 M)}$$
Dit is de geïntegreerde tariefwet voor de reactie van A op Producten.
 Orkaanrecords gebroken in 2017
Orkaanrecords gebroken in 2017 Over het hoofd geziene trends in jaarlijkse neerslag onthullen wereldwijd onderschatte risico's
Over het hoofd geziene trends in jaarlijkse neerslag onthullen wereldwijd onderschatte risico's Giftige, brandwerende chemicaliën kunnen worden geabsorbeerd door aanraking, zo blijkt uit een 3D-geprint huidmodel
Giftige, brandwerende chemicaliën kunnen worden geabsorbeerd door aanraking, zo blijkt uit een 3D-geprint huidmodel  Zo heet dat je niet kunt ademen:extreme hitte treft de Filipijnen
Zo heet dat je niet kunt ademen:extreme hitte treft de Filipijnen  Oude bergen vastgelegd in Antarctische zandsteen onthullen mogelijke verbanden met wereldwijde gebeurtenissen
Oude bergen vastgelegd in Antarctische zandsteen onthullen mogelijke verbanden met wereldwijde gebeurtenissen
Hoofdlijnen
- Het grootste deel van het graasland voor rendieren staat onder cumulatieve druk
- Herstel van de Braziliaanse Spixs-ara, gepopulariseerd in geanimeerde Rio-films, bedreigd door klimaatverandering
- Waar in de cel worden enzymen gevonden die reacties van glycolyse katalyseren?
- De toekomst zaaien? Ark conserven zeldzaam, bedreigde planten
- Internationaal team kraakt genomische code voor vroegste vormen van terrestrische planten
- Voorbeelden van genetische kenmerken
- Hoe evolueerden zenuwstelsels, met hun ongelooflijke complexiteit, tussen verschillende soorten?
- Wat is een verandering in de DNA-code?
- Natuurbehoud werkt, en we worden er steeds beter in, zegt nieuw onderzoek
- Waarnemen van materie-golfdiffractie vanuit een periodieke reeks halve vlakken

- Natuurkunde Nobel-beloningen werken aan complexe systemen, zoals klimaat

- Quantum internet wordt hybride

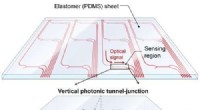
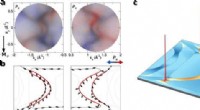
- Optische drukdetector kan de robothuid verbeteren, draagbare apparaten en aanraakschermen
- Exotisch elektronisch effect gevonden in 2D-topologisch materiaal
 Wat zijn de kenmerken van een elektromagneet?
Wat zijn de kenmerken van een elektromagneet?  Soorten Bobcats in Pennsylvania
Soorten Bobcats in Pennsylvania  LAMOST publiceert zijn zesde gegevens internationaal
LAMOST publiceert zijn zesde gegevens internationaal Een zeldzame en weinig bekende groep apen zou de tropische bossen in Afrika kunnen helpen redden
Een zeldzame en weinig bekende groep apen zou de tropische bossen in Afrika kunnen helpen redden  Helpt het antiparasitaire medicijn te verminderen
Helpt het antiparasitaire medicijn te verminderen Is calciumoxide zuur of alkali?
Is calciumoxide zuur of alkali?  Wrijving in het vacuüm?
Wrijving in het vacuüm?  Negatieve nummers splitsen
Negatieve nummers splitsen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

